NEJM:新冠病毒疫苗NVX-CoV2373的1-2期临床试验结果
2020-09-03 QQY MedSci原创
本试验是一项1-2期的随机对照试验,评估了重症急性呼吸综合征冠状病毒2(rSARS-CoV-2)的纳米颗粒疫苗NVX-CoV2373的安全性和免疫原性。

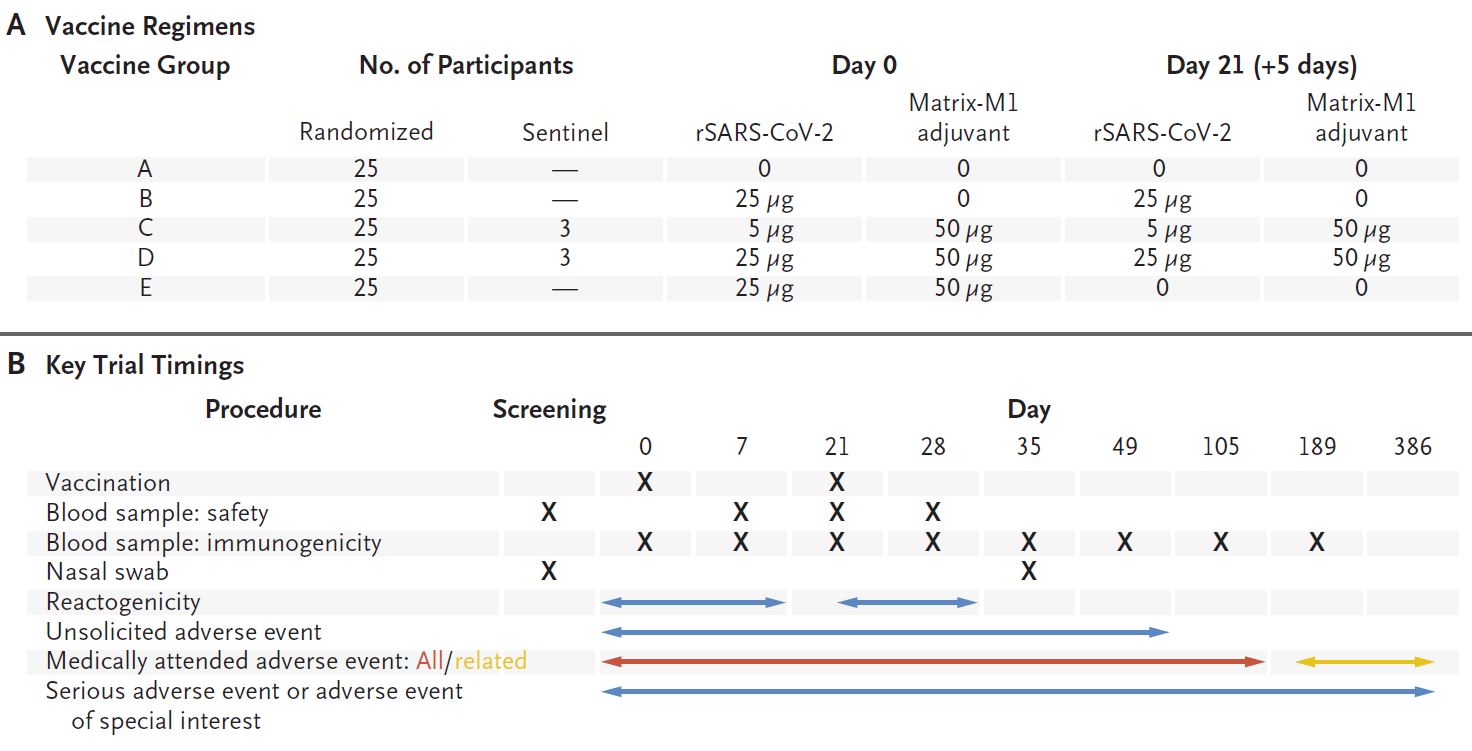
研究人员开展了一项随机的安慰剂为对照的1-2期试验,以评估rSARS-CoV-2疫苗的安全性和免疫原性。招募了131位健康成年人。在1期时,疫苗接种分为两次肌肉注射(5 μg 或25 μg,有或无Matrix-M1佐剂),间隔21天。主要预后为反应原性;实验室评估(血清生化和血液学),并根据FDA毒性评分评估安全性;IgG 抗棘突蛋白反应(ELISA)。次要预后包括不良反应、野生型病毒中和(微量中和试验)和T细胞反应(细胞因子染色)。
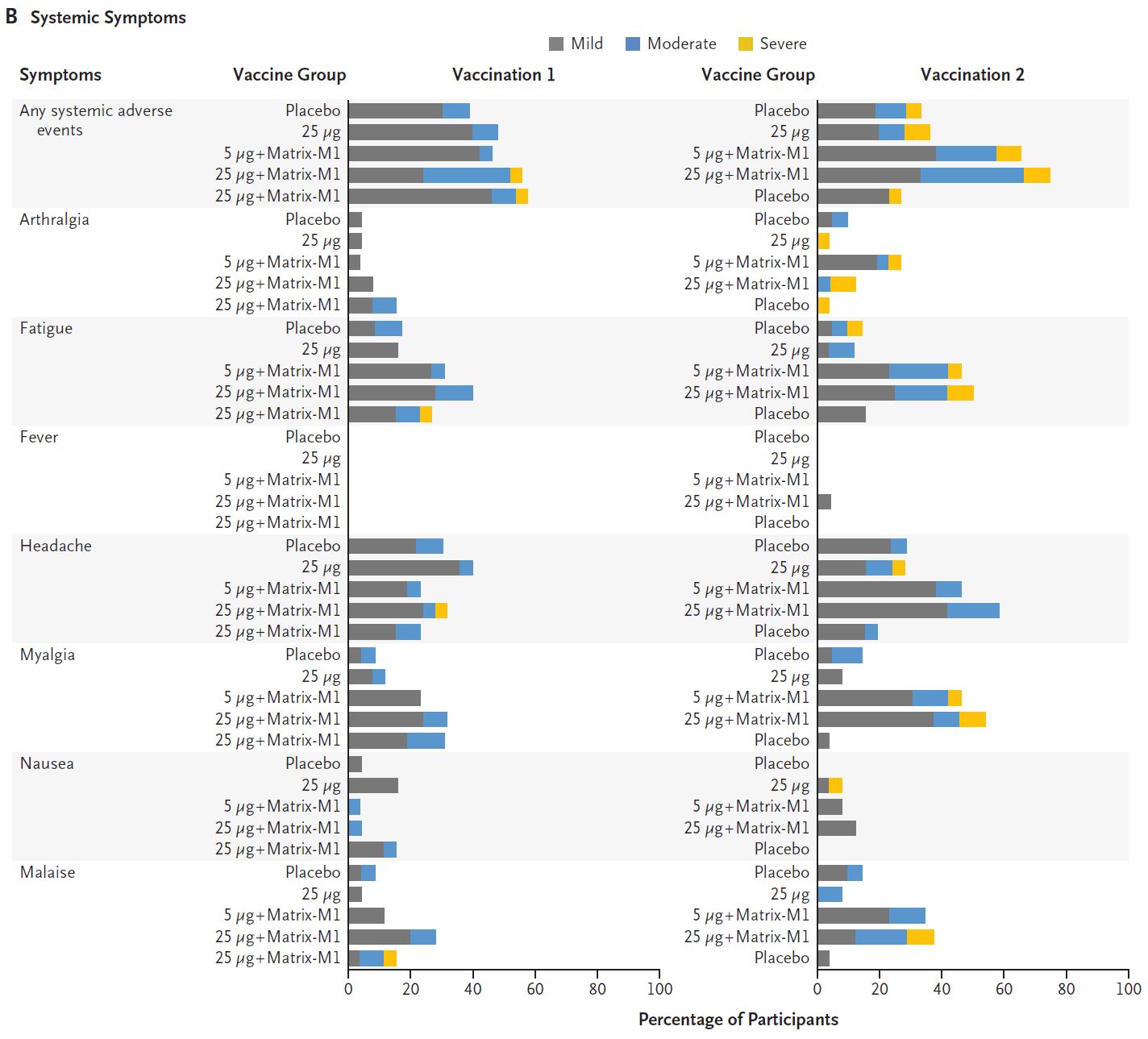
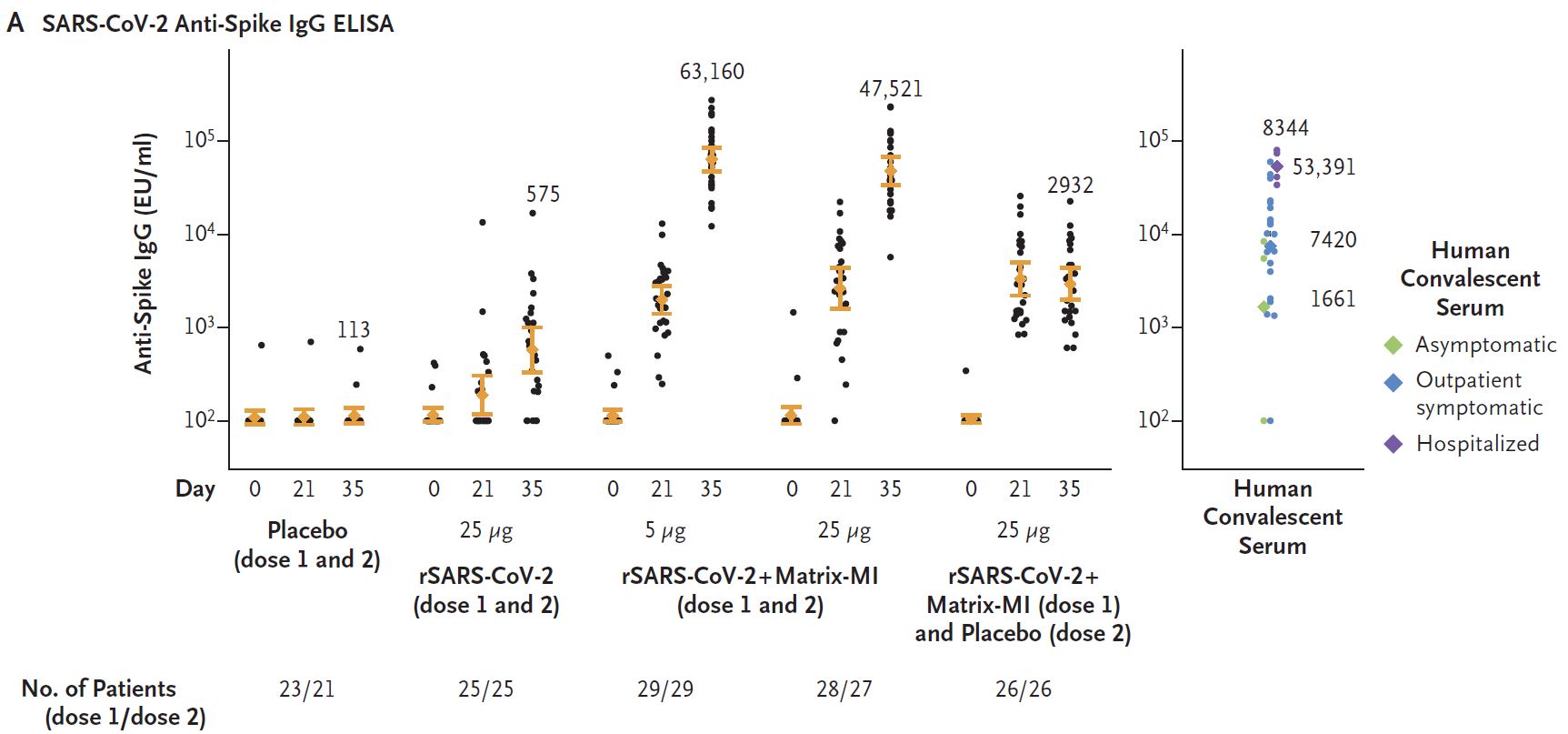
两剂5 μg的佐剂方案诱导的几何平均抗棘突IgG (63160 ELISA单位)和中和反应(3906)即可超过大多数有症状的Covid-19患者在恢复期血清中的反应水平(8344和983)。
原始出处:
C. Keech, et al. Phase 1–2 Trial of a SARS-CoV-2 Recombinant Spike Protein Nanoparticle Vaccine. The New England Journal of Medicine. September 2,2020. DOI: 10.1056/NEJMoa2026920
作者:QQY
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





#2期临床#
88
#病毒疫苗#
56
#NVX-CoV2373#
75
期待上市
126
#新冠病毒疫苗#值得期待
248