Nature:重磅:华人学者联手阐明黑色素瘤复发机制
2017-09-28 佚名 药明康德
黑色素瘤是一种致命的皮肤癌,威胁了大量患者的生命。2014年,针对BRAF与MEK的组合疗法进入市场,给了患者新的希望——即便是黑色素瘤出现转移的晚期癌症患者,也能从这些疗法中受益。然而好景不长。医生们发现,尽管能控制病情,尽管能延长患者的生命,黑色素瘤却总能在治疗的几个月后卷土重来,这也让研究人员们百思不得其解。
黑色素瘤是一种致命的皮肤癌,威胁了大量患者的生命。2014年,针对BRAF与MEK的组合疗法进入市场,给了患者新的希望——即便是黑色素瘤出现转移的晚期癌症患者,也能从这些疗法中受益。然而好景不长。医生们发现,尽管能控制病情,尽管能延长患者的生命,黑色素瘤却总能在治疗的几个月后卷土重来,这也让研究人员们百思不得其解。
今日,顶尖学术期刊《自然》上刊登了一项来自华人学者联手带来的研究。宾夕法尼亚大学(University of Pennsylvania)的郭巍教授、徐小威教授与Wistar研究所的Meenhard Herlyn教授一道,阐明了黑色素瘤复发的分子机理。这对这种恶性癌症的治疗有着极为重要的指导意义。
先来说黑色素瘤。据估计,大约有一半的黑色素瘤是由BRAF基因突变所引起的。这个基因编码了MAPK/ERK信号通路里的一个酶。当它发生突变时,会导致这条通路过度活跃,诱发细胞生长,导致癌症。因此,许多针对黑色素瘤的新药,背后的机理正是抑制BRAF。诚然,这些疗法取得了一些成功,但仍然有一些患者对这种治疗完全没有反应,而许多病情一度得到缓解的患者,最终也难免会产生耐药,让疗法失去作用。
既然独木难支,那就双管齐下。为了增强BRAF抑制剂的效果,最近新药研发人员又开发出了一类新药,它们能抑制BRAF/MEK通路下游的酶。目前,BRAF抑制剂与MEK抑制剂的组合对于晚期黑色素瘤患者来说是最有力的治疗方案之一,但研究人员们沮丧地发现,如同BRAF抑制剂一样,组合疗法的效果同样转瞬即逝。
我们当然可以继续开发第三、第四种针对同一通路的抑制剂,并期待奇迹发生,但这并不是一个理性的做法。一方面来说,越多的药物,可能带来越多的副作用;另一方面,谁能保证研发人员花了10年辛苦开发出来的新药,不会在区区几个月后诱生出耐药的癌细胞呢?
为此,科学家们转化了思路,寻找黑色素瘤耐药复发的根本原因。几年前,郭巍教授团队发现,耐药的黑色素瘤细胞比普通黑色素瘤细胞长得更为凶猛,这让他产生了深深的好奇。为了了解这些癌细胞究竟发生了什么,他与徐小威教授、Herlyn教授开展合作,寻找背后的生物学原因。
首先,他们从黑色素瘤患者中提取了两批癌细胞,第一批是在治疗前提取的,第二批是在经过了BRAF抑制剂疗法,或是BRAF/MEK抑制剂组合疗法后提取的。通过比较这两批细胞的不同,研究人员们意外发现,黑色素瘤在接受单药治疗和接受组合治疗后,产生耐药的机制竟截然不同!
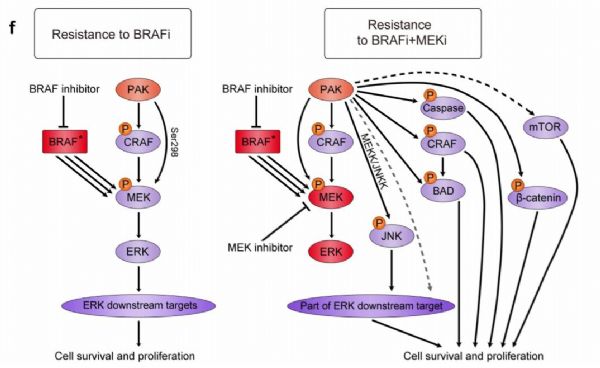
在仅接受了BRAF抑制剂治疗的黑色素瘤中,研究人员们发现癌细胞内的ERK蛋白被重新激活。这是一个BRAF的下游蛋白,可以规避BRAF的抑制,从机理上说合情合理。先前,其他课题组的研究也证实了这一点。
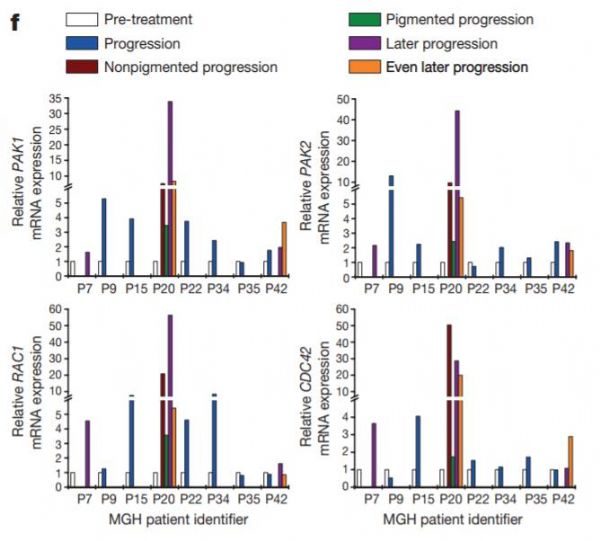
但是,在接受了组合疗法治疗的黑色素瘤里,意想不到的情况发生了!研究人员们发现,ERK蛋白并没有在这些癌细胞内被激活。相反,另一条控制细胞生长的通路——PAK通路得到了激活。
“我们不仅发现PAK酶被激活,它的许多下游靶点也得到了激活。” 郭巍教授说。
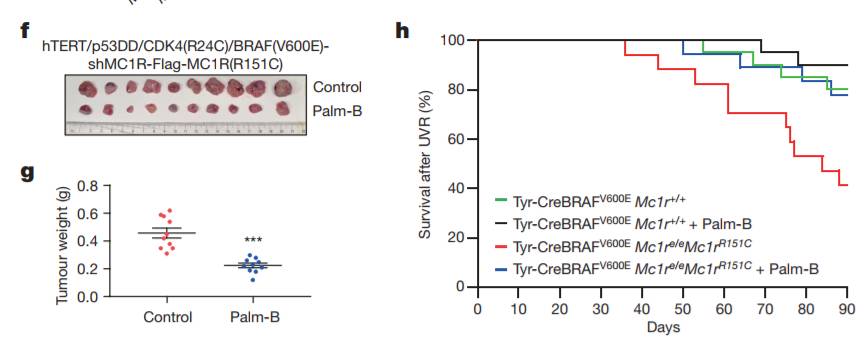
这条通路是否是黑色素瘤产生耐药的关键呢?为了回答这个问题,研究人员们又进行了进一步的实验。首先,他们在BRAF/MEK组合疗法之外,进一步使用了PAK抑制剂。结果表明,这些癌细胞的生长能力果然得到了抑制。相反,当他们激活转移性黑色素瘤细胞中的PAK蛋白后,这些癌细胞对MAPK通路的抑制剂更为耐受。这些结果清楚地表明,PAK通路的额外激活是BRAF/MEK疗法耐药的重要原因。
“这些癌细胞很聪明。当一条信号通路被抑制时,第二条信号通路就会激活,带来更具侵略性的疾病,” 郭巍教授说:“只有当ERK通路被抑制时,PAK通路才会苏醒。这时使用PAK抑制剂,就能看到疗效。”
“黑色素瘤细胞能重新编排信号通路。我们的发现提供了一种针对黑色素瘤的迂回策略,”Herlyn教授评论道:“癌症很聪明,我们要比癌症更聪明。”
“我们的发现有望带来针对PAK的新药开发。” 徐小威教授补充道。
正如徐小威教授所说的那样,这个发现能让人们重新审视PAK通路的重要性。有趣的是,癌症研究人员过去曾尝试开发过PAK抑制剂,但抗癌效果极为一般。现在我们知道,想要让PAK抑制剂起效,我们还得抑制BRAF/MEK通路。幸运的是,我们已经有了这些药物。
原始出处:
Lu H1, Liu S, Zhang G, Bin Wu, et al.PAK signalling drives acquired drug resistance to MAPK inhibitors in BRAF-mutant melanomas.Nature. 2017 Sep 27. doi: 10.1038/nature24040. [Epub ahead of print]
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
小提示:本篇资讯需要登录阅读,点击跳转登录







#Nat#
56
#复发机制#
71
#色素#
58
#重磅#
0
#黑色素#
64