Cell Rep:病毒学国家重点实验室刘昱课题组在抗病毒天然免疫方面取得新进展
2019-01-21 佚名 病毒学国重室
近日,病毒学国家重点实验室刘昱教授课题组在国际学术期刊Cell Reports上在线发表了最新研究成果,论文题为“TMED2 potentiates cellular IFN responses to DNA viruses by reinforcing MITA dimerization and facilitating its trafficking”。
近日,病毒学国家重点实验室刘昱教授课题组在国际学术期刊Cell Reports上在线发表了最新研究成果,论文题为“TMED2 potentiates cellular IFN responses to DNA viruses by reinforcing MITA dimerization and facilitating its trafficking”。
DNA病毒感染宿主细胞后,细胞质内模式识别受体cGAS识别病毒DNA后催化胞质内ATP和GTP合成cGAMP。cGAMP作为胞内第二信使活化位于内质网(ER)上的接头蛋白MITA(又称为STING)。活化后的MITA增强自身二聚体形成,从ER经由高尔基体转运到核周小泡,并招募激酶TBK1和IKKe,形成MITA信号复合体。TBK1不仅磷酸化MITA,导致MITA进一步泛素化,也可磷酸化活化招募到复合体中的转录因子IRF3。
磷酸化的IRF3二聚化并转位到细胞核内,启动I型干扰素转录。MITA信号转导复合物的组装也诱导了NF-kB的激活,启动相关炎症因子和趋化因子的产生。IFN效应和炎症反应不仅作为机体天然免疫反应帮助机体抵御病毒入侵,也促进了适应性免疫的产生。由于MITA在抗DNA病毒信号通路中的重要作用,其表达和活化的调控机制一直是研究热点。
该研究利用双荧光素酶报告基因实验系统对人源cDNA文库进行了功能性筛选,获得了能明显协同cGAS-MITA激活ISRE启动子的分子TMED2。研究人员发现敲低或敲除TMED2明显抑制HSV-1感染诱导的MITA二聚化以及转录因子IRF3和NF-kB的活化,降低I型干扰素和炎症因子的相关基因转录;在TMED2敲除的细胞中HSV-1复制也明显增加,表明TMED2促进抗DNA病毒天然免疫信号通路。进一步的研究发现HSV-1感染诱导内源性TMED2与MITA在ER腔内发生相互作用。TMED2通过增强MITA与转位复合体关键成分TRAPb的相互作用,促进MITA翻译后从核糖体向ER转位;TMED2也通过强化MITA与COPII复合物成分Sec24C的相互作用,促进MITA经COPII复合物组装,由ER向高尔基体转运。该论文发现了MITA信号通路的新调控分子TMED2,并解析了其作用机制,为构建天然免疫信号转导调控网络提供重要支持,也为筛选抗病毒药物的分子靶点提供线索。
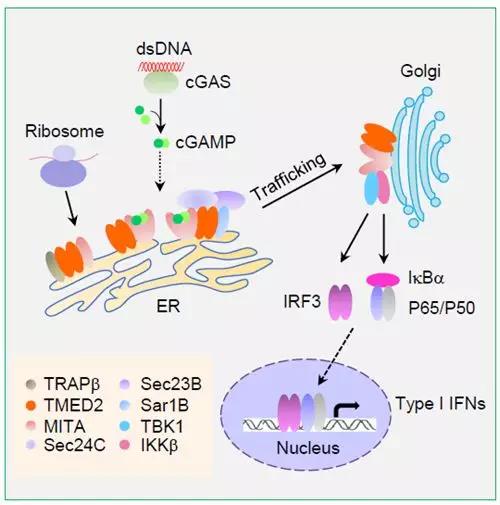
TMED2调控MITA作用机制的示意图
博士研究生孙明顺为本文第一作者。该研究得到国家自然科学基金(31770941,31521091)、国家重大基础研究计划(2014CB910103)、武汉大学自主科研基金(2042018kf0241)等项目资助。
原始出处:Sun MS1, Zhang J1, Jiang LQ1, et al. TMED2 Potentiates Cellular IFN Responses to DNA Viruses by Reinforcing MITA Dimerization and Facilitating Its Trafficking. Cell Rep. 2018 Dec 11;25(11):3086-3098.e3.
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#国家重点#
71
#CEL#
55
#Cell#
60
学习
113
#抗病毒#
0