JCO:3期临床试验| 吉西他滨+顺铂联合贝伐单抗治疗晚期尿路上皮癌
2021-05-15 Nebula MedSci原创
在GC方案中加入贝伐单抗并不能改善转移性尿路上皮癌患者的总生存期
自2016年批准了首个免疫检查点抑制剂应用与临床以来,转移性尿路上皮细胞(移行细胞)癌的治疗发生了重大变化;自此之后,已有7个新药获批用于治疗转移性尿路上皮癌。但是,以铂类为基础的联合化疗方案仍是尿路上皮癌的标准一线疗法。此外,吉西他滨和顺铂(GC)双化疗方案也已成为转移性尿路上皮癌的标准疗法。
基于血管生成在尿路上皮癌的生长和发展中的作用,Rosenberg等人开展了一项安慰剂为对照的随机试验,旨在评估GC方案联合贝伐单抗(GCB)vs GC方案+安慰剂(GCP)用于转移性尿路上皮癌的疗效。
2009年7月-2014年12月,共506位既往未针对转移病灶进行过化疗的、且在12个月内未进行过新辅助或辅助化疗的转移性尿路上皮癌患者被随机分至GCB组或GCP组。主要终点是总生存期(OS),次要终点是无进展生存期(PFS)、客观缓解率和毒性。
A:总生存期;B:无进展生存期
中位随访了76.3个月,接受GCB治疗的患者的中位OS为14.5个月,而接受GCP治疗的患者的中位OS为14.3个月(死亡风险比[HR] 0.87; 95% CI 0.72-1.05;p=0.14)。GCB组和GCP组的中位无进展生存期粪便是8.0个月和6.7个月(HR 0.77; 95% CI 0.63-0.95; p = 0.016)。
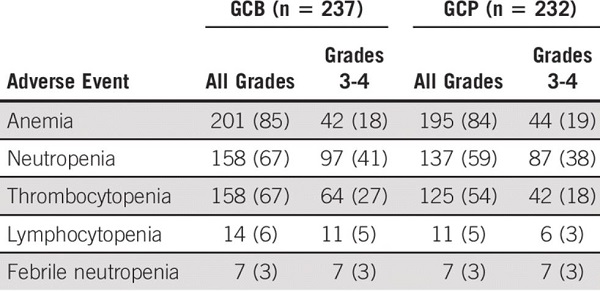
血液学不良反应
两个治疗臂的发生3级或以上不良反应事件的患者比例无明显差异,虽然贝伐单抗治疗组中贝伐单抗相关毒性(如高血压和蛋白尿)的发生次数增多。
综上所述,在GC方案中加入贝伐单抗并不能改善转移性尿路上皮癌患者的总生存期。本研究中的中位OS(14.5个月)与既往在以铂类为基础的化疗的3期临床试验中的结果一致。
原始出处:
Jonathan E. Rosenberg, et al. Randomized Phase III Trial of Gemcitabine and Cisplatin With Bevacizumab or Placebo in Patients With Advanced Urothelial Carcinoma: Results of CALGB 90601 (Alliance). Journal of Clinical Oncology. May 14, 2021. https://ascopubs.org/doi/full/10.1200/JCO.21.00286
作者:Nebula
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#铂#
74
#JCO#
76
#3期临床#
82
#晚期尿路上皮癌#
81
#贝伐#
74