免疫检查点疗法突破性进展一览
2017-01-22 佚名 生物谷
近些年来,随着科学家们研究的深入使得癌症免疫疗法取得了突飞猛进的发展,而“免疫监视”这一概念在临床中也产生了巨大的影响;如今位于免疫疗法前沿的的免疫检查点阻断剂在治疗人类很多癌症,尤其是恶性癌症以及化疗耐受性癌症的治疗上有着明显的效果;当然,其中治疗效果最明显的就是CTLA-4和PD-1两类免疫检查点阻断剂。 本文中,小编对近期免疫检查点疗法研究领域取得的进展进行了整理,分享给各位。

近些年来,随着科学家们研究的深入使得癌症免疫疗法取得了突飞猛进的发展,而“免疫监视”这一概念在临床中也产生了巨大的影响;如今位于免疫疗法前沿的的免疫检查点阻断剂在治疗人类很多癌症,尤其是恶性癌症以及化疗耐受性癌症的治疗上有着明显的效果;当然,其中治疗效果最明显的就是CTLA-4和PD-1两类免疫检查点阻断剂。
本文中,小编对近期免疫检查点疗法研究领域取得的进展进行了整理,分享给各位。
【1】J immunol:肿瘤免疫检查点疗法联合药物研究新进展
癌症免疫疗法对特定类型的癌症具有显著的治疗效果,但单一的免疫治疗策略往往治疗效果有限,因此,在实践中往往需要结合两种或多种免疫治疗手段进行癌细胞的杀伤。
Anti-CD40抗体是天然免疫与后天免疫的激活剂之一,它能够有效激活癌症患者中的抗肿瘤免疫反应。临床上该药物也能够延缓胰腺癌患者的发病时间。此外,小鼠水平的试验也表明抗CD40抗体能够有效激活巨噬细胞,而且在天然免疫刺激的共同作用下还能够有效延缓特定癌细胞的生长。
众所周知,CTLA-4与PD-1是最常见的免疫检查点疗法的靶点分子,特异性针对CTLA-4与PD-1的抗体能够有效促进T细胞的激活,并对癌细胞进行杀伤。
【2】Cell:肿瘤干扰素信号调节免疫检查点抑制剂抵抗性
doi:10.1016/j.cell.2016.11.022
一项新的临床前研究提示着一种现存的被称作JAK抑制剂的药物可能有助对所谓的检查点抑制剂免疫治疗药物不作出反应的病人克服这种耐药性。重要地,这些结果证实利用JAK抑制剂关闭在肿瘤对免疫治疗药物产生耐药性中起着至关重要作用的干扰素途径可能改善检查点抑制剂药物的疗效,甚至绕过对这些药物组合使用的需要,其中这种组合使用经常伴随着严重的副作用。相关研究结果发表在2016年12月1日那期Cell期刊上,论文标题为“Tumor Interferon Signaling Regulates a Multigenic Resistance Program to Immune Checkpoint Blockade”。
如今的检查点抑制剂药物靶向PD1和CTLA-4等受体,其中这些受体作为T细胞表面上的一种“关闭开关”阻止它攻击其他的细胞。利用一种或多种这样的药物抑制这些途径释放这些“车闸”,这样免疫系统才能够抵抗肿瘤。然而,一半以上依赖这些药物的病人发生病情复发,或者说,他们的癌症发生恶化。
【3】NEJM:联合使用免疫检查点抑制剂或导致癌症病人死于心脏副作用
利用两种通过批准的免疫治疗药物联合治疗癌症可能引起罕见但有时非常致命的心脏副作用,这种副作用的产生与一种意外的免疫应答有关。
在一项发表在国际学术期刊NEJM上的研究中,研究人员介绍了两名黑色素瘤病人在接受了ipilimumab和nivolumab这两种药物的联合治疗后意外出现急性心肌炎并发生死亡的病例。这两种药物都是FDA批准的免疫检查点抑制剂能够刺激病人的抗肿瘤应答。Ipilimumab是一种抗CTLA-4抗体,nivolumab是抗PD-1抗体。
这两种免疫检查点抑制剂药物的使用,特别是联合使用,能够增强对几种恶性癌症的治疗效果。这两种药物的常见副作用包括皮肤,结肠,肝脏,内分泌腺和肺部炎症,其原因可能是对免疫系统内T细胞的脱靶激活所导致。
【4】Science重磅研究揭示免疫检查点药物治疗癌症为何不能持久
T细胞能够负责清除感染杀伤肿瘤细胞,有时也会变得“疲劳”。细胞表面的一些受体作为天然存在的制动分子能够告诉免疫系统在正常情况下不要进行强烈反应,避免损伤健康组织或引起自身免疫疾病。阻断PD-1能够为疲劳的T 细胞重新注入活力,提高对慢性感染和癌症的控制能力。但是阻断PD-1能否对疲劳的T细胞进行重编程使其成为可持续存在的记忆T细胞,目前尚未可知。
来自宾夕法尼亚大学的研究人员发现,利用PD-L1阻断药物对小鼠进行治疗虽然可以使疲劳的T细胞重新恢复活力,但是几乎不会产生记忆T细胞。在进行治疗后,如果病毒抗原水平仍然很高,恢复活力的T细胞会再次变得疲劳;而病毒得到清除之后这些T 细胞也无法变成记忆T细胞。
相关研究结果发表在国际学术期刊Science上。
该团队发现疲劳的T细胞与效应T细胞和记忆T细胞具有不同的表观遗传学特征。后两种细胞类型能够对病毒和肿瘤发起有效的免疫应答,而疲劳的T细胞无法发挥该作用。疲劳的T细胞所具有的独特表观遗传学特征导致这些细胞表达了与效应T细胞和记忆T细胞所不同的一些基因,但是进行了PD-L1阻断之后其表观遗传学模式只发生了微小变化,这可能导致了疲劳T细胞无法变成效应T细胞或记忆T细胞。
【5】免疫检查点抗体副作用所引发的思考
免疫检查点抑制剂药物的成功上市,改变了实体瘤治疗的格局,展现出了巨大的前景。殊不知,免疫检查点抑制剂药物伴随的副作用会引发一系列问题。下面将为您梳理一下免疫检查点抗体治疗毒性作用与肿瘤治疗的错综复杂关系。
自从治疗转移性黑色素瘤的抗CTLA-4单抗药物ipilimumab被批准上市后,其他一系列药物,尤其是靶向PD-1/PD-L1通路,在治疗不同类型的肿瘤中均显示出较好的临床效果。此类药物可以重新激活免疫系统,但同时会导致新的免疫毒性作用,即免疫相关的副作用(irAEs)。irAEs涉及许多器官组织,处理方法完全不同于其他细胞毒性药物,irAEs需要肾上腺皮质素或者肿瘤坏死因子TNFα抗体等免疫抑制剂处理。
【6】癌症免疫检查点疗法的现状与展望
越来越多的证据表明,天然或诱导产生的免疫反应能够有效针对肿瘤抗原产生反应,从而杀伤肿瘤细胞。临床试验也表明,肿瘤组织间隙的免疫细胞浸润能够促进癌症患者的治疗效果。研究者们通过寻找在不同肿瘤组织中浸润的淋巴细胞的类型、功能和空间分布等信息,能够改善针对癌症患者的诊断与治疗方案的设计。伴随这些临床试验的进展,研究者们对癌症的"免疫监视(immunosurveillance)"现象开始越来越关注,即在除了少数特殊的环境下,肿瘤细胞能够被其特异性的免疫细胞杀伤。而上述的"特殊环境"指的是肿瘤微环境(TME)或癌症的免疫编辑作用造成免疫耐受性的细胞的产生。
过去几十年来,癌症的免疫疗法取得了突飞猛进的发展,"免疫监视"这一概念在临床上产生了巨大的现实意义。目前位于免疫疗法尖端的"免疫检查点阻断剂"对于很多癌症,尤其是恶性且化学药物耐受性癌症的治疗中有着明显的效果。其中,效果最显著的是"cytotoxic-T-lymphocyte-associated protein 4 (CTLA-4)"以及"programmed cell death 1 (PD-1)"两类免疫检查点阻断剂。
【7】首个小分子免疫检查点抑制剂IND获批
此前,Curis宣布,美国FDA已经接受了该公司产品CA-170的新药研究申请(IND)。总部位于美国马萨诸塞州莱克星顿的Curis是一家专注于人类癌症药物研究和开发的生物技术公司。CA-170是一剂口服小分子,用于靶向抑制免疫检查点程序性死亡配体-1(PD-L1)和 T细胞活化的免疫球蛋白抑制V型结构域(V-domain Immunoglobulin Suppressor of T-cell Activation,VISTA)。
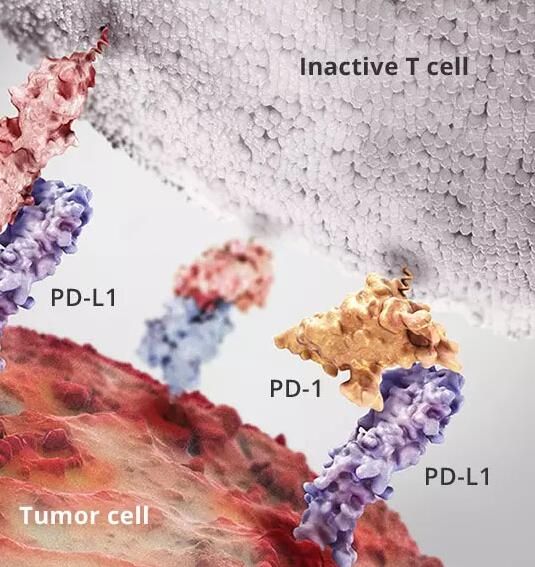
某些人类癌症肿瘤细胞会在细胞表面表达一种特殊的配体PD-L1,它可以结合存在于免疫系统T细胞表面的同源受体PD-1。肿瘤细胞和T细胞之间通过PD-L1 / PD-1分子的细胞表面相互作用往往导致T细胞失活,因此机体无法针对肿瘤产生有效免疫反应。众多研究显示由抗PD1抗体或抗PD-L1抗体介导的抑制调控可导致T细胞的活化,进而在肿瘤组织中观察到抗肿瘤作用。除了PD-L1 / PD-1以外,其它与免疫抑制相关的细胞表面分子,比如说VISTA也逐渐被发现。多个靶向PD-1 / PD-L1相互作用的治疗性单克隆抗体已被美国FDA批准上市。除了开发相关单克隆抗体之外,寻找方便癌症患者的口服小分子化合物用来靶向抑制免疫检查点也是肿瘤免疫疗法的前沿领域。小分子化合物能够穿过细胞膜作用于细胞内靶点,所以应用范围广泛。其次,小分子经化学修饰后往往具有良好的生物利用度和依从性,有效避免消化肠道中酶类的分解失活。最后,在生产工艺、剂型设计和给药方式等多种层面,小分子的研究也颇为成熟。Curis公司的在研新药CA-170被设计为一种能选择性靶向免疫激活的口服小分子药物。临床前数据表明,在细胞培养实验中,CA-170可通过抑制PD-L1或VISTA有效诱导免疫T细胞的增殖,以及细胞因子IFN-γ(γ干扰素)的产生。此外,CA-170在多个小鼠肿瘤模型中被证明了毒理学上的安全性。

【8】Immunity:免疫检查点调节因子为肿瘤免疫治疗提供新靶点
doi:10.1016/j.immuni.2016.04.015
最近,美国科学家发现了一种新的免疫应答调控因子,在这篇发表在国际学术期刊Immunity上的文章中,研究人员还对于T细胞为何无法清除慢性感染,消除肿瘤细胞的原因进行了解读。这些研究发现为许多临床背景下的T细胞应答调节开辟了新的道路。
T细胞是负责识别并清除特异性入侵者的免疫细胞,它们的活性受到高度调控--来自其他细胞的信号会调节T细胞应答进而对抗病原体。但是有时候这些应答很快就会消失,比如慢性病毒感染或癌症都会通过诱导T细胞紊乱导致免疫应答受阻。
近来一些阻断免疫检查点的新型药物的出现为肺癌以及黑色素瘤等特定类型癌症的治疗提供了新的改进方法。免疫检查点的作用类似于T细胞的制动系统,能够限制免疫系统对自身健康细胞进行攻击,防止自身免疫疾病的发生。
【9】Nature medcine:PD-1免疫检查点疗法可用于治疗老年痴呆症
doi:10.1038/nm.4022
慢性神经炎症反应常见于各类神经退行性疾病,而且是导致疾病恶化的重要因素。然而,虽然一些抗炎药物与免疫抑制疗法能够减轻部分神经退行性疾病的症状,但这些疗法在临床试验中大多以失败而告终。在小鼠阿兹海默症疾病模型中,单核细胞分化成的巨噬细胞向中枢神经系统(CNS)聚集能够保护神经系统免受损伤,然而后续的实验证明巨噬细胞的自发聚集不足以起到保护的作用。
最近,作者所在实验室利用五个家族性AD位点突变的阿兹海默症小鼠模型进行研究,发现FOXP3+ 的调节性T细胞(Treg)的暂时性缺失能够引发由IFN-gamma介导的系统性免疫反应以及大脑脉络丛的激活(这是一种能够引导淋巴细胞向中枢神经系统移动的途径)。后续伴随着巨噬细胞以及Treg细胞在中枢神经系统的聚集,最终导致大脑皮层老年斑(主要成分是β淀粉样蛋白)的清除以及神经退化症状的改善。因此,作者认为在神经退行性疾病发生过程中,系统性的免疫反应应该能够帮助大脑进行损伤修复。

【10】Nature medcine:CD47是癌症免疫检查点疗法的新型靶点
新闻阅读:CD47 blockade triggers T cell-mediated destruction of immunogenic tumors
CD47主要表达于癌细胞表面,通常被认为是癌细胞免于宿主免疫系统攻击的保护性受体。最近一项研究表明T细胞与树突状细胞(DC)可以通过CD47阻断效应发挥抗肿瘤的效应。
巨噬细胞发挥吞噬效应需要两个信号同时起作用:一个是靶向细胞表面的"eat me"信号的激活,另一个是同意目标表面"don't eat me"信号的失活。任何一个信号的缺少都不足以引发吞噬效应的发生。越来越多的证据表明,CD47是一类"don't eat me"信号,它通过与巨噬细胞表面的SIRP-α相互结合抑制巨噬细胞的同能。CD47作为癌症治疗的靶点具有不可比拟的优势:1.它广泛地表达于各类癌细胞表面,因此可以用于治疗各种类型的癌症;2. 正常细胞由于缺乏"eat me"signal,因此单单阻断CD47并不能引发巨噬细胞对正常细胞的吞噬效应,因此CD47阻断剂的副作用也十分小。前期的基础实验数据已经支持了这一观点。他们通过小鼠异体肿瘤移植模型说明了CD47阻断的有效性与安全性。事实上,目前已经有许多CD47抗体类药物进入了临床试验阶段。
【11】Science: 癌症免疫检查点疗法展望
免疫检查点疗法(immune chenkpoint therapy)是一类通过调节T细胞活性来提高抗肿瘤免疫反应的治疗方法。在最新一期的《科学》杂志中,来自美国MD.Anderson癌症中心的Padmanee Sharma与James P. Allison通过一篇综述文章分析了免疫检查点疗法的发展趋势。
目前,免疫检查点疗法已经加入了由手术,放疗,化疗,靶向治疗等组成的"抗癌大军"中。由FDA批准的三种免疫疗法药物中,一种是特异性结合T细胞表面CTLA-4受体的抗体类药物,叫做ipilimumab,于2011年得到批准。另外两种是特异性结合T细胞表面PD-1受体的抗体类药物,分别叫做pembrolizumab与nivolumab,于2014年得到批准。
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





#免疫检查点#
63
#免疫检查点疗法#
0