Leukemia :罗特西普用于骨髓增生异常综合征/骨髓增生性肿瘤伴环状铁粒幼细胞和血小板增多症
2022-03-03 MedSci原创 MedSci原创
骨髓增生异常综合征/骨髓增生性肿瘤伴环状铁粒幼细胞和血小板增多症 (MDS/MPN-RS-T) 是一种具有骨髓增生异常和骨髓增生特征的骨髓疾病。MDS/MPN-RS-T相关性贫血会导致疲劳、生活质量下

骨髓增生异常综合征/骨髓增生性肿瘤伴环状铁粒幼细胞和血小板增多症 (MDS/MPN-RS-T) 是一种具有骨髓增生异常和骨髓增生特征的骨髓疾病。MDS/MPN-RS-T相关性贫血会导致疲劳、生活质量下降和生存恶化,其治疗旨在改善贫血、降低血栓事件风险、降低血小板和/或改变病程。然而,支持这些治疗效果的数据很少。
罗特西普是一流的红细胞成熟剂,可结合多种转化生长因子-β 超家族配体,增强晚期红细胞生成。一项3 期 MEDALIST 研究 (NCT02631070)的结果使其获得美国食品和药物管理局和欧洲药品管理局的批准,用于治疗患有低风险 MDS-RS 或 MDS/MPN-RS 的成人贫血-T 在红细胞生成刺激剂 (ESA) 失败后需要 ≥2 RBC 单位/8 周。此处报告了 MEDALIST 研究中对 MDS/MPN-RS-T 患者的罗特西普疗效和安全性的事后分析。
MEDALIST 研究招募了 229 名患有低风险 MDS-RS 的成年人,他们需要 ≥2 RBC 单位/8 周,并且对 ESA 不耐受或不耐受。患者按 2:1 随机分配至罗特西普或安慰剂组,每 3 周皮下给药,持续 24 周。罗特西普起始剂量为 1.0 mg/kg,根据输血要求和不良事件滴定至最大 1.75 mg/kg。使用细胞形态学、细胞遗传学和分子遗传学结果以及血细胞计数对意向治疗人群中的 MDS/MPN-RS-T 患者进行诊断。
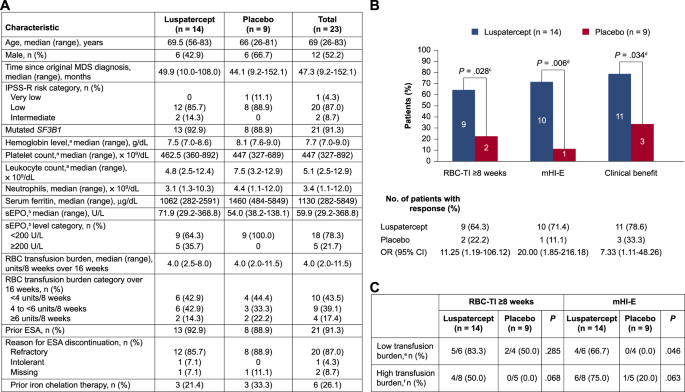
在 MEDALIST 研究的 229 名患者中,23 名 (10.0%) 患有 MDS/MPN-RS-T;14 人被随机分配到罗特西普组,9 人被随机分配到安慰剂组。两组之间不同的基线特征包括较低的中位白细胞计数(4.8 vs 7.5 × 10 9 /dL)和血清铁蛋白(1062 vs 1460 µg/dL),以及较高的血清促红细胞生成素(sEPO)(71.9 vs 54.0 U/L) (图 1A)。罗特西普和安慰剂组的中位(范围)随访时间分别为 27.4(3.5-35.6)和 13.8(3.3-32.2)个月。
图 1:MEDALIST 试验中 MDS/MPN-RS-T 患者的基线特征和治疗反应。
MEDALIST 研究的主要终点是第 1-24 周期间 RBC 输血独立性 (RBC-TI) ≥8 周。次要终点包括:改良的血液学反应——红细胞(mHI-E;平均血红蛋白增加 ≥1.5 g/dL [基线时接受 <4 RBC 单位/8 周的患者]或减少 ≥4 单位 RBC 输血[接受 ≥4 RBC 的患者单位/基线 8 周],连续 56 天以上);在第 1-24 周内连续 56 天从基线增加≥1.0 g/dL 血红蛋白;进展为急性髓性白血病(AML) 的速度;和治疗中出现的不良事件 (TEAE) 的发生率。还进行了临床益处的事后分析(定义为 RBC-TI ≥8 周和/或第 1-24 周期间的 mHI-E)。所有P值都是描述性的,未针对多重性进行调整。
截至 2019 年 7 月,随机分配到罗特西普的MDS/MPN-RS-T 患者在第 1-24 周期间达到 RBC-TI ≥8 周的比例显着增加(64.3 对 22.2%;P = 0.028);mHI-E(71.4 对 11.1%;P = 0.006);和临床获益(78.6 对 33.3%;P = 0.034),与安慰剂相比(图 1B)。罗特西普组从临床获益开始到治疗结束的中位时间为 94.6周,安慰剂组为 23.9(范围 23.7-57.9)周。
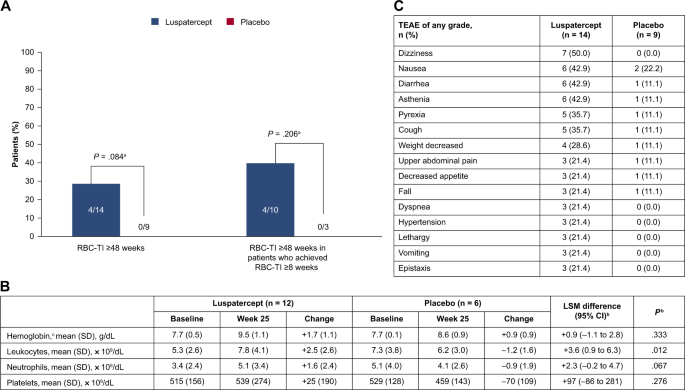
随机分配到罗特西普组与安慰剂组的低输血负担患者(<4 个单位/8 周)的数值更高,RBC-TI ≥8 周(5/6 [83.3%] vs 2/4 [50.0%];P = 0.285)在第 1-24 周内,实现 mHI-E 的比例显着增加(4/6 [66.7%] vs 0/4 [0.0%];P = 0.046)(图 1C)。随机分配到罗特西普组与安慰剂组的高输血负担患者(≥4 个单位/8 周)的数值更高,RBC-TI ≥8 周(4/8 [50.0%] vs 0/5 [0.0%];P = 0.068)和 mHI-E(6/8 [75.0%] vs 1/5 [20.0%];P = 0.063)(图 1C)。64.3% 的患者随机分配到罗特西普组,而安慰剂组为 33.3%,第 1-48 周 RBC-TI ≥8 周(P = 0.088)。随机分配至罗特西普组的患者与无安慰剂组的患者相比,28.6% 的患者在治疗期间的任何时间都达到了 RBC-TI ≥48 周;在治疗期间任何时间 RBC-TI ≥ 8 周的罗特西普组患者中,40.0% 的患者 RBC-TI ≥ 48 周,而没有安慰剂患者(图 2A)。
图 2:治疗反应、实验室参数和 TEAE
尽管数量有限,但通过与整个 MEDALIST 研究人群的数据进行比较,支持了罗特西普对 MDS/MPN-RS-T 患者的价值。MDS/MPN-RS-T 患者在第 1-24 周内 RBC-TI ≥8 周的实现率(64.3 对 22.2%)高于 MEDALIST 总体人群(37.9 对 13.2%)。同样,随机分配到罗特西普和安慰剂组的 MDS/MPN-RS-T 患者中有 71.4% 对 11.1% 的患者实现了 mHI-E,而 MEDALIST 总体人群中的这一比例为 52.9% 对 11.8%。
治疗 24 周后,随机分配至罗特西普的患者的平均血红蛋白、白细胞和中性粒细胞较基线升高,而血小板水平保持稳定(图 2B)。虽然 24 周后 MDS/MPN-RS-T 患者的血红蛋白水平升高在罗特西普和安慰剂之间没有显着差异,但绝对升高幅度名义上更高。随机分配到罗特西普与安慰剂组的患者平均白细胞计数显着增加,但平均血小板或中性粒细胞计数没有增加。在基线时,MDS/MPN-RS-T 患者的血小板计数中位数高于 MEDALIST 总体人群,正如预期的那样,sEPO 中位数较低,接受铁螯合治疗的可能性较小,输血负担中位数较低,这与他们较高的 RBC-TI 和 mHI-E 反应率一致。
罗特西普组最常见的任何级别的 TEAE 是头晕、恶心、腹泻和虚弱(图2B)。导致停药的 TEAE 发生在罗特西普组 14 名患者中的 2 名(14.3%)和安慰剂组9名患者中的3名(33.3%)。一名随机分配到罗特西普的患者经历了短暂性脑缺血发作。一名随机分配到安慰剂组的患者进展为 AML(P = 0.202),而没有随机分配到罗特西普组。
对 MDS/MPN-RS-T 患者的治疗建议包括 ESA 和贫血输血,来那度胺治疗贫血和血小板水平降低 。对 MDS/MPN-RS-T 患者使用来那度胺的建议基于 12 例患者的病例报告和167例患者的回顾性分析,而不是临床试验;ESA 的使用基于一项单一的回顾性研究,该研究包括 40 名 MDS/MPN-RS-T 患者,其中 45% 达到红系反应(血红蛋白增加≥2.0 g/dL 或 RBC-TI ≥8 周的患者)要求 ≥4 个单位/8 周),而目前研究中接受罗特西普(难治性或不适合 ESAs)治疗的患者占 71.4%。然而,鉴于红系反应的不同定义,这种比较应谨慎进行。
总之,该亚组分析提供了第一个临床试验数据,以支持罗特西普对MDS/MPN-RS-T患者的疗效。总体而言,罗特西普被发现是有效的——显着降低输血负担并改善 mHI-E 和白细胞水平——具有普遍良好耐受的安全性。
原始出处:
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#增生性#
113
#骨髓增生异常综合#
106
#血小板增多症#
92
#骨髓增生异常#
86
#骨髓增生#
100