Nat Communi:唐本忠等团队合作开发治疗阿尔茨海默病的潜在新策略
2024-01-27 iNature iNature
本研究设计了一种用于精确治疗AD的近红外II聚集诱导发射(AIE)纳米治疗剂。
毒性β淀粉样蛋白(Aβ)斑块和有害炎症是阿尔茨海默病(AD)的两个主要症状。然而,由于缺乏双靶点治疗功能、血脑屏障渗透率差、成像灵敏度低等原因,无法实现精准的AD治疗。
2024年1月24日,香港中文大学唐本忠、南方医科大学张静、河南大学汪欣及师冰洋共同通讯在Nature Communications 发表题为“A one-two punch targeting reactive oxygen species and fibril for rescuing Alzheimer’s disease”的研究论文,本研究设计了一种用于精确治疗AD的近红外II聚集诱导发射(AIE)纳米治疗剂。1350 nm 的抗猝灭发射可准确监测体内BBB的渗透以及 nanotheranostic 与斑块的特异性结合。
在活性氧(ROS)的触发下,两个封装的治疗型AIE分子被可控释放以激活自我增强治疗计划。一种特异性地抑制Aβ原纤维的形成,降解 Aβ原纤维,并通过计算分析验证的多竞争性相互作用阻止重新聚集,从而进一步缓解炎症。另一种有效清除ROS和炎症,重塑大脑氧化还原平衡并增强治疗效果,共同逆转神经毒性,并在雌性AD小鼠模型中实现有效的行为和认知改善。

随着人口老龄化,中枢神经系统(CNS)神经退行性疾病的患病率逐渐上升,构成重大的公共卫生危机。阿尔茨海默病(AD)是最常见的神经退行性疾病之一,损害大脑健康并导致严重的神经功能障碍和运动障碍,这被认为是一种无法治愈的疾病。毒性β淀粉样蛋白(Aβ)斑块和有害炎症是AD的主要标志,它们相互强化并加重破坏性过程,即Aβ沉积物激活炎症。因此,迫切需要设计一种针对AD的Aβ和炎症双靶向治疗体系。
在过去几十年中,尽管投入了大量资金,但只有几类获批用于治疗AD的药物被开发出来。然而,这些药物是单靶向的,对 Aβ 和炎症症状的特异性较低,并且有些存在高毒性风险。更糟糕的是,血脑屏障(BBB)阻止了大多数药物进入大脑,从而导致治疗效果不佳。精准高效药物的开发依赖于肉眼可见的体内研究手段。因此,迫切需要开发一种具有穿透BBB、高特异性和双靶点潜能的视觉治疗药物,通过高灵敏度的活体可视化监测BBB穿透和与Aβ斑块的结合,逆转Aβ斑块,原位抗炎,实现安全、有效、精准的AD治疗。
高灵敏度成像跟踪技术可以通过体内监测结果的反馈来指导药物的定向和精确设计。在众多成像技术中,具有非放射性、无创、安全和实时观察的荧光成像具有优点,是制造AD视觉药物的理想人选。尽管已经开发了越来越多的体外检测到的 Aβ 斑块探针,不幸的是,这些报道的探针仅作为淀粉样纤维的离体组织学染色的报告基因,无法支持体内成像和治疗应用。最重要的是,目前所有探针都缺乏用于特定双靶向治疗的活性中心。
具有聚集诱导发射(AIE)特性的治疗型NIR-II探针,即视觉药物,应该具有非侵入性、大穿透深度、抗淬火和高信噪比(S/N)以及潜在的药物活性优点。作为一种先进的概念视觉药物,它有望支持对血脑屏障穿越过程和药物与Aβ斑块结合过程的高逼真可视化,并为实现上述AD的双靶点治疗提供机会。然而,获得这种理想的探针存在巨大的挑战。迄今为止,由于缺乏适当的设计策略,仍然没有成功的范式可以解决上述挑战,以实现这种具有理想的NIR-II 发射药物。
该研究通过巧妙的分子设计和共组装策略,构建了一种脑靶向、纤维降解和ROS调节的NIR-II纳米治疗系统,成功解决了上述长期存在的AD挑战。 首先,通过想象的多重优化和金属络合策略合成了两种具有NIR-II发射的治疗诊断型AIE发光剂(AIEgens)。然后,通过智能共组装工程策略和脑靶向血管肽-2(Ang-2)修饰,将它们进一步制备成活性氧(ROS)响应的纳米治疗药物。
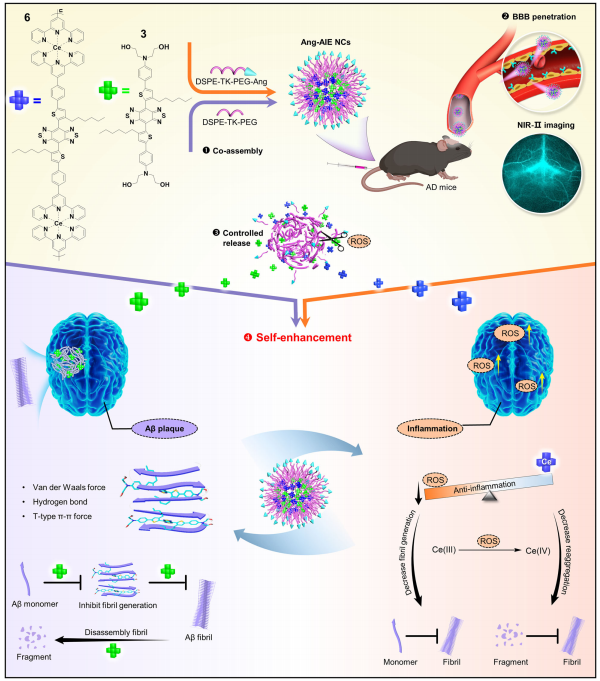
通过四步途径进行AD双靶点治疗的NIR-II脑靶向治疗系统示意图(图源自Nature Communications )
所得纳米复合材料(Ang-AIE NCs,简称Ang-NCs)产生了两种AIEgens所不具备的新优势:(i)两个疏水分子变成了具有较长体内消除半衰期(3.9 h)的亲水NCs,有利于体内长期追踪和提高治疗效果。(ii)NCs在1350 nm处具有迄今为止AD领域最长的发射波长,这产生了通过血脑屏障后有效监测体内Aβ斑块与NCs结合的跨颅信号的最高灵敏度。(iii)AD区域中与炎症相关的活性氧触发NCs可控释放两种AIEgens,产生相加和协同自我增强的治疗效果。此外,NCs强烈抑制降解的Aβ片段的有效有害再聚集过程,重塑大脑氧化还原平衡,并逆转神经毒性,从而在AD小鼠模型中获得显着的行为和认知改善。总体而言,NIR-II双靶向策略的实现,作为概念验证,很好地解决了AD中Aβ原纤维和炎症的困境,从而可能激发更先进的视觉纳米治疗方法,用于其他神经退行性疾病,以保护我们的大脑健康。
参考消息:
https://doi.org/10.1038/s41467-024-44737-x
作者:iNature
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#阿尔茨海默病# #毒性β淀粉样蛋白# #纳米治疗剂#
0