EGFR突变状态大变样导致三代TKI耐药,阿法替尼+安罗替尼稳定病情
2024-01-25 苏州绘真医学 苏州绘真医学
本文报告了一名患者于2016年9月被诊断为EGFR阳性晚期肺腺癌。吉非替尼一线靶向治疗后,基因检测显示EGFR T790M阳性,改用奥希替尼靶向治疗。
第三代EGFR-TKIs可用于治疗第一代或第二代EGFR-TKIs诱导的T790M耐药突变的晚期非小细胞肺癌患者。但第三代EGFR-TKIs也会产生耐药性,耐药机制复杂。本文报告了一名患者于2016年9月被诊断为EGFR阳性晚期肺腺癌。吉非替尼一线靶向治疗后,基因检测显示EGFR T790M阳性,改用奥希替尼靶向治疗。2021年5月,肌钙蛋白和肌酐水平升高,肿瘤超进展为重症肺癌。重复基因检测显示,EGFR突变转为非经典突变,EGFR T790M转为阴性,导致第三代EGFR-TKI耐药。于是,选择阿法替尼联合安罗替尼来稳定患者病情。本病例反映了在整个治疗过程中探索耐药机制和动态检测基因状态的意义和必要性,这可能有助于实现个体化精准治疗,使患者结局最优化。
背 景
表皮生长因子受体(EGFR)是非小细胞肺癌(NSCLC)抗癌治疗的关键分子靶点。EGFR外显子19缺失和外显子21 Leu858Arg点突变约占体细胞EGFR突变的85%,称为经典突变。也存在不常见的突变,第二代EGFR-TKI对其有效。与前两代EGFR-TKIs常见的T790M耐药突变不同,第三代EGFR-TKIs的潜在耐药机制复杂,目前相关了解较少。除了继发性EGFR C797S突变外,靶内耐药机制还包括其他罕见的EGFR三级突变,如T790M消失。脱靶机制主要包括间充质-上皮转化因子(MET)扩增和HER-2扩增导致异常旁路通路激活,下游通路激活(RAS/RAF/MEK/ERK和PI3K/AKT/mTOR)和组织学/表型转化(SCLC转化和上皮-间充质转化)。本文报告了一例重症肺癌患者在接受第一代和第三代EGFR-TKIs治疗后肿瘤超进展,阿法替尼联合安罗替尼治疗成功。该患者EGFR突变转为非经典突变,T790M转为阴性,导致第三代EGFR-TKIs耐药。
病 例
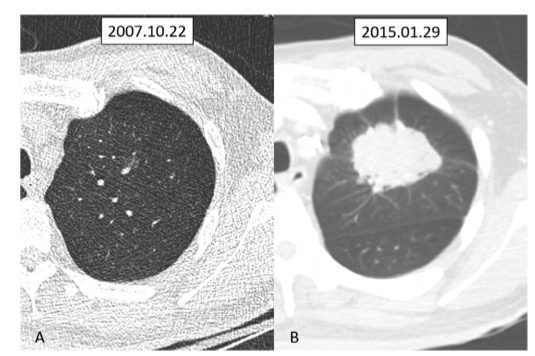
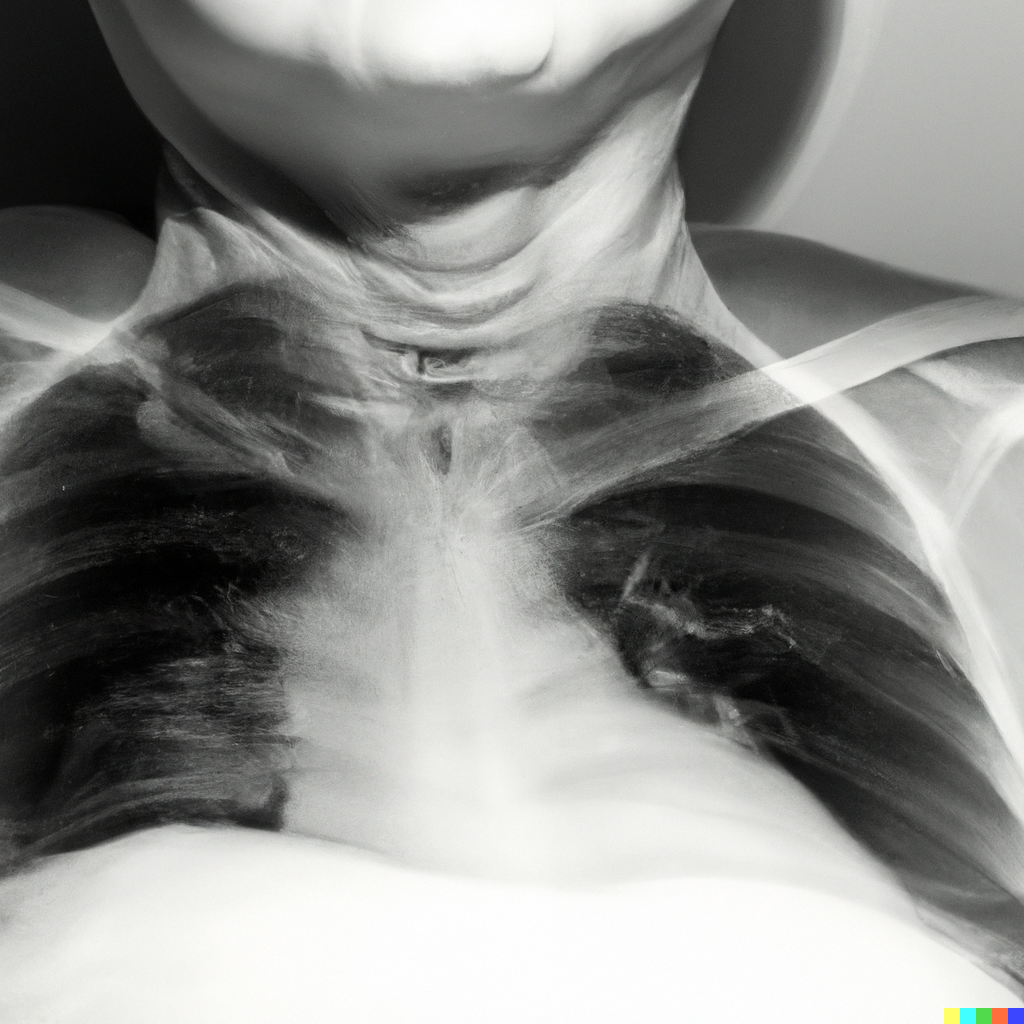
2016年9月,一名63岁男性确诊临床分期T1N0M1b(IVA期)左肺腺癌(图1)。基因检测显示EGFR 19-del delE746-A750。2016年10月至2018年2月,接受吉非替尼作为一线靶向治疗(图1b),无进展生存期(PFS)为16个月,疗效评估为PD。重复基因检测显示EGFR T790M突变阳性,于是,2018年2月至10月,改用奥希替尼作为二线靶向治疗(图1c),PFS为8个月,疗效评估再次为PD。2018 年 10 月至 12 月,接受了 4 个周期的培美曲塞联合贝伐珠单抗治疗,PFS 为 23 个月。2020年11月,出现双侧腰痛,MRI显示多发骨转移,在局部调强放疗联合唑来膦酸治疗后消退。2020 年 12 月至 2021 年 3 月,接受了 5 个周期的奥希替尼联合贝伐珠单抗治疗(图1d)。2021 年 5 月,cTnI 升至 6.2 ng/ml,无胸闷或疼痛,冠状动脉 CTA 未见异常。此外,肌酐升至 167umol/L,因此停止了所有抗肿瘤治疗。2021年6月25日,出现呼吸短促,伴有双下肢水肿,PS评分为4。胸部X光显示双肺多发病变,其中一些是炎症,另一些是恶性肿瘤(图2a)。超声显示右侧大量胸腔积液。NT-proBNP 升至 3220 pg/ml。被认为与肺腺癌超进展有关,导致心力衰竭、肾功能不全、肺部感染、恶性胸腔积液、肢体血管栓塞等一系列改变。重复基因检测显示EGFR 19-del p.L747P753delinsS,T790M转为阴性,ERK/MAPK信号通路激活(表1)。因此,给予该通路抑制剂哌柏西利,但反应较差。诊断为左上肺腺癌,T4N3M1c(多发骨转移),IVB期。进行最佳支持和对症治疗。7月23日,选择阿法替尼联合安罗替尼作为抗肿瘤治疗,病情显著缓解(图2b)。然而,不幸的是,缓解1个月后,出现脑梗塞,最终于2021年9月26日死亡。治疗史总结于图3。
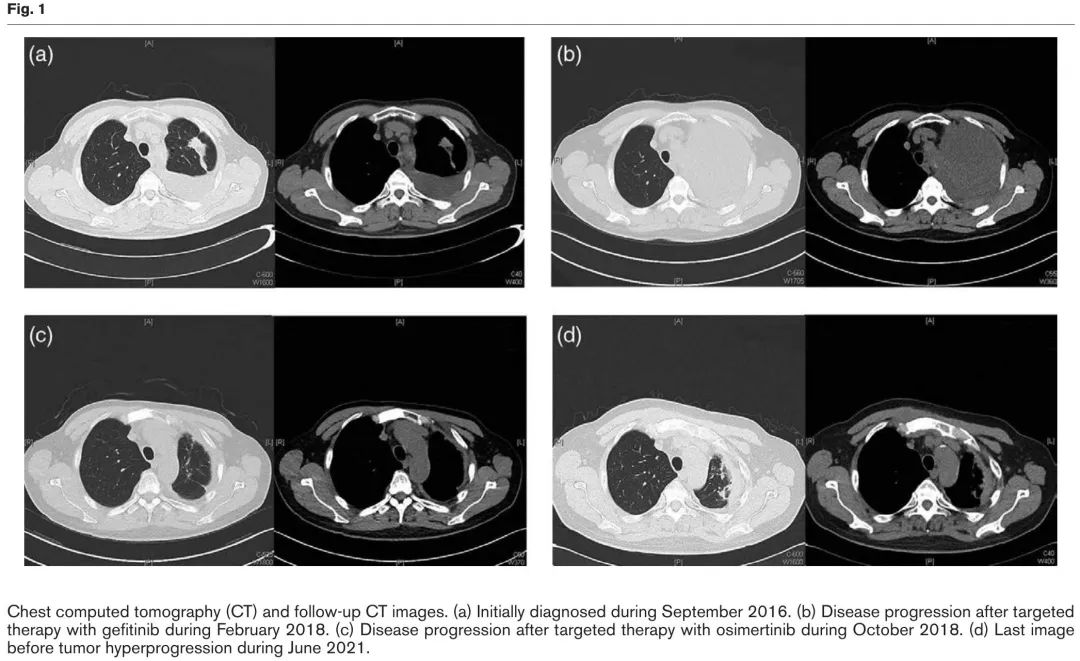
图1

图2
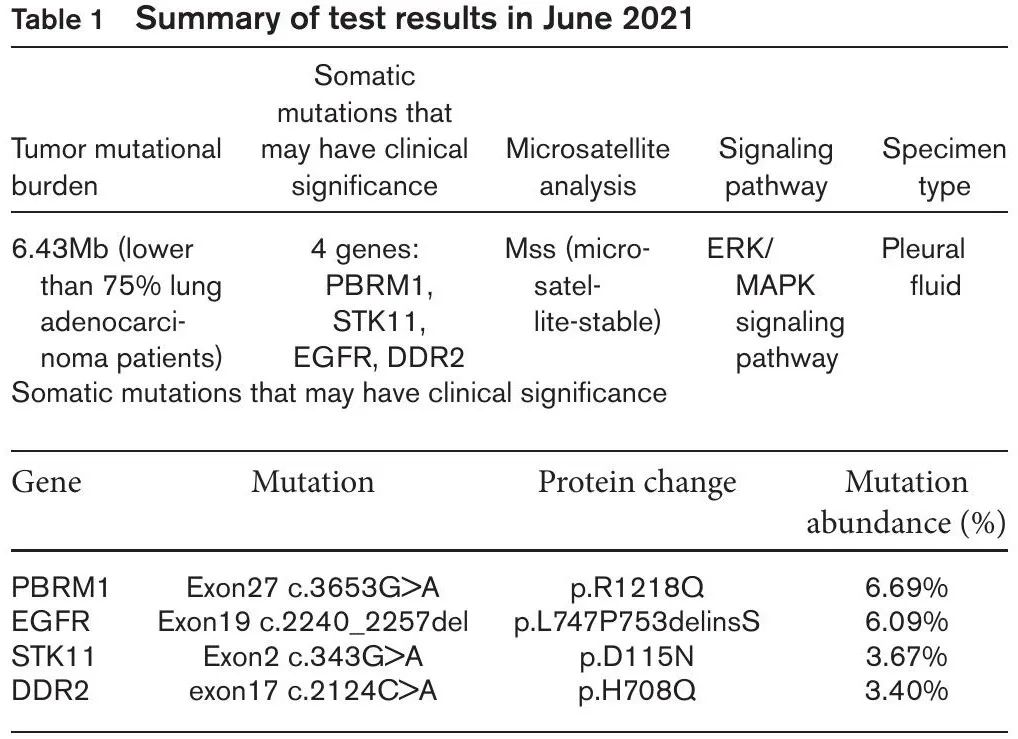
表1
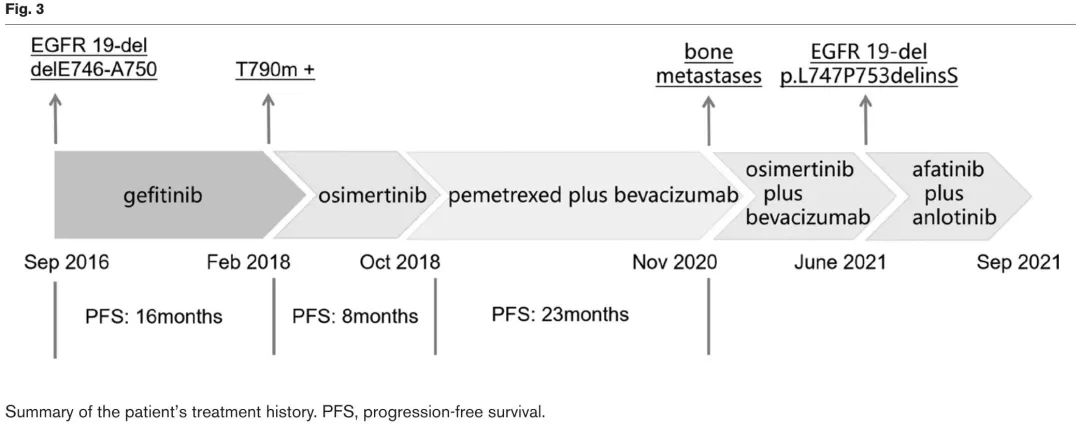
图3
讨 论
该晚期肺癌患者,EGFR 19-del,T790M阳性,接受第一代和第三代EGFR-TKIs靶向治疗,PFS为24个月,改用培美曲塞联合贝伐珠单抗,PFS为23个月。再次进展,出现骨转移,再次接受第三代EGFR-TKIs联合抗血管生成药物,但疗效较差,出现超进展。患者肌钙蛋白升高,肾功能损害,冠状动脉CTA未显示冠心病迹象,考虑肿瘤进展导致心肌损伤。2周内未接受有效抗肿瘤治疗,随后病情迅速进展为晚期重症肺癌,伴有肾功能衰竭、心力衰竭、肢体血管栓塞等一系列变化。病情危急,可能与突然停止靶向治疗后出现反跳现象有关,导致肿瘤超进展。肿瘤超进展时,基因检测显示 EGFR 外显子 19 缺失突变从 delE746-A750 经典突变转为 p.L747P753delinsS 非经典突变。EGFR 19delins突变导致酪氨酸激酶结构域空间构象变化,这是由于插入新的氨基酸序列所致,这影响其与EGFR TKI的结合。一项研究显示,奥希替尼在罕见外显子19缺失突变的二线治疗中效果较差。基因检测还显示EGFR T790M呈阴性,可能是由于使用第三代EGFRTKIs后抑制了部分T790M阳性肿瘤细胞。在第三代EGFR-TKIs靶向治疗和化疗后,T790M阴性肿瘤细胞增殖成为优势肿瘤细胞群,提示肿瘤异质性。这反映了在肿瘤发展过程中肿瘤基因不断进化,提示在癌症治疗过程中,进行多次基因检测对于了解优势肿瘤细胞群的重要性。选择阿法替尼联合安罗替尼作为治疗方案。阿法替尼对非经典突变类型有效,与低毒性抗血管生成药物安罗替尼联合使用,可协同作用并降低耐药性,该治疗在约1周内挽救了危重症患者。然而,奥希替尼耐药机制是多种多样的,一些研究表明,在大多数情况下,奥希替尼耐药后T790M消失意味着其他脱靶耐药机制(如MET扩增和SCLC转化)的产生。因此,再使用前两代EGFR TKI并不总是有效的,只有一小部分幸运的患者能够治疗成功。此外,基因检测显示ERK/MAPK信号通路激活,这可能是EGFR-TKIs耐药的原因之一。患者接受了 ERK/MAPK 通路抑制剂哌柏西利治疗,但无效,可能是由于耐药性导致多个下游通路激活。其仅限于抑制ERK/MAPK通路。最终,患者在缓解后死于脑梗死并发症,值得回顾。在晚期癌症患者中,阿法替尼联合安罗替尼可能引起血管内皮损伤,增加栓塞风险,需要谨慎和积极临床预防。
鉴于EGFR突变NSCLC患者奥希替尼耐药的复杂性,要克服耐药问题还有很长的路要走。除了开发第四代TKIs外,还需要探索更多解决、预防或延缓奥希替尼耐药发生的方法,如新用旧药或多种疗法联合使用等。此外,动态基因监测在患者治疗过程中具有重要意义,可以避免不必要的抗肿瘤治疗。
参考文献:
Li Q, Xu N, Lin M, Chen Y, Li H. Successful treatment of severe lung cancer caused by third-generation EGFR-TKI resistance due to EGFR genotype conversion with afatinib plus anlotinib. Anticancer Drugs. 2024 Jan 1;35(1):93-96. doi: 10.1097/CAD.0000000000001530. Epub 2023 Jul 7. PMID: 37449979.

作者:苏州绘真医学
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







学习了
24
#肺腺癌# #阿法替尼# #安罗替尼#
25