Nat Commun:倍沙罗素如何抑制Aβ42聚积?
2021-01-30 haibei MedSci原创
研究人员利用红外纳米光谱的单分子形态和化学敏感性,首次直接测量了单个Aβ42低聚物和纤维状物种与聚集抑制剂倍沙罗素之间的结构和相互作用。
老年痴呆症的特点是记忆丧失和认知障碍。AD是导致痴呆症的主要原因,目前全球有超过5千万人受到影响,预计到2050年,这一数字将超过1.5亿。淀粉样蛋白-β(Aβ)肽的42个残基异构体可以自组装成不溶聚合体,其被认为是引起AD的分子途径的核心。因此,在分子水平上了解Aβ42的聚集过程是非常重要的,以便开发有效的治疗策略,旨在抑制其自组装。

在过去的20年里,人们一直在努力开发能够干扰蛋白质错误折叠聚积的化合物。然而,到目前为止,还没有任何药物可用于这些疾病的临床使用。这种失败的主要原因之一是我们对小分子与蛋白质聚集物相互作用并干扰其聚集的过程不完全了解。
最近,研究人员利用红外纳米光谱的单分子形态和化学敏感性,首次直接测量了单个Aβ42低聚物和纤维状物种与聚集抑制剂倍沙罗素之间的结构和相互作用,倍沙罗素能够在体外防止Aβ42聚集,并在阿尔茨海默病的细胞和动物模型中逆转其神经毒性。
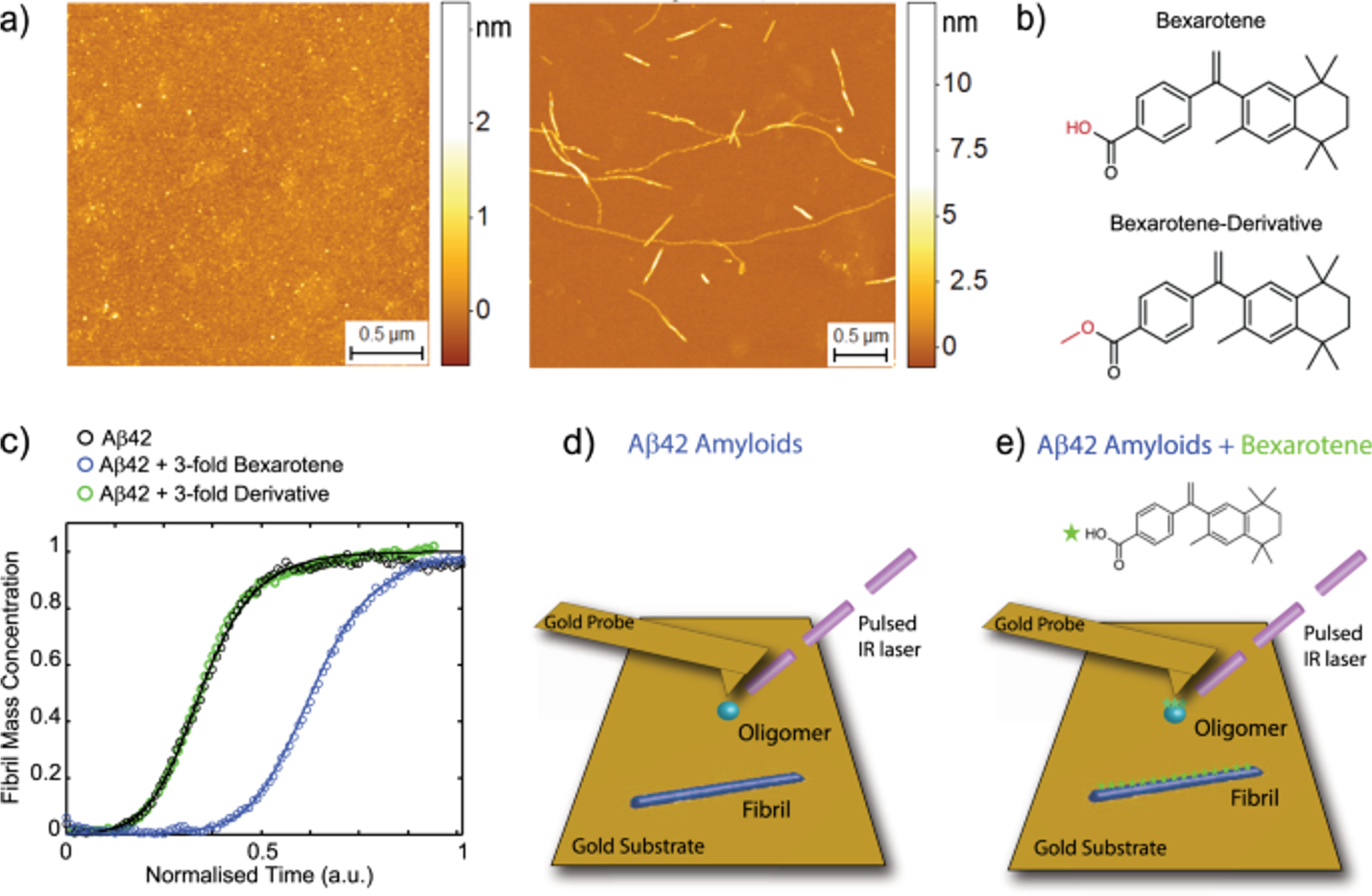
其研究结果表明,该化合物的羧基通过单个氢键与Aβ42聚集物相互作用。这些结果确立了红外纳米光谱作为一种基于结构的药物发现的强大工具,用于蛋白质错误折叠引起的疾病。
原始出处:
Francesco Simone Ruggeri et al. Infrared nanospectroscopy reveals the molecular interaction fingerprint of an aggregation inhibitor with single Aβ42 oligomers. Nature Communications (2021).
作者:haibei
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#Nat#
31
#Aβ42#
50
#COMMUN#
25
#Aβ#
32
新知识
0