CTM:SIRT5缺失通过代谢转换促进脂肪间充质干细胞的增殖和治疗潜能
2020-10-09 XD – 程欣 CTMWorld
间充质干细胞(MSCs)是典型的成体干细胞。MSCs可以通过组织特异性分化,旁分泌作用和免疫调节等机制促进组织修复。不论是在基础研究还是临床科研中,因为MSCs很容易分离,没有免疫原性且显示出很强的治
间充质干细胞(MSCs)是典型的成体干细胞。MSCs可以通过组织特异性分化,旁分泌作用和免疫调节等机制促进组织修复。不论是在基础研究还是临床科研中,因为MSCs很容易分离,没有免疫原性且显示出很强的治疗潜能,所以MSCs被广泛地用于缺血性疾病的研究。原代MSCs较为稀有,所以在临床应用前的培养扩增就显得至关重要。但是体外的人工环境很可能使MSCs的能量代谢发生改变,进而使MSCs的细胞稳态受到破坏,使MSCs细胞的自我更新能力耗竭,最终使MSCs的治疗功效受到破坏。因此维护MSCs细胞的治疗潜能,保护MSCs的增殖能力在MSCs的临床应用中显得至关重要。
2020年9月11日,Clinical and Translational Medicine杂志在线发表了上海中山医院葛均波院士团队的最新成果 “SIRT5 deficiency enhances the proliferative and therapeutic capacities of adipose-derived mesenchymal stem cells via metabolic switching”[6] 。


MSCs对多种缺血性疾病有治疗潜能。但是临床应用前的体外扩增可以导致MSCs的代谢发生从糖酵解到氧化磷酸化的转变,大大损害了MSCs的增殖和治疗潜能。本项研究的目的是探讨在体外扩增过程中去乙酰化酶5(SIRT5)对脂肪来源的MSCs(ADMSCs)增殖和治疗功能的调节作用。
首先从野生型(WT)和Sirt5 敲除(Sirt5-/-)小鼠中分离出 ADMSCs。通过细胞计数监测ADMSCs的增殖能力。用二氢乙锭和senescence相关的β-半乳糖苷酶染色检测细胞内ROS和senescence情况。用质谱分析蛋白琥珀酰化情况。通过测量氧消耗率和细胞外酸化率来检测线粒体呼吸和糖酵解的情况。用定量PCR和western法检测代谢相关基因的表达情况。用后肢缺血小鼠模型评估WT和Sirt5-/- ADMSCs的治疗潜能。

结果表明在体外扩增过程中ADMSCs的SIRT5蛋白水平被上调。Sirt5-/- ADMSCs表现出更高的增殖率,senescence延缓和ROS累积量降低。此外Sirt5-/- ADMSCs的蛋白琥珀酰化水平升高,导致三羧酸循环相关酶活性降低和线粒体呼吸减弱。Sirt5-/- ADMSCs中葡萄糖的摄取,糖酵解和磷酸戊糖途径都升高/加强。如果在Sirt5-/- ADMSCs中通过用甘氨酸或重新表达Sirt5来抑制琥珀酰化或逆转代谢的改变,则可以消除Sirt5-/- ADMSCs的高增殖力。与WT ADMSCs相比,在后肢缺血小鼠模型中Sirt5-/- ADMSCs移植可以更好地促进血流恢复和血管生成。
结论是在ADMSC培养和扩增过程中,SIRT5缺失可以逆转代谢的改变,促进ADMSCs增殖能力,增强ADMSCs的治疗效能。说明SIRT5可以作为促进MSCs功能和临床应用的潜在靶点。
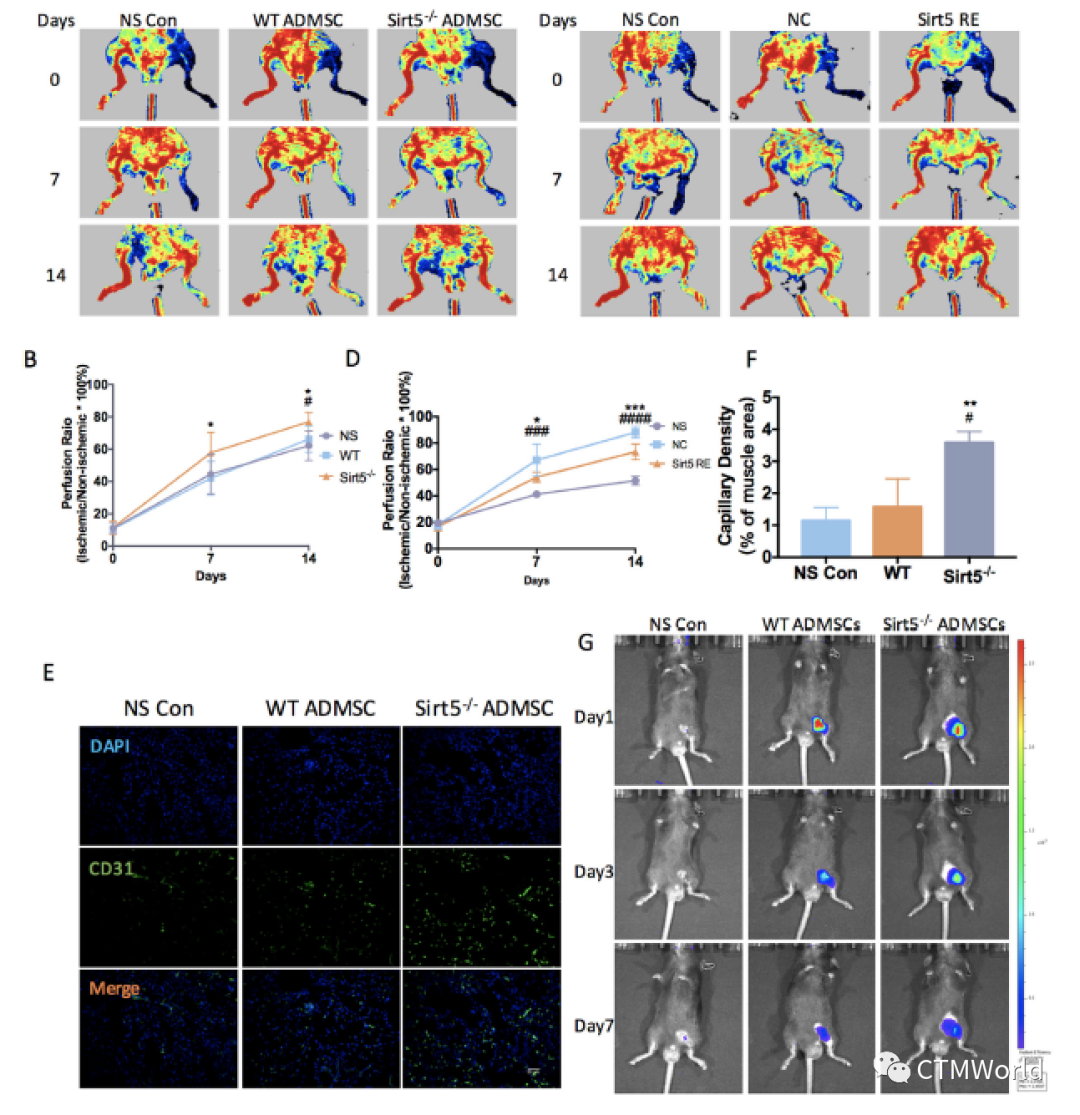
总之,作者及其团队的研究表明在体外不断的传代过程中ADMSCs中SIRT5会聚积,并可以导致ADMSCs干性的消失。ADMSCs中SIRT5缺失可以逆转体外培养过程中ADMSCs代谢的改变,通过升高无氧酵解和减缓线粒体呼吸,使ADMSCs处于更接近体内的代谢模式。此外,Sirt5-/- ADMSCs的代谢改变可以促进其增殖能力和治疗功能。本项研究表明SIRT5对细胞培养过程中的ADMSCs有代谢调节等功能。此外,作者提出SIRT5是促进ADMSCs临床功效的潜在靶点。本项研究不仅促进了MSC治疗研究的深入,而且为有类似代谢机制、其它种类干细胞的临床治疗策略提供有力的支持。
REFERENCES
1. Uccelli A, Moretta L, Pistoia V. Mesenchymal stem cells in health and disease. Nat Rev Immunol. 2008;8(9):726-736.
2. Luo R, Lu Y, Liu J, et al. Enhancement of the efficacy of mesenchymal stem cells in the treatment of ischemic diseases. Biomed Pharmacother. 2019;109:2022-2034.
3. Ward MR, Abadeh A, Connelly KA. Concise review: rational use of mesenchymal stem cells in the treatment of ischemic heart disease. Stem Cells Transl Med. 2018;7(7):543-550.
4. Galipeau J, Sensebe L. Mesenchymal stromal cells: clinical challenges and therapeutic opportunities. Cell Stem Cell.
2018;22(6):824-833.
5. Yuan X, Logan TM, Ma T. Metabolism in human mesenchymal stromal cells: a missing link between hMSC biomanufacturing and therapy? Front Immunol. 2019;10:977.
6. Ou T, Yang W, Li W, et al. SIRT5 deficiency enhances the proliferative and therapeutic capacities of adipose-derived
mesenchymal stem cells via metabolic switching. Clin Transl Med . 2020;10:e172.
作者:XD – 程欣
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#脂肪间充质干细胞#
48
#间充质干细#
47
干细胞是热点,但是进入临床仍然需要时间和临床疗效验证哦
60