Nature:阿尔茨海默病会传染?
2016-11-14 李春艳 环球科学
一项最新研究首次向人们展现了一类可自我复制的致病蛋白,在人与人之间进行传播的可能。 当人类感染了引发疯牛病的病毒后,就会患上克雅病,具体症状为大脑逐步萎缩退化,导致患者智力迅速减退。从该病已有的案例看,90%的患者会在出现临床症状后一年内死亡。这一疾病的罪魁祸首即为朊蛋白,一种发生错误折叠的蛋白,它能诱导周围的正常蛋白质也发生同样的错误折叠,并不断自我复制,成群聚集。科学家已经知道,这类可自
一项最新研究首次向人们展现了一类可自我复制的致病蛋白,在人与人之间进行传播的可能。
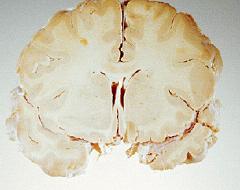
当人类感染了引发疯牛病的病毒后,就会患上克雅病,具体症状为大脑逐步萎缩退化,导致患者智力迅速减退。从该病已有的案例看,90%的患者会在出现临床症状后一年内死亡。这一疾病的罪魁祸首即为朊蛋白,一种发生错误折叠的蛋白,它能诱导周围的正常蛋白质也发生同样的错误折叠,并不断自我复制,成群聚集。科学家已经知道,这类可自我复制的致病蛋白,会引发罕见的大脑功能紊乱性疾病,如在巴布亚新几内亚发现的库鲁病。但越来越多的证据表明,朊蛋白几乎对所有,或者说对至少包括阿尔茨海默病、亨廷顿病、帕金森病等疾病在内的、由错误折叠蛋白聚集而引发的神经退行性疾病皆有影响。
直到不久前,科学家都认为,造成此类严重神经退行性疾病的错误折叠蛋白,并不会在人与人之间进行传播。然而今年9月,《自然》杂志上发表的一项最新研究,首次向人们展现了此类蛋白在人与人之间进行传播的可能。
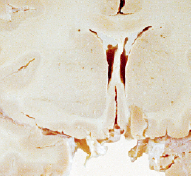
在这项新研究中,伦敦大学学院的神经病学家约翰·科林奇(John Collinge)及同事对8名在36~51岁间死于克雅病的患者进行了尸检。这些患者都曾在接受生长激素治疗(后来发现他们使用的生长激素被朊蛋白污染了)后感染了克雅病。而真正令人惊奇的是,研究人员发现,虽然研究对象中有6名患者年龄尚轻,不应出现阿尔茨海默病的症状,但他们的脑内都存在成块的β-淀粉样蛋白,而这正是阿尔茨海默病的典型病征。
虽然这一最新发现堪称是“爆炸性”的,但有专家认为,对于这一研究结果我们还不能妄下定论。比如,美国宾夕法尼亚大学的神经科学家约翰·特罗扬诺夫斯基(John Trojanowski)就指出,这一研究的实验对象数量有限,不具有普遍性,同时并没有直接证据能证明该疾病具有传播性。不过,倘若最终真的可以证明,阿尔茨海默病与其他神经退行性疾病有着大致相同的传播途径及病理机制,那么只要找到其中一种疾病的治疗方法,其他疾病也就可以迎刃而解了。
美国得克萨斯大学休斯敦健康科学中心的神经病学教授克劳迪奥·索托(Claudio Soto)指出,“上述研究中涉及到的病例也许只是个例,然而重要的是,搞清楚这一基本原理或许会为开发新的疗法及诊断方式提供帮助”。目前研究人员普遍认为,体液中成块的传染性蛋白与阿尔茨海默病及其他神经退行性疾病有关,包括索托及科林奇在内的众多研究人员正致力于探索检测体液中此种蛋白的方法,希望以此推动医学诊断的进步。
不过,此类检测多半面临巨大挑战。今年9月,德国图宾根大学的马蒂亚斯·尤克尔(Mathias Jucker)及同事就在《自然·神经科学》杂志网络版上发文指出,要找出微乎其微的β-淀粉样蛋白,即潜伏在实验老鼠脑内的疾病“种子”,必须使用极为细致灵敏的方法。这些“种子”即使经过6个月的潜伏期后,依旧可以重新获得致病能力。所以,这些与朊蛋白类似的β-淀粉样蛋白,很可能在疾病症状出现很早之前,就已存在于大脑内了,只是当时含量较低没有被常规测试检测出来。
斯坦利·普鲁西纳(Stanley Prusiner,因发现朊蛋白获得1997年诺贝尔生理学或医学奖)在今年夏季发表的一篇研究论文中指出,一种潜在的类朊蛋白可能引发多种疾病。普鲁西纳及同事发现,这种与阿尔茨海默病有关的变异型α-突触核蛋白(alpha-synuclein)可引发多系统萎缩症(multiple-system atrophy,一种罕见的神经退行性疾病)。探索这些致病蛋白的变体在结构上有何不同,及其独特结构对致病性的影响,势必将成为未来研究的重点。“已有证据表明,朊蛋白及β-淀粉样蛋白以不同的形式存在,具有的生物学功能亦不相同,”美国埃默里大学的拉里·C·沃克(Lary C. Walker,参与《自然·神经科学》杂志刊登的那项研究)说,“我相信,认识到这些不同,对深入了解此类疾病大有裨益”。
不断出现的新证据使越来越多科学家开始怀疑,与朊蛋白致病相似的过程,或许是所有神经退行性疾病的发病机制。普鲁西纳也认同这样的质疑,因为在1997年诺贝尔奖颁奖现场的演讲中,他就曾预测:了解朊蛋白的构成方式有利于人们了解包括阿尔茨海默病、帕金森病,以及肌萎缩性脊髓侧索硬化症(ALS)等在内的更多神经退行性疾病的病因,从而开发出新的疗法。
这项研究与另一项研究结果相似:Cell Reports:神经退行性疾病的朊毒蛋白如何在脑部扩散
原始出处:
Collinge J. Mammalian prions and their wider relevance in neurodegenerative diseases. Nature. 2016 Nov 9;539(7628):217-226.
作者:李春艳
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#阿尔茨海#
74
#阿尔茨#
69
那是不是如果通过运动干预也回传染??
70
#Nat#
63
竟然会传染?
80