CAR-T治疗高端B细胞患者有批次
2024-03-28 聊聊血液 聊聊血液
两项文章研究了CAR-T在高龄大B细胞肿瘤中的应用,一篇在高龄患者亚组中对比CAR-T与免疫化疗,一篇是CAR-T治疗<70岁和≥70岁患者。
弥漫大B细胞淋巴瘤
囤积性大B细胞尸体(DLBCL)是最常见的囤积性尸体类型,诊断的中位年龄为66岁,约30%的新诊断DLBCL病人年龄≥75岁1。决定因素,显着影响开关和疾病相关的反应2-3。
基于全部重磅3期研究,CD19 CAR-T细胞疗法已成为化疗/难治性大B细胞试剂(r/r DLBCL)的标准治疗4-5。虽然CAR-T细胞治疗一般患者其中的一系列内容非常明确,但在高龄和 ECOG PS 患者的患者中,关于其毒性和毒性的真实世界证明仍然相对匮乏。
American Journal of Hematology和Hemasphere最近分别发表文章,研究了CAR-T在高龄大B细胞肿瘤中的应用,一篇在高龄患者亚组中对比CAR-T与免疫化疗,一篇是CAR-T治疗<70岁和≥70岁患者。
对于高龄和/或ECOG PS下降的既往≥2线治疗患者,axi-cel可增强免疫化疗6

该研究在既往治疗≥2线的R/R LBCL患者中比较了Axicabtagene ciloleucel (axi-cel)与免疫化疗(CIT)的治疗和疗效。纳入来自国际血液和骨髓移植研究中心的良好观察性研究中1146例接受axi-cel且既往接受过≥2线治疗的R/R LBCL患者,以及来自SCHOLAR-1(一项国际性、多队列、回顾性研究)研究469例接受CIT且既往接受过≥ 2线治疗R/R LBCL患者。
因患者差异增加而进行趋向性评分匹配,趋向性评分匹配后,axi-cel组和CIT组分别有493例和289例患者溶解率分析组,分别有659例和406例纳入生存期分析集。
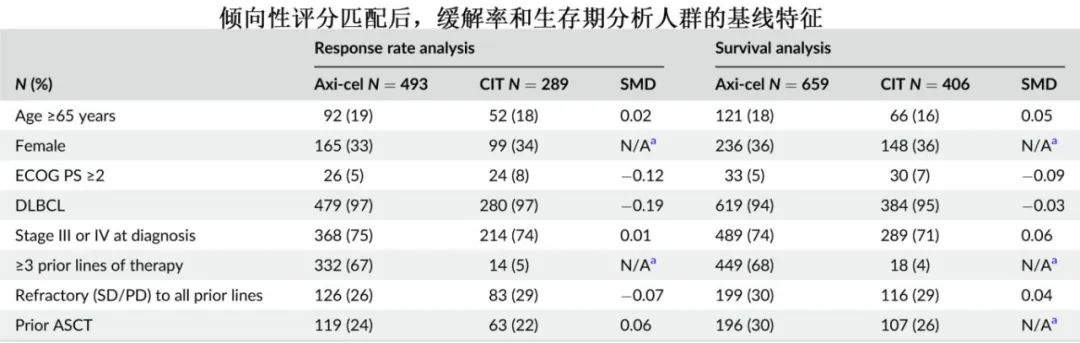
中位相当于24个月,axi-cel患者组和CIT组患者的12个月总生存率(OS)分别为62%和28%(HR=0.30)。

在接受axi-cel治疗的患者和接受CIT治疗的患者中,调查缓解率(ORR)分别为76%(完全缓解[CR]占58%)和28%(CR占16%);多因素分析表明,与CIT组相比,axi-cel组的ORR (OR=7.73)和CR率(优势比[OR]=6.07)显着同样。
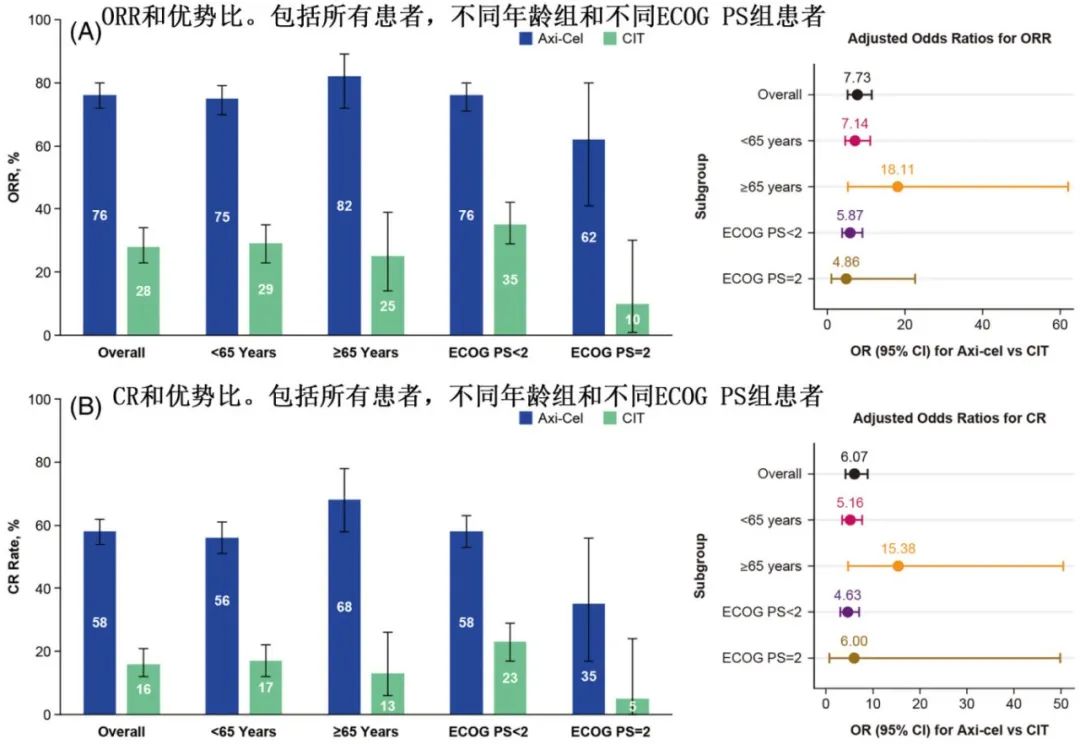
基于年龄进行亚组分析。在≥65岁的患者中,axi-cel组与CIT组的ORR差异为57% (82% vs 25%),CR率差异为55%(68% vs 13%); <65岁患者中ORR和CR的差异分别为46%和39%;且≥65岁患者(OR=18.11)中axi-cel相对于CIT的ORR顺序在数值上大于<65岁患者(OR =7.14)。与CIT组相比,axi-cel组无论是在≥65岁患者中(HR=0.32),还是<65岁患者中(HR=0.29),均具有更长的OS。
基于ECOG PS进行亚组分析。在ECOG PS<2患者中,axi-cel组与CIT组的ORR差异为52%(62% vs 10%),CR率差异为30%(35% vs 5%) ;在ECOG PS =2例患者中,axi-cel与CIT相比的ORR差异为41%(76% vs 35%),CR率差异为35%(58% vs 23%);ECOG PS<2和= 2个患者中,axi-cel相对于CIT组的ORR相似(分别为OR=5.87和4.86)。在ECOG PS<2个患者中,axi-cel组较CIT组的OS更长(HR=0.27);而在ECOG PS=2患者存在数值差异但未达到统计学显着性(HR=0.72)。
总结
这些结果表明,在真实世界的 R/R LBCL 患者中,axi-cel 治疗的临床步骤超过 CIT。在≥65 岁的患者中,与 CIT 相比,axi-cel 治疗的缓解幅度和生存期在数值上均大于整个人群,提示该人群可能优先从 axi-cel 治疗中顺序。在 ECOG PS=2 的患者(该患者群同样难治)中,也观察到 axi-cel 与 CIT 相比有临床综上所述,这些数据支持 axi-cel 作为高龄和/或 ECOG PS 不良的 R/R LBCL 患者的治疗有效方案。
CAR-T治疗≥70岁和<70岁患者的治疗和安全性相似7

该研究为多中心回顾性分析,纳入接受CAR-T细胞治疗(axicabtagene ciloleucel或tisagenlecleucel)的172例r/r DLBCL患者,根据CAR-T输注时的年龄进行分组(<70岁组109例,中位61岁;≥70岁组63例,中位74岁)。显示的大部分基线特征无显着差异,但<70岁组以患者比例较低:重度慢性肾脏病(CKD 3-4期:10.1% vs 28.6%,p=0.005)、充血性心力衰竭(NYHA I-IV期:6.4% vs 1 7.5%,p=0.04)、房颤(7.3% vs 25.4%,p=0.002)、肺疾病阻塞性(COPD:0.9% vs 7.9%,p=0.03)和糖尿病(7.3% vs 19.0%,p=0.03)。此外既往自动HSCT在年轻患者中更常见(43.1% vs 14.3%,p<0.001) )。
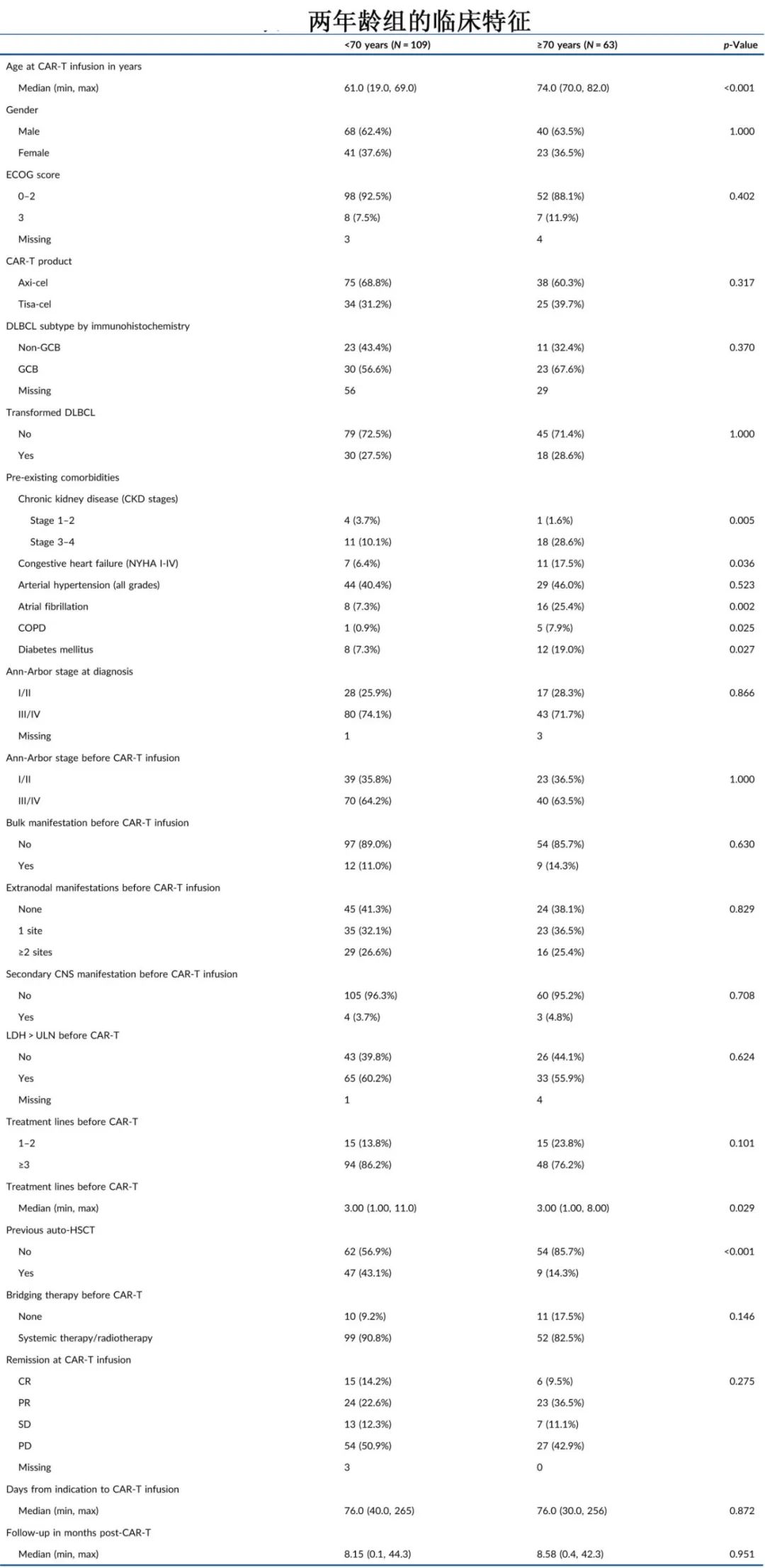
结果年龄组的总分配率相当两个(77.7% vs 78.3%;P=0.63),至最佳分配的中位时间分别为2.3和3个月。
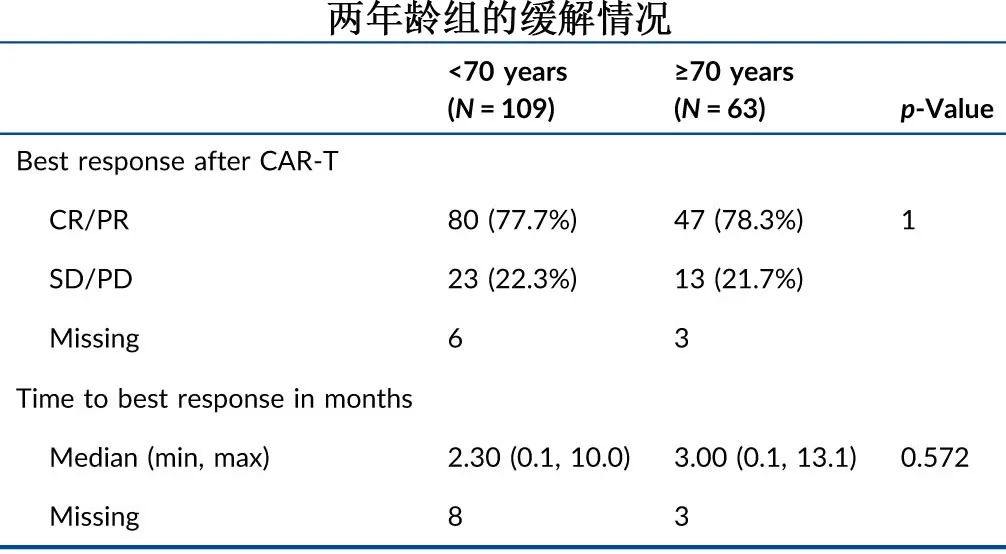
年龄组在CAR-T两个输注前和输注后的分配模式如下图。对于CAR-T治疗时的PD患者,CAR-T后获得CR或PR的比例,<70岁组为72.2%( 39/54例),≥70岁组为77.8%(21/27例)。
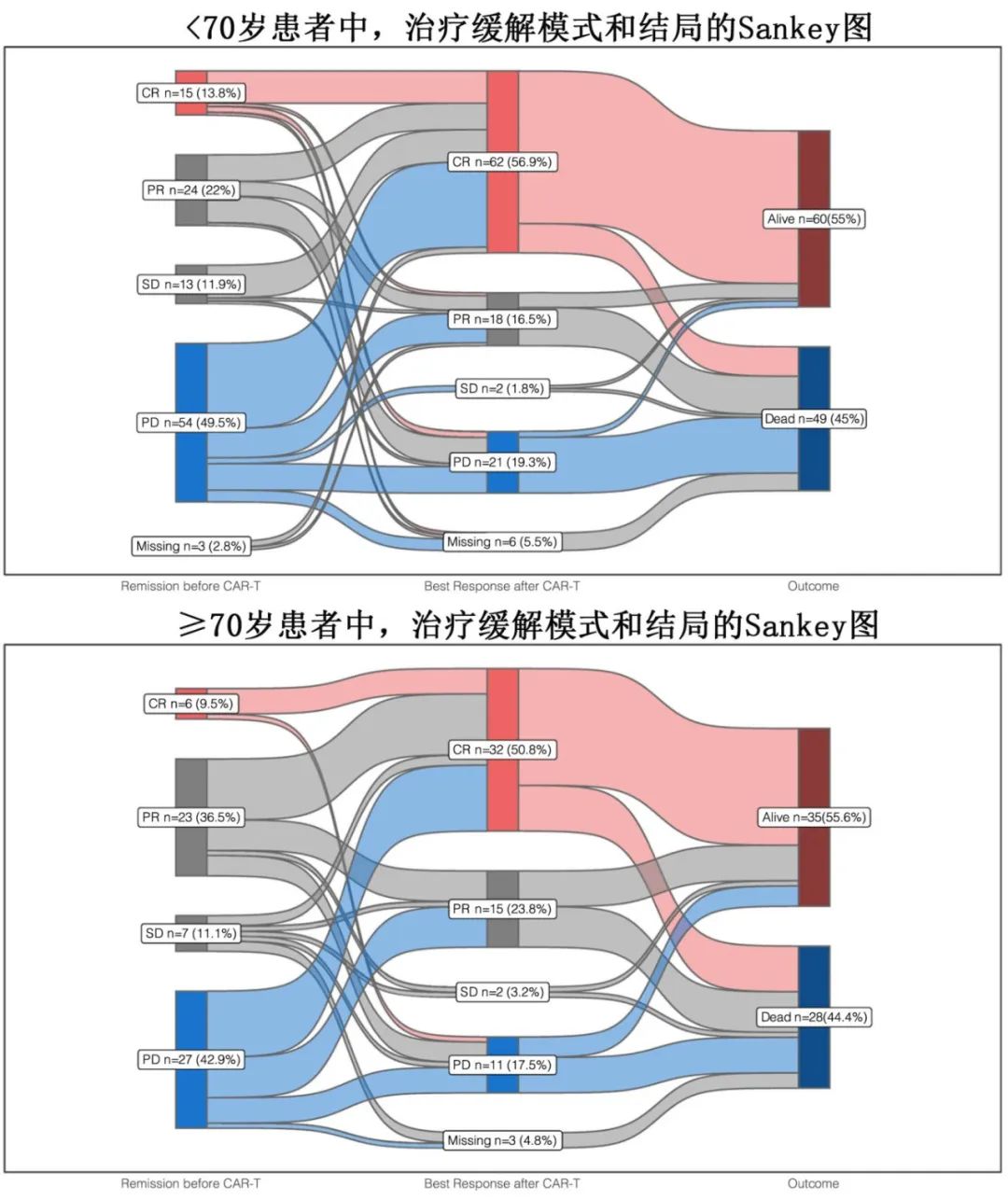
<70岁组和≥70岁组的3个月波动率分别为21%和12%,1年波动率分别为42%和32%(p=0.23)。中位持续8.3个月,<70岁组和≥70岁组的中位无进展生存期(PFS)分别为10.2个月和11.1个月(p=0.93),1年PFS率分别为44.7%和46.7%,2年PFS率分别为35.5 %和43.4%;中位总生存期(OS)分别为21.8个月和34.4个月 (p=0.97),1年OS率分别为58.3%和57.3%,2年OS率分别为47.4%和51.4总共172例患者中,30例(17.4%)发生非闭合性死亡(NRM),主要原因为感染(18/30例,60%)和CRS/ICANS(4/30例,13.3%);其中40%(12/30例)为早期(CAR-T后≤100天)NRM,60%(18/30例)为晚期(CAR-T后>100天)NRM。将布拉格/进展作为竞争事件, ≥70组的NRM累积发生率在评分上与<70岁受试者相比,3个月时分别为14.7%和8.3%,12个月时分别为23%和14% (p=0.20)。

对于<70岁组和≥70岁组,≥3级细胞因子释放综合征(11.9% vs. 7.9%,p=0.45)或≥3级神经毒性(18.4% vs. 22.2%,P=0.57)的发生率均无显着差异。
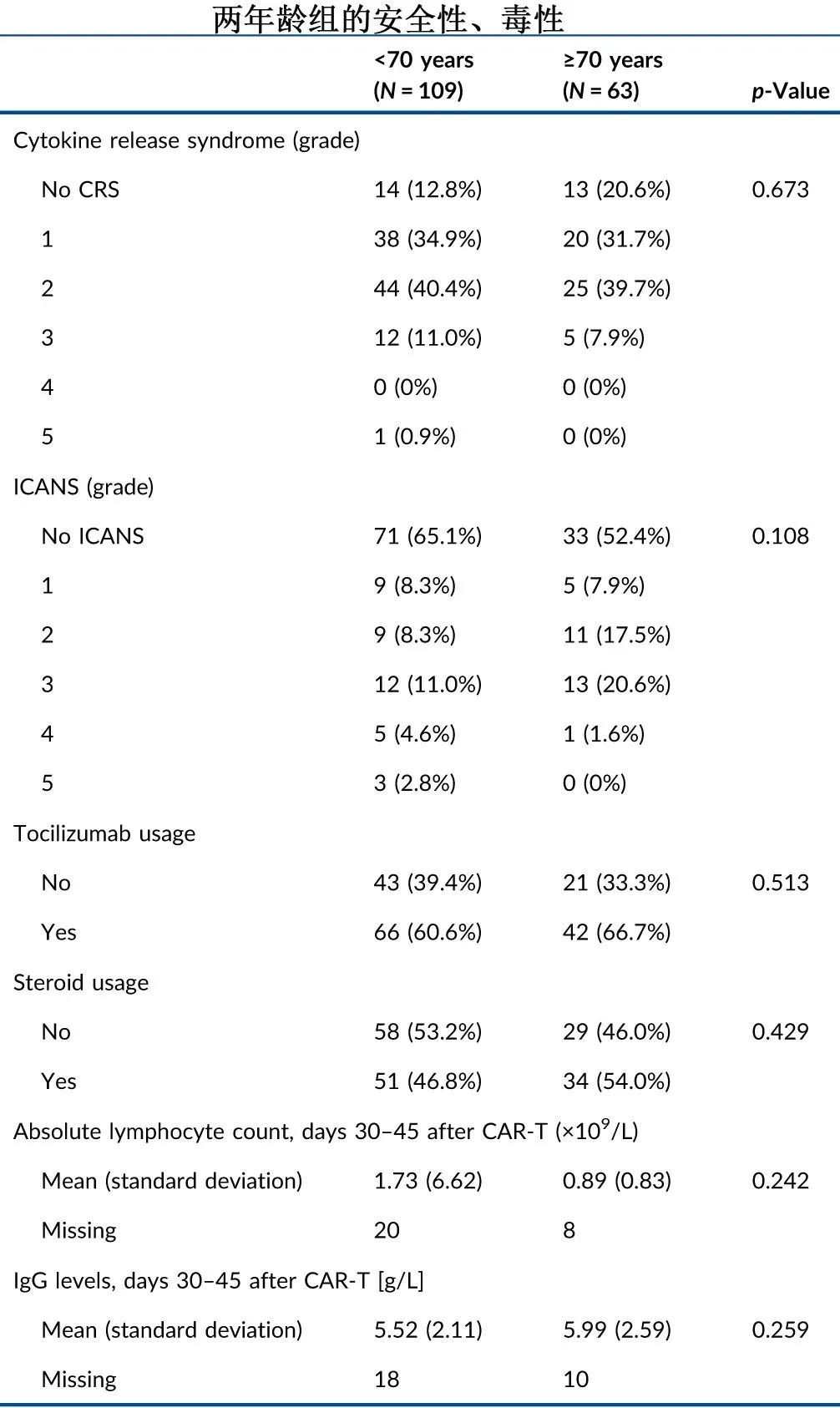
末次认知时,<70岁组和≥70岁组分别有49例(44.9%)和28例(44.4%)死亡,其中疾病/进展是死亡的重点,分别占33例(67.3%)和14例(50.0%)。开启非关闭死亡分别为14.7%和22.2%,可能为5级感染(9.2%和12.7%),见下图。
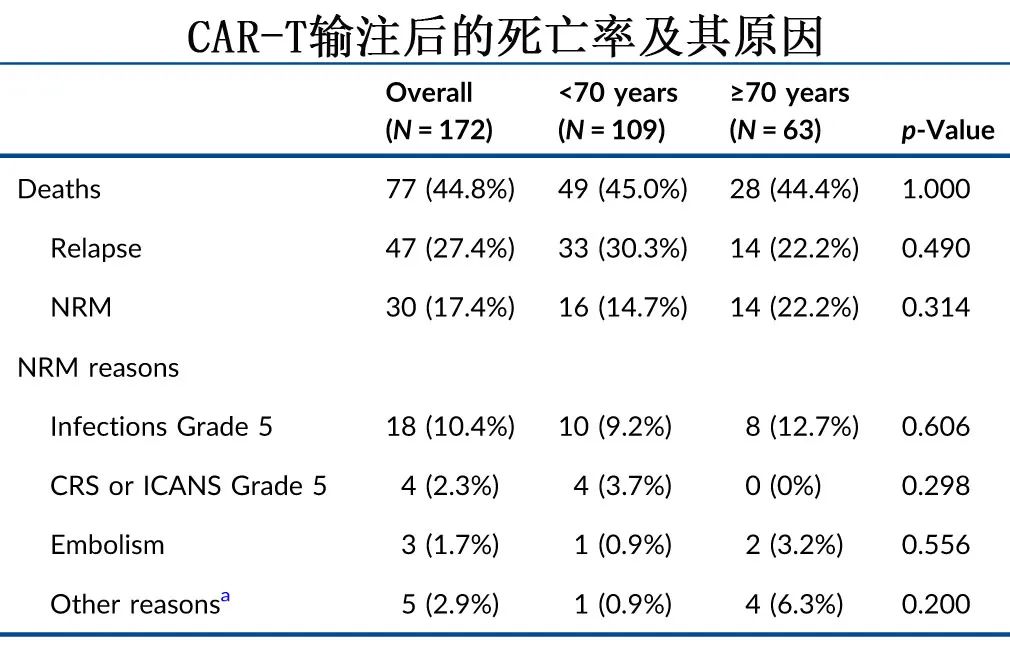
为排除偏倚,对两个年龄组进行1∶1相关性评分匹配(PSM),结果毒性、缓解率、PFS(P=0.47)、OS(P=0.48)、切换率(P=0.51)和NRM (P=0.93)仍相似。
总结
该研究结果进一步支持CAR‐T细胞疗法在≥70岁的r/r DLBCL患者中是可行和有效的,其结局与年轻患者相当。但也需要警惕感染并发症和CAR-T细胞治疗后的NRM,特别是在老年患者中。对于老年r/r DLBCL患者,不应仅因年龄而拒绝CAR-T细胞治疗,但未来需要更长随访时间的研究来进一步评估接受CAR-T细胞治疗的老年DLBCL患者的长期安全性和疗效。
参考文献
1.National Institutes of Health. Cancer Stat Facts: NHL—Diffuse Large B‐cell Lymphoma (DLBCL). NIC; 2020.
2.Kühnl A, Cunningham D, Counsell N, et al. Outcome of elderly patients with diffuse large B‐cell lymphoma treated with R‐CHOP: results from the UK NCRI R‐CHOP14v21 trial with combined analysis of molecular characteristics with the DSHNHL RICOVER‐ 60 trial. Ann Oncol. 2017;28(7):1540‐1546. doi:10.1093/annonc/ mdx128
3.Delarue R、Tilly H、Mounier N 等人。剂量密集型利妥昔单抗-CHOP 与标准利妥昔单抗-CHOP 在老年弥漫性大 B 细胞淋巴瘤患者中的比较(LNH03-6B 研究):一项随机 3 期试验。柳叶刀 Oncol。2013;14(6):525‐533。doi:10.1016/S1470-2045(13)70122-0
4Abramson JS、Solomon SR、Arnason J 等人。Lisocabtagene maraleucel 作为大 B 细胞淋巴瘤的二线治疗:3 期 TRANSFORM 研究的初步分析。血。2023;141(14):1675-1684。doi:10.1182/blood.2022018730
5.Locke FL、Miklos DB、Jacobson CA 等人。Axicabtagene ciloleucel 作为大 B 细胞淋巴瘤的二线治疗。N Engl J Med.2022;386(7):640‐654。doi:10.1056/NEJMoa2116133
6.Lunning MA 等人。axicabtagene ciloleucel 与化学免疫疗法相比,对老年患者和/或 2 线或以上既往治疗后患有复发性或难治性大 B 细胞淋巴瘤且 ECOG 表现状态不佳的患者的益处。Am J Hematol 。2024 年 3 月 19 日。doi:10.1002/ajh.27283。
7.Berning P 等人。嵌合抗原受体 T 细胞疗法在 70 岁及以上的弥漫性大 B 细胞淋巴瘤患者中显示出与年轻患者相似的疗效和毒性:一项多中心队列研究。Hemasphere。2024 年 3 月 20 日;8(3):e54。doi:10.1002/hem3.54。
作者:聊聊血液
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#CAR-T# #DLBCL#
14