最新Nature系列综述:靶向肿瘤血管疗法
2024-09-04 BioMed科技 BioMed科技
综述靶向肿瘤血管方法,包括多种抗血管生成策略及与免疫的关系,为癌症治疗提供新思路,强调血管在肿瘤中的关键作用及未来研究方向。
随着血管生成被认为是癌症生长和存活的核心标志,人们已经实施了几种策略来靶向肿瘤血管系统。迄今为止,其中一些策略,加上标准的护理,已经转化为更加先进的癌症疗法,但它们的成功仅限于某些癌症类型。
在本综述中,比利时鲁汶VIB-KU癌症生物学中心Gabriele Bergers和伦敦玛丽女王大学Kairbaan Hodivala-Dilke等人概述了这些血管靶向方法,并根据对肿瘤血管系统作为肿瘤微环境不可或缺的一部分的理解进行了阐述,肿瘤血管系统在功能上与肿瘤微环境相互关联。这些发现可实现对血管和免疫细胞室的双重靶向,并为未来研究可能的替代方法奠定了基础,以改善癌症治疗。相关工作以“Targeting the tumour vasculature: from vessel destruction to promotion”为题发表在Nature Reviews Cancer。

【文章要点】
在最近对肿瘤血管功能领域的扩展理解而出现的替代血管调节概念的背景下,本综述主要关注抗血管生成疗法,包括抗血管生成治疗、血管破坏策略、促进血管策略、靶向旁分泌信号、血管正常化(图1)、血管生成和免疫抑制、抗血管生成免疫疗法(图2)等等。这些新想法,其中大多数尚未在临床环境中进行测试,但可以为改进癌症治疗的替代血管靶向策略提供基础。
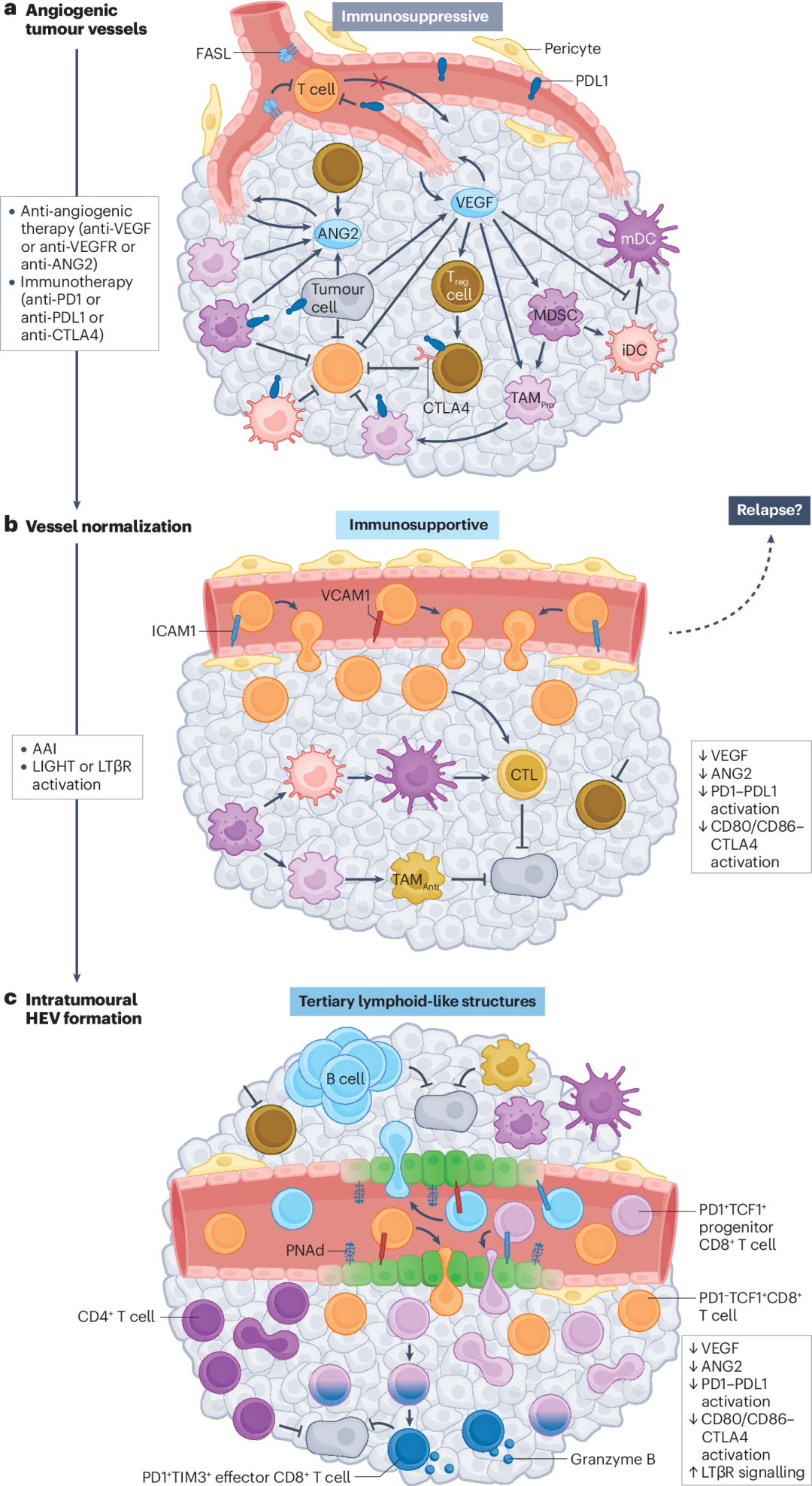
图1 重建血管以获得有效的抗肿瘤免疫
最后,作者还指出,血管是肿瘤的中心和关键隔室,除了免疫细胞外,还与各种其他细胞类型相互作用。特别是神经系统,它与脉管系统密切相互作用,并共享类似的发育、生长和分化信号。最突出的例子是促进血管和神经元生长的不同VEGF配体。前列腺癌症、胰腺导管腺癌或胶质母细胞瘤中交感神经系统的肾上腺素能神经不仅可以促进癌症细胞的增殖,而且还可以促进肿瘤炎症并支持肿瘤血管生成。这些神经与血管紧密并置,因为它们在发育过程中生长在一起,肾上腺素能神经引导器官的血管结构。鉴于这种串扰,可以想象肿瘤内神经和血管会在抗血管生成、神经靶向或免疫调节疗法的反应中相互影响,因此这值得进一步研究。综上所述,本综述中描述的研究证明了血管细胞在肿瘤发生中的关键和复杂作用,以及不同的血管治疗策略如何影响不同的肿瘤微环境成分和随后的肿瘤行为。在针对肿瘤微环境的治疗策略中使用肿瘤的空间组学分析的新兴趋势可能会为肿瘤血管系统和肿瘤微环境其他成分之间的复杂关系提供更全面的视角和新的理解。

图2 将肿瘤血管重编程为高内皮小静脉的简单模型
原文链接:
https://www.nature.com/articles/s41568-024-00736-0
作者:BioMed科技
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#肿瘤微环境# #免疫疗法# #抗血管生成疗法# #靶向肿瘤血管#
13