Blood:中国科学技术大学魏海明/田志刚发现,异基因造血干细胞移植治疗急性髓细胞性白血病复发的潜在机理
2022-08-22 iNature iNature
该研究结果揭示了解释 BMNK 细胞功能障碍的机制,并表明靶向抑制 TGF-β1 信号传导可能代表一种潜在的治疗干预措施,以改善接受 allo-HSCT 或基于 NK 细胞的免疫治疗的 AML 患者的
急性髓性白血病 (AML) 是一种侵袭性血液系统恶性肿瘤,在老年人中发病率较高,在过去几十年中给血液学家带来了挑战。异基因造血干细胞移植 (allo-HSCT) 是一种有效的治疗方法,也是大多数 AML 患者的唯一治愈选择。即使采用目前的治疗方法,移植后原始疾病的复发仍然很频繁,并且与特别差的结果相关。特别是,allo-HSCT 后第 100 天后,复发成为主要的死亡原因。然而,导致早期复发的潜在机制知之甚少,需要进一步研究。

AML 复发与 AML 细胞逃避免疫监视的能力有关。自然杀伤 (NK) 细胞在癌症的免疫监视中起着至关重要的作用。最近,一些研究表明,allo-HSCT 后 NK 细胞对 AML 细胞杀伤的下调可能有助于 AML 细胞逃避免疫监视。NK 细胞在移植后的前 100 天内可能占外周血淋巴细胞的 80%。
NK 细胞通过胞吐作用杀死白血病细胞,这些颗粒含有细胞溶解相关蛋白如粒酶、效应细胞因子如干扰素-γ (IFN-γ) 和肿瘤坏死因子 α (TNF-α) 的分泌。然而,由于免疫抑制因子如 TGF-β1 的作用,肿瘤细胞经常在肿瘤微环境中逃避 NK 细胞介导的细胞毒性和免疫监视。AML 患者中功能受损的 NK 细胞表现出激活受体表达减少和抑制受体表达增加。
TGF-β1 在调节免疫反应中起着不可或缺的作用,主要通过与 TGF-β 受体 (TGF-βR) 复合物结合来触发信号传导。它由两个 I 型 TGF-β(TGF-βRI,也称为 ALK5)和两个 II 型 TGF-β(TGF-βRII)受体亚基组成。两种受体都是丝氨酸/苏氨酸激酶。TGF-β1 以无活性二聚体复合物的形式产生,在发挥其功能作用之前经历活化和加工。Glycoprotein-A repetitions predominant (GARP) 是一种 I 型跨膜细胞表面对接受体,在血小板和调节性 T (Treg) 淋巴细胞上大量表达,并调节 TGF-β1 的激活。
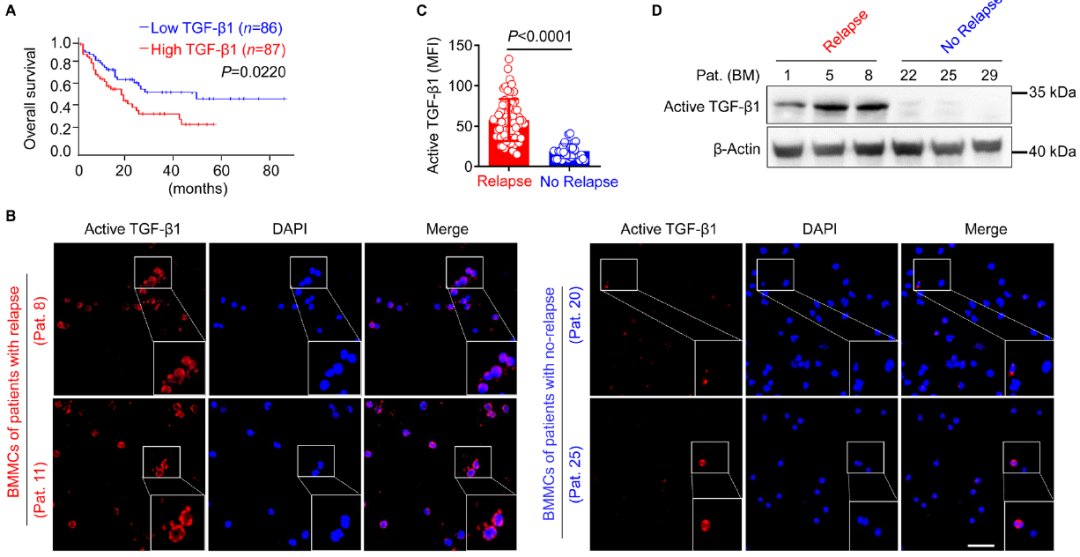
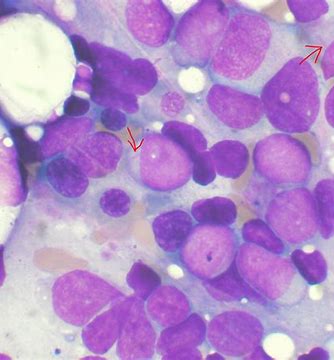
allo-HSCT 后早期复发的 AML 患者骨髓中活性 TGF-β1 水平显著上调(图源自Blood )
活性TGF-β1可以抑制NK细胞和 CD8+ T细胞的效应功能。阻断 TGF-β1 通路已成为恢复抗肿瘤免疫的有吸引力的方法。Galunisertib 是一种口服给药的 TGF-βR1 激酶小分子抑制剂。它通过特异性下调 SMAD2 的磷酸化来消除经典 TGF-β1 途径的激活。在几种小鼠模型中显示了其抑制肿瘤细胞增殖的能力。然而,导致骨髓 NK (BMNK) 细胞功能障碍的机制尚未在 AML 患者中得到充分表征。因此,抑制 TGF-β1 信号传导是否可以恢复复发性 AML 患者的抗肿瘤活性仍不清楚。
在这项研究中,进行了离体实验,以研究在 allo-HSCT 后复发的 AML 患者骨髓中 TGF-β1 活化的机制。 该研究还探索了 TGF-β1 诱导 BMNK 细胞功能障碍的机制。此外,该研究想确定是否可以通过抑制 TGF-β1 信号传导来恢复 NK 细胞的体外和体内抗肿瘤活性。
该研究证明了较高水平的活性转化生长因子-β1 (TGF-β1) 与这些 AML 患者中 BMNK 细胞的效应功能受损有关。 TGF-β1 活化是由 CD4+ T 细胞表面上Glycoprotein-A repetitions predominant (GARP) 的过表达诱导的。活性 TGF-β1 显著抑制 mTORC1 活性、线粒体氧化磷酸化、BMNK 细胞的增殖和细胞毒性。
此外,用临床阶段 TGF-β1 通路抑制剂 galunisertib 进行预处理显著恢复了 mTORC1 活性、线粒体稳态和细胞毒性。重要的是,阻断 TGF-β1 信号通路提高了 NK 细胞在白血病异种移植小鼠模型中的抗肿瘤活性。因此,该研究结果揭示了解释 BMNK 细胞功能障碍的机制,并表明靶向抑制 TGF-β1 信号传导可能代表一种潜在的治疗干预措施,以改善接受 allo-HSCT 或基于 NK 细胞的免疫治疗的 AML 患者的预后。
参考消息:
https://ashpublications.org/blood/article/doi/10.1182/blood.2022015474/486316/GARP-mediated-active-TGF-1-induces-bone-marrow-NK
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





#中国科学#
81
#干细胞移植治疗#
88
#细胞性#
120
#中国科学技术大学#
80
#细胞移植#
81