Nat Commun:I期临床试验: 全反式视黄酸作为胰腺癌基质靶向药物
2020-09-27 haibei MedSci原创
在一项针对晚期不可切除的PDAC患者(n = 27)的Ib期、剂量升级和扩展试验中,采用两步自适应持续再评估法试验设计,ATRA作为基质靶向药物与gemcitabine-nab-紫杉醇化疗联合使用。
晚期胰腺导管腺癌(PDAC)预后不佳,现有的治疗方案效果不大。促结缔织增生的基质和低血管性是PDAC的显著特征,阻碍了化疗药物的成功输送。胰腺星状细胞(PSC),结缔组织生成关键的组成部分和诱导物,通过多个信号级联介导了癌细胞的亲生存和亲入侵能力。这种肿瘤-基质交叉对话不太可能仅仅通过针对单一途径的疗法有效阻断。而通过多个角度针对肿瘤-基质细胞的相互作用(如促结缔组织增生的基质的正常化)可能会增强常规化疗的有效性。
PDAC患者由于胆汁和胰腺分泌受损,表现出脂溶性维生素的缺乏。虽然维生素K缺乏在临床上有表现和治疗,但缺乏维生素A可能会使PSC长期活化,临床上还没有认识到这一点。
在健康的胰腺中,PSC储存着维生素A(视黄醇)的代谢产物[视黄酸(RA)]。当其在在癌症或炎症中被激活,PSC失去RA的存储,并表现出激活的肌成纤维细胞表型。此外,RA也是一个调节关键信号通路的重要分子,介导胚胎胰腺发育,信号级联,在胰腺癌发生期间被劫持。

基于这些观察,研究人员已经证明,在各种PDAC实验模型中,使用全反式视黄酸(ATRA)可以在PSC内恢复RA库,限制了结缔组织增生,以及抑制了肿瘤生长。此外,研究人员发现激活的PSC阻碍了免疫细胞迁移进入直接的PDAC微环境,如CD8 + T细胞,自然杀伤力和B细胞,这个过程可以被ATRA5逆转。因此,ATRA是抑制PDAC中激活的多种、放大的、胚胎的、特定环境的信号级联的理想药物。
最近,研究人员在Nature Communications杂志发文,在一项针对晚期不可切除的PDAC患者(n = 27)的Ib期、剂量升级和扩展试验中,采用两步自适应持续再评估法试验设计,ATRA作为基质靶向药物与gemcitabine-nab-紫杉醇化疗联合使用。
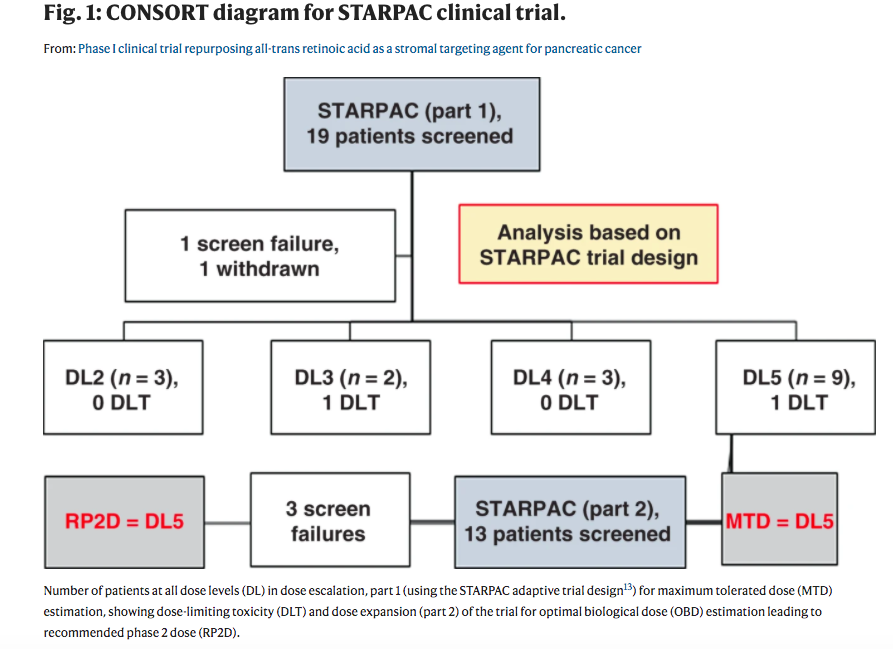
最大耐受剂量(MTD)和2期推荐剂量(RP2D,主要结果)为FDA/EMEA批准的gemcitabine-nab-紫杉醇剂量与ATRA一起使用(45mg/m2口服,第1-15天/周期)。剂量限制性毒性(DLT)为4级血小板减少症(n = 2)。
次要结果显示,对ATRA药代动力学无损害。RP2D治疗评价人群的中位总生存期是11.7个月(95%CI 8.6-15.7个月,n = 15,局部晚期和转移性)。探索性药效学研究包括一个周期后扩散加权(DW)-MRI测量的表观扩散系数的变化,以及,表征基质调控的周期特异性血清五羟色胺3水平在不同周期内的调控。
基线基质特异性视黄素转运蛋白(FABP5,CRABP2)的表达可能是反应的预示。
总之,联用gemcitabine-nab-紫杉醇和ATRA作为基质靶向药物是安全和耐受的。该组合将在一项II期随机对照试验中对局部晚期PDAC进行评估。临床试验编号 EudraCT:2015-002662-23;NCT03307148。试验简称:STARPAC。
原始出处:
Hemant M. Kocher et al. Phase I clinical trial repurposing all-trans retinoic acid as a stromal targeting agent for pancreatic cancer. Nature Communications(2020).
作者:haibei
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#基质#
74
#Nat#
69
#全反式视黄酸#
79
#I期临床试验#
57
#COMMUN#
89