Cell Death Dis:SPATS2调控细胞周期促进肝癌的发生发展
2020-10-20 星云 MedSci原创
肝细胞癌(HCC)作为全球第六大最常见的肿瘤,也是癌症相关死亡的第三大诱因。尽管外科手术切除、动脉化疗栓塞、射频消融术和肝移植等治疗策略目前已取得较大的进展,但HCC的五年生存率仍不足10%。由于确诊
肝细胞癌(HCC)作为全球第六大最常见的肿瘤,也是癌症相关死亡的第三大诱因。尽管外科手术切除、动脉化疗栓塞、射频消融术和肝移植等治疗策略目前已取得较大的进展,但HCC的五年生存率仍不足10%。由于确诊时已为晚期以及疾病的复发等因素,导致肝癌的预后不良。因此,进一步研究HCC发生发展的相关机制并鉴定新的HCC诊断标记物显得尤为重要。
SPATS2被预测为一种胞质RNA结合蛋白,最初在睾丸中发现,并在精子的发生中起着至关重要的作用。SPATS2参与多种恶性肿瘤的发生发展。然而SPATS2在HCC中的表达水平以及相关的分子功能仍不完全清楚。
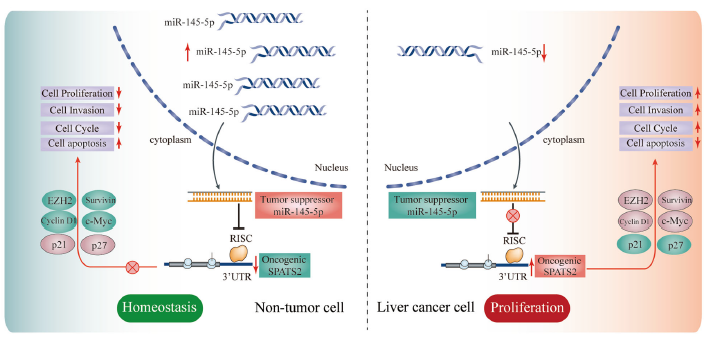
在HCC中MiR-145-5p/SPATS2通路调控细胞凋亡和细胞周期
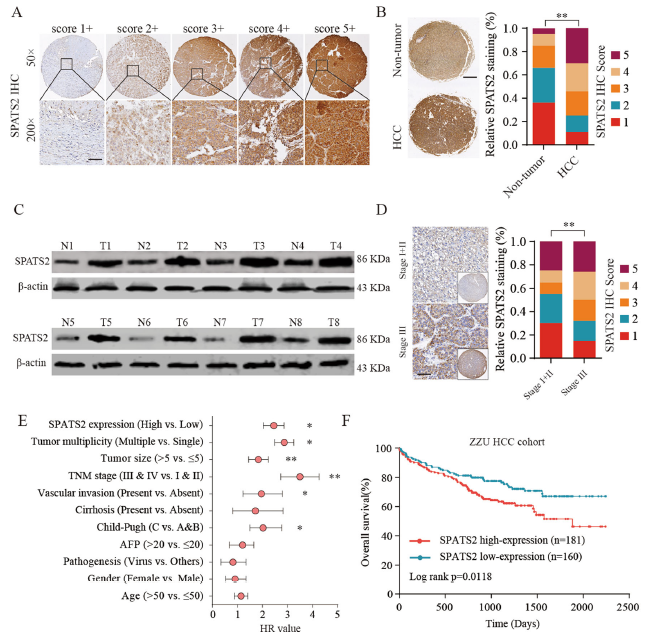
该研究旨在揭示SPATS2在肝癌中的表达谱和功能作用,并探讨SPATS2的相关调控作用。研究人员发现,相比于邻近的正常组织,SPATS2在HCC组织中呈现高表达水平。SPATS2的高表达水平也与血管的浸润、晚期TNM分期、肿瘤的多样性和不良的生存率息息相关。
SPATS2在HCC组织中表达上调且与HCC患者的不良预后相关
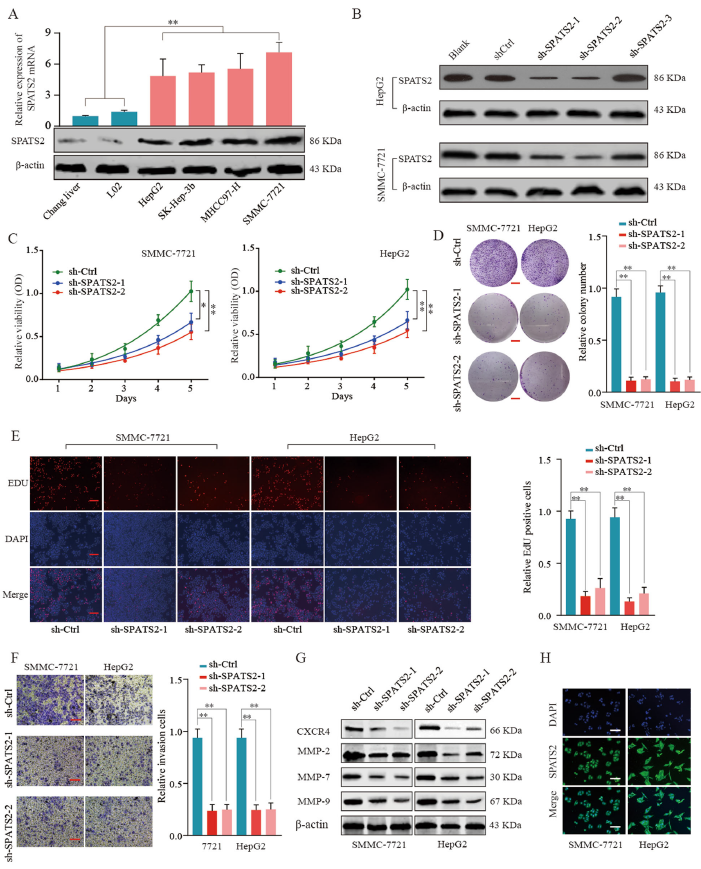
功能研究显示,SPATS2能够促进HCC细胞的增殖和转移,而敲除SPATS2则能够增强HCC细胞的凋亡作用且细胞周期阻滞于G1。生物信息学分析显示,MiR-145-5p能够直接靶向SPATS2,而功能拯救rescue实验显示,过表达MiR-145-5p可消除SPATS2对HCC恶性的调节作用。
(
敲低SPATS2可抑制肝癌细胞的恶性程度
综上所述,该研究结果揭示了在HCC中SPATS2所起的致癌基因的作用。MiR-145-5p/SPATS2通路也为HCC的发生发展提供了潜在的新机制,可作为HCC的潜在治疗靶标。
原始出处:
Dong, G., Zhang, S., Shen, S. et al. SPATS2, negatively regulated by miR-145-5p, promotes hepatocellular carcinoma progression through regulating cell cycle. Cell Death Dis 11, 837 (09 October 2020).
作者:星云
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#Cell#
45
#ATS#
46
#CEL#
53
#SpA#
55
#Dis#
60