Cell Metab:颠覆认知!脂肪组织竟是糖尿病罪魁祸首!
2018-10-17 奇点糕 奇点网
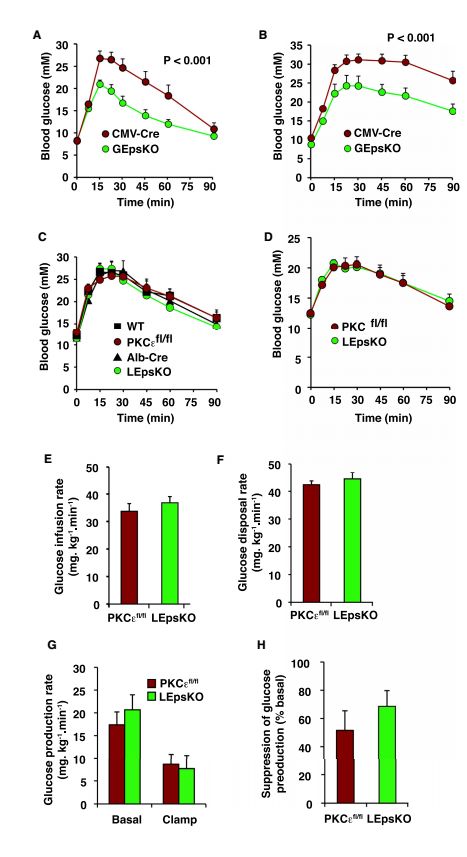
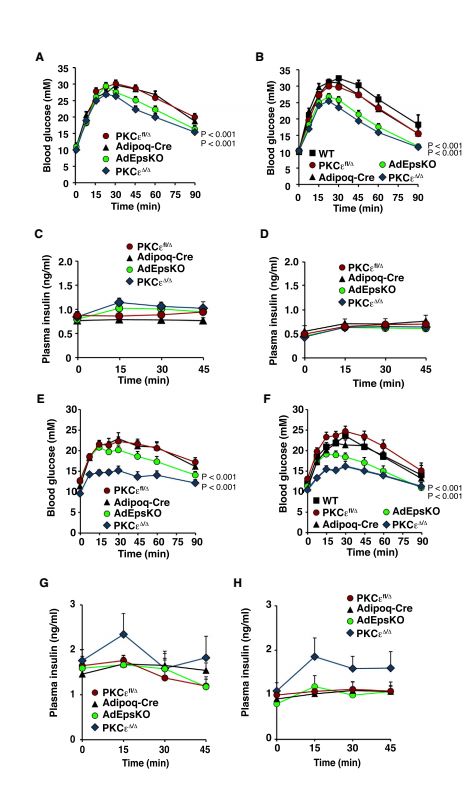
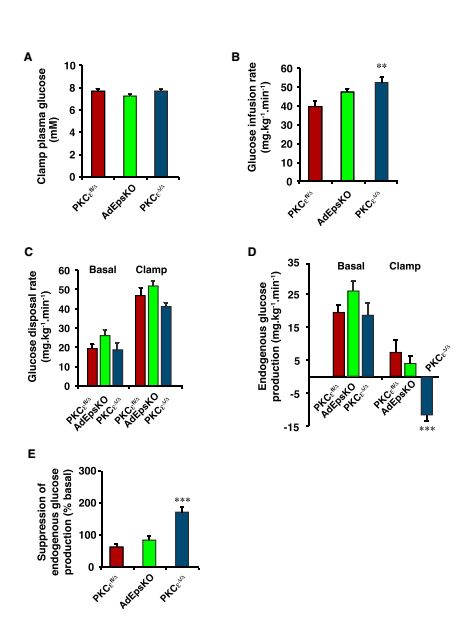
研究人员将目光放到了每个人都有的组织—脂肪上。他们发现,只要去除糖尿病小鼠全身脂肪组织中的PKCε,小鼠就不会出现葡萄糖耐受不良,换言之,就是胰岛素抵抗消除!
作者:奇点糕
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#Meta#
36
#Cell#
31
#CEL#
40
学习了谢谢
81
#MET#
26