Immunity:新的anti-CD25抗体,使抑制肿瘤内的Treg细胞的免疫疗法重获生机
2017-04-17 MedSci MedSci原创
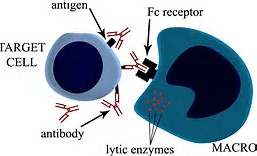
接着研究组改良了原来的anti-CD25 r1抗体,使其能更好的结合起作用的I,III,IV型Fc gamma受体,结果改良后的抗体相较于原来的抗体能够更好的杀死肿瘤组织中的Treg细胞。并且如果搭配使用时下刚被美国FDA批准使用的anti-PD-L1抗体使用,能够起到加成的作用。即杀死了肿瘤中的Treg细胞,同时又使原来疲惫的Teff细胞重新恢复活性。 这项研究使本来已经失去研究重心的an
作者:MedSci
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#CD25#
47
#Immunity#
44
#抑制肿瘤#
58
#Treg细胞#
60
#Treg#
59