【TCT】淋巴细胞计数与ide-cel治疗多发性骨髓瘤的结局相关
2024-06-12 聊聊血液 聊聊血液
美国多中心学者开展一项大样本真实世界研究,旨在评估从单采到清淋时外周血ALC的深度变化如何影响接受ide-cel标准治疗 (SOC)的临床结局。
淋巴细胞计数的预测价值
BCMA CAR-T细胞来疗法Idecabtagene vicleucel (ide-cel)在复发难治性多发性骨髓瘤(RRMM)中显示出令人印象深刻的疗效。CAR-T细胞的疗效取决于多种内在因素,包括制造前后的T细胞表型、CAR-T细胞的持续和扩增以及肿瘤特征,也有CAR-HEMATOTOX模型等用于预测患者预后。但很多因素在常规临床实践中不容易测试,或不足以单独预测长期缓解,或较为复杂。
研究证实,清淋前(pre-LD)的淋巴细胞计数ALC)可能与各种恶性肿瘤(包括淋巴瘤和MM)患者的缓解深度和生存结果有潜在的关联。因此美国多中心学者开展一项大样本真实世界研究,旨在评估从单采到清淋时外周血ALC的深度变化如何影响接受ide-cel标准治疗 (SOC)的临床结局。研究结果近日发表于《Transplantation and Cellular Therapy》。

本文重点
作者探讨了ALC对商业化idecabtagene vicleucel治疗骨髓瘤患者的生存结局的影响。
作者创建了一个新的ALC模型,分为3个分组:清淋前ALC正常,清淋前低ALC +单采前到清淋前的降低率(%R) <37.5,清淋前低ALC+ %R≥37.5。
清淋前低ALC+单采前(pre-A)到清淋前的降低率≥37.5与较差的生存结局相关。
研究结果
患者特征
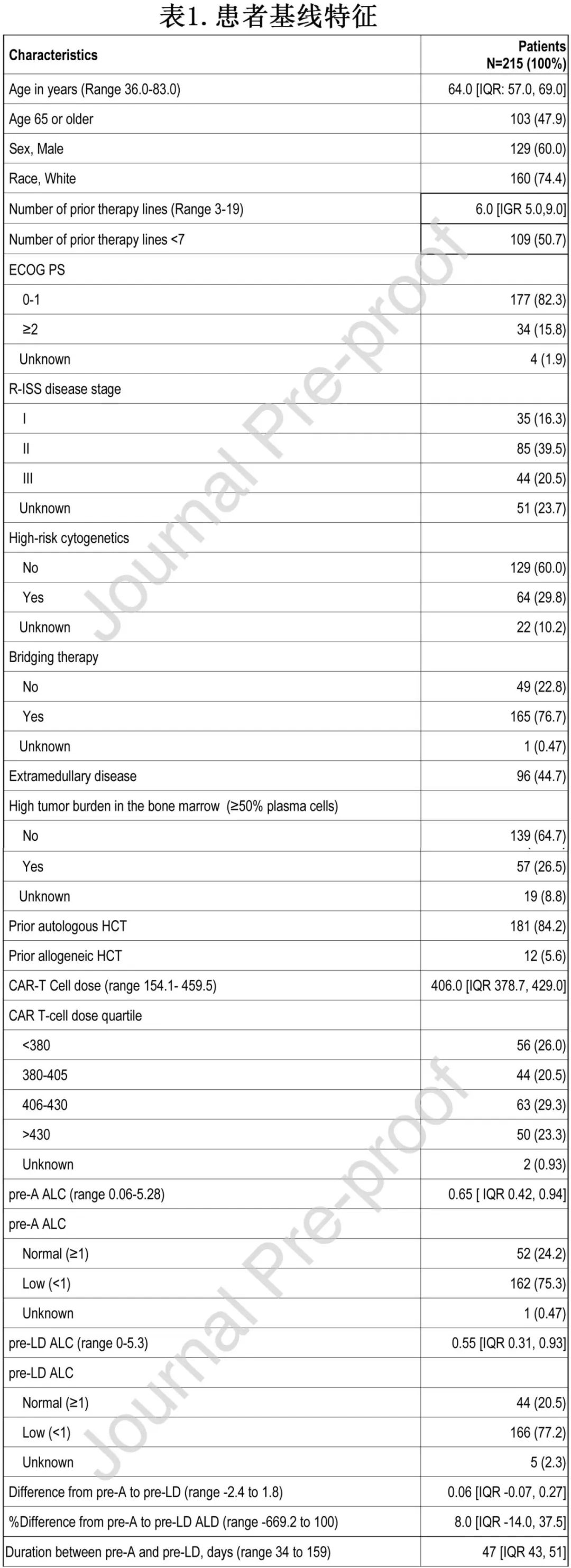
该回顾性研究纳入美国11家中心接受单采的RRMM患者214例,基线特征见表1。中位年龄为64岁,29.8%的患者为高危细胞遗传学,26.5%的患者为高骨髓肿瘤负荷,44.7%的患者存在髓外病变(EMD)。既往治疗中位线数为6。ALC参数如表1所示,包括pre-A、pre-LD、pre-A与pre-LD ALC的绝对差值、差值百分比。清淋前ALC显著低于单采前ALC(中位数为0.55 vs 0.65, p<0.0001)。
ALC特征对PFS和OS的影响
中位随访时间5.4个月,中位PFS为8.1个月,3、6、12个月PFS率分别为77.8%、60%、38.5%。中位OS为12.5个月,3个月、6个月和12个月OS率分别为93.5%,84.9%和61.9%。
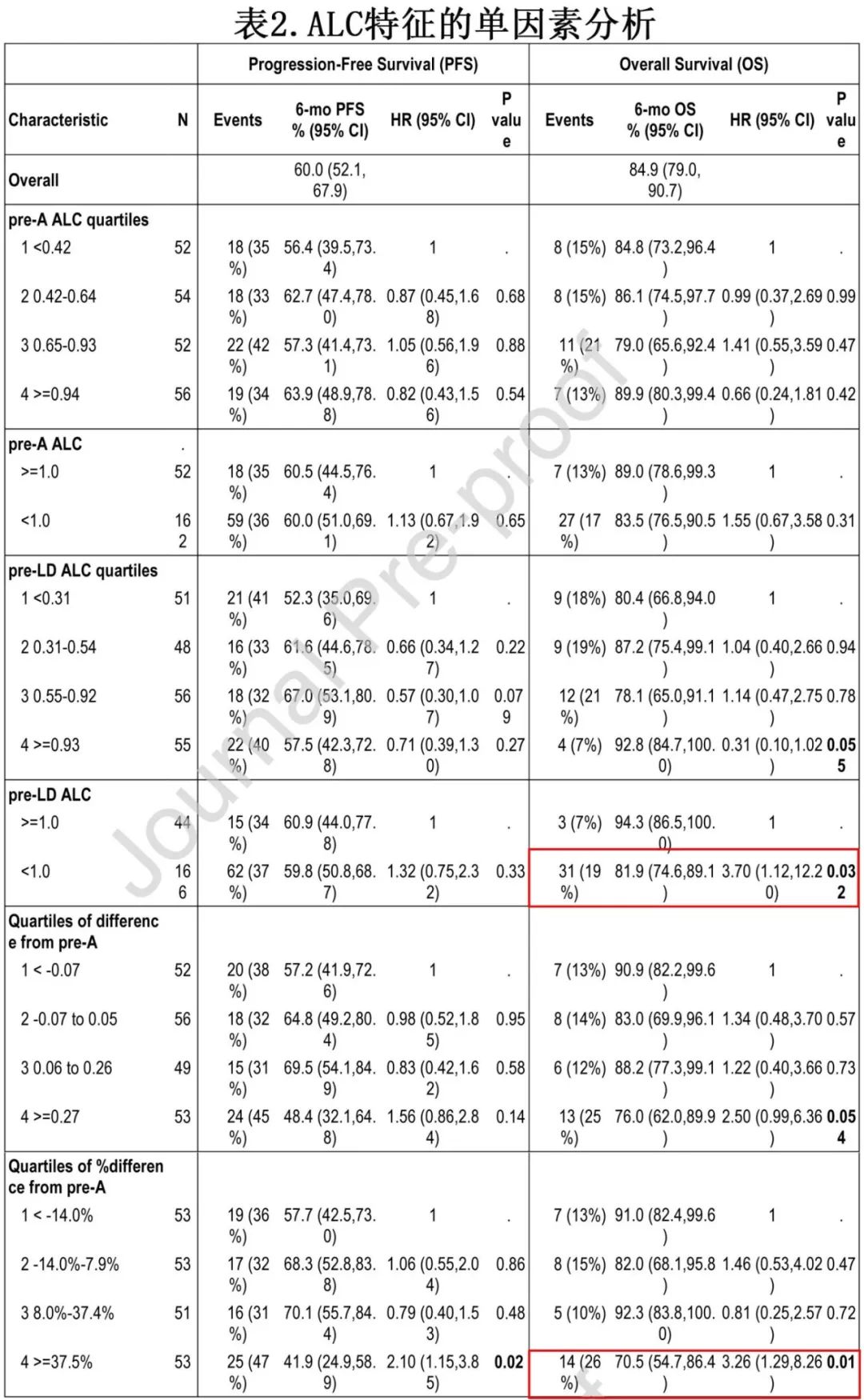
在单因素分析中评估异常的单采前和清淋前ALC的影响以及所有ALC参数的四分位数水平对PFS和OS的关联。证实清淋前正常ALC对比低ALC的OS有差异,ALC从单采前到清淋前的降低率(%R)以37.5%为界同样影响OS。
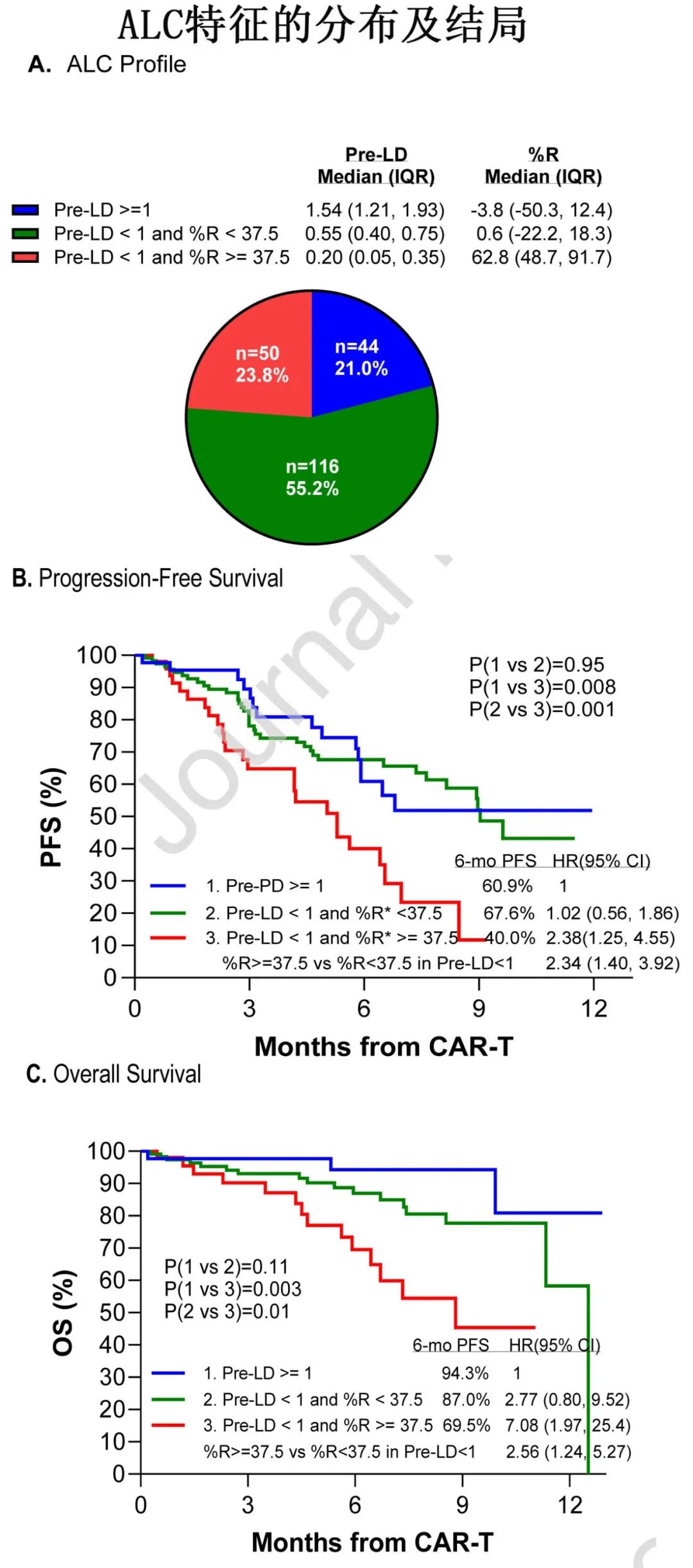
基于单因素分析建立了新的ALC模型,包括三组:清淋前正常ALC (≥1×109/L) 、清淋前低ALC(<1×109/L) +单采前到清淋前的降低率(%R) <37.5和清淋前低ALC+%R≥37.5,分别占21%、55.2%和23.8%的患者,6个月PFS分别为40%、67.6%和60.9%,6个月OS分别为69.5%、87% 和94.3%;此外30天ORR分别为87.8%、77.6%和69.8%,≥2级神经系统事件分别为4.9%、12.3%和14.9%,≥2级CRS分别为27.9%、16.5%和12%(p=0.04)。
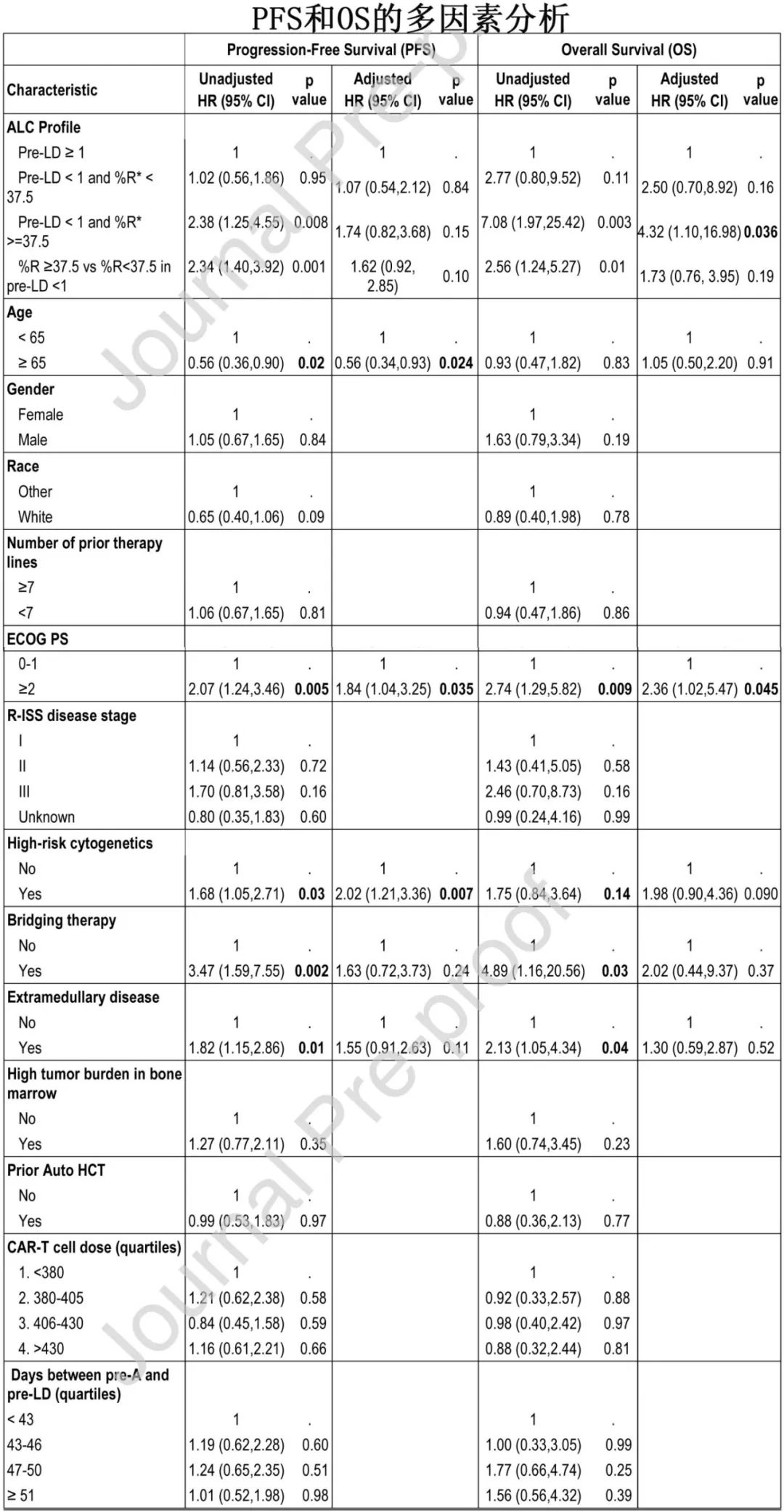
在多因素分析中,在校正年龄、运动状态、细胞遗传学风险、桥接治疗的使用和髓外病变后,ALC对PFS的影响未保持统计学意义;但与清淋前正常ALC组相比,清淋前低ALC+%R≥37.5组的OS仍明显较差(HR=4.3,P=0.036),但清淋前低ALC+%R≥37.5组与清淋前低ALC+%R<37.5组之间无统计学差异(HR=1.73,P=0.13)。
总结
该研究表明,在接受SOC ide-cel治疗的患者中,清淋前低ALC+单采前到清淋前ALC高降低率与较差的生存结局(特别是OS)相关。但还要开展更大规模的研究来进一步研究ALC与ide-cel后生存结局的关系,以证实该结果并提供ALC预测价值的更有力证据,包括37.5%的ALC降低阈值可能并非最佳。
参考文献
Khouri J, et al. Absolute Lymphocyte Count and Outcomes of Multiple Myeloma Patients Treated with Idecabtagene Vicleucel: The U.S. Myeloma Immunotherapy Consortium Real World Experience, Transplantation and Cellular Therapy (2024), doi: https://doi.org/10.1016/j.jtct.2024.05.025
作者:聊聊血液
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#多发性骨髓瘤# #淋巴细胞计数#
9