【Nat Med】Isa-VRd对比IsaRd治疗不适合移植NDMM的3期研究
2024-06-15 聊聊血液 聊聊血液
3 期研究比较 Isa-VRd 与 IsaRd 对不适合移植的 NDMM 患者疗效,Isa-VRd 显著提高 18 个月 MRD 阴性率等,或成新标,安全性可,随访期未现生存期差异。
Isa-VRd
CD38单抗联合来那度胺和地塞米松的三药方案已成为不适合移植 (TI)的新诊断多发性骨髓瘤(NDMM)患者额最佳标准治疗(SOC)。为了进一步改善SOC,尤其是提高MRD阴性率和预防复发,学者开展一项3期BENEFIT/IFM2020-05研究,在不适合移植NDMM中评估了在艾沙妥昔单抗(Isatuximab)+来那度胺和地塞米松的基础上加入每周硼替佐米(V) 的价值(IsaRd对比Isa-VRd)。研究的初步结果近日发表于《Nature Medicine》。

研究结果
患者及治疗
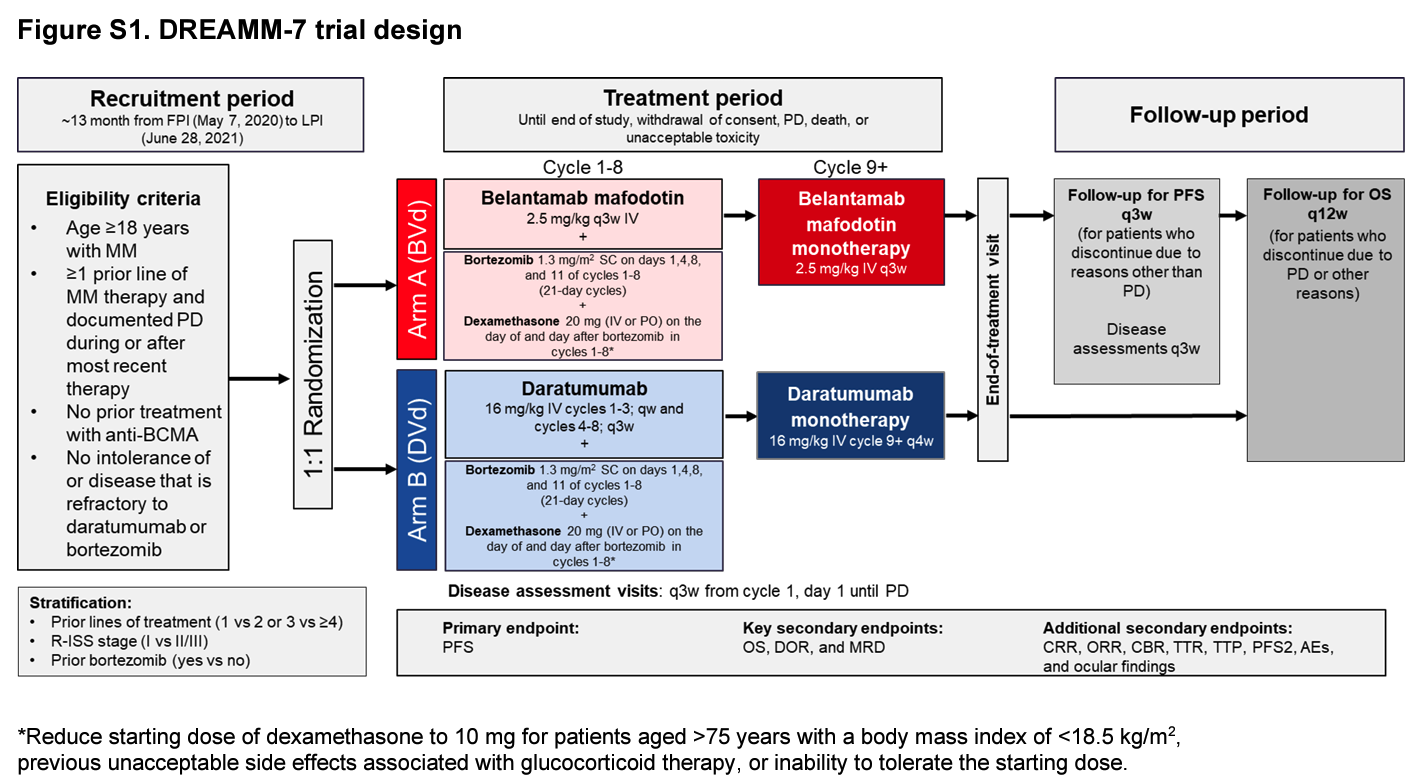
该开放标签、多中心、随机对照研究纳入65-79岁不适合移植的NDMM患者,1:1随机接受Isa-VRd或IsaRd治疗。艾沙妥昔单抗的剂量为10 mg/kg,来那度胺为25 mg,地塞米松为20 mg,硼替佐米为1.3 mg/m2,具体方案如下。
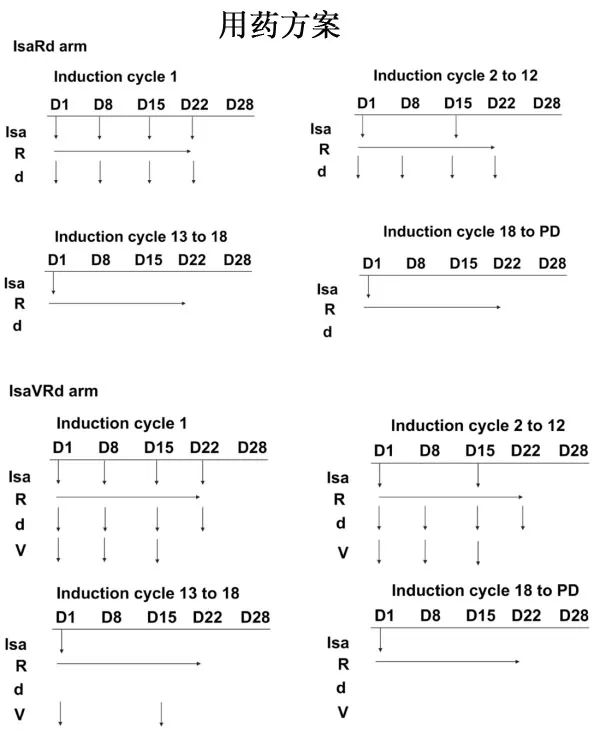
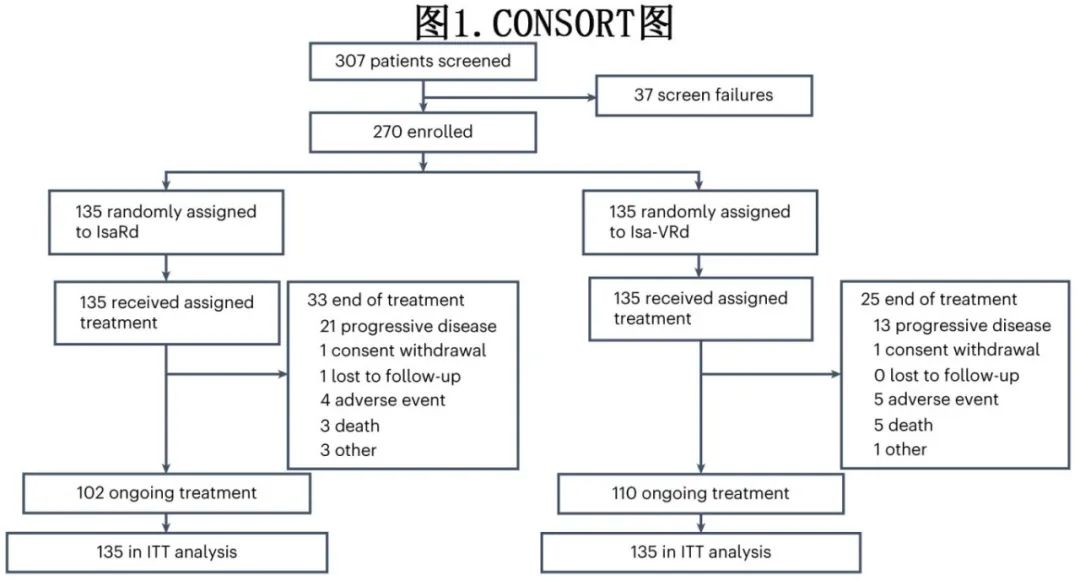
共入组270例患者,Isa-VRd和IsaRd组各135例,均接受至少一次治疗(图1)。
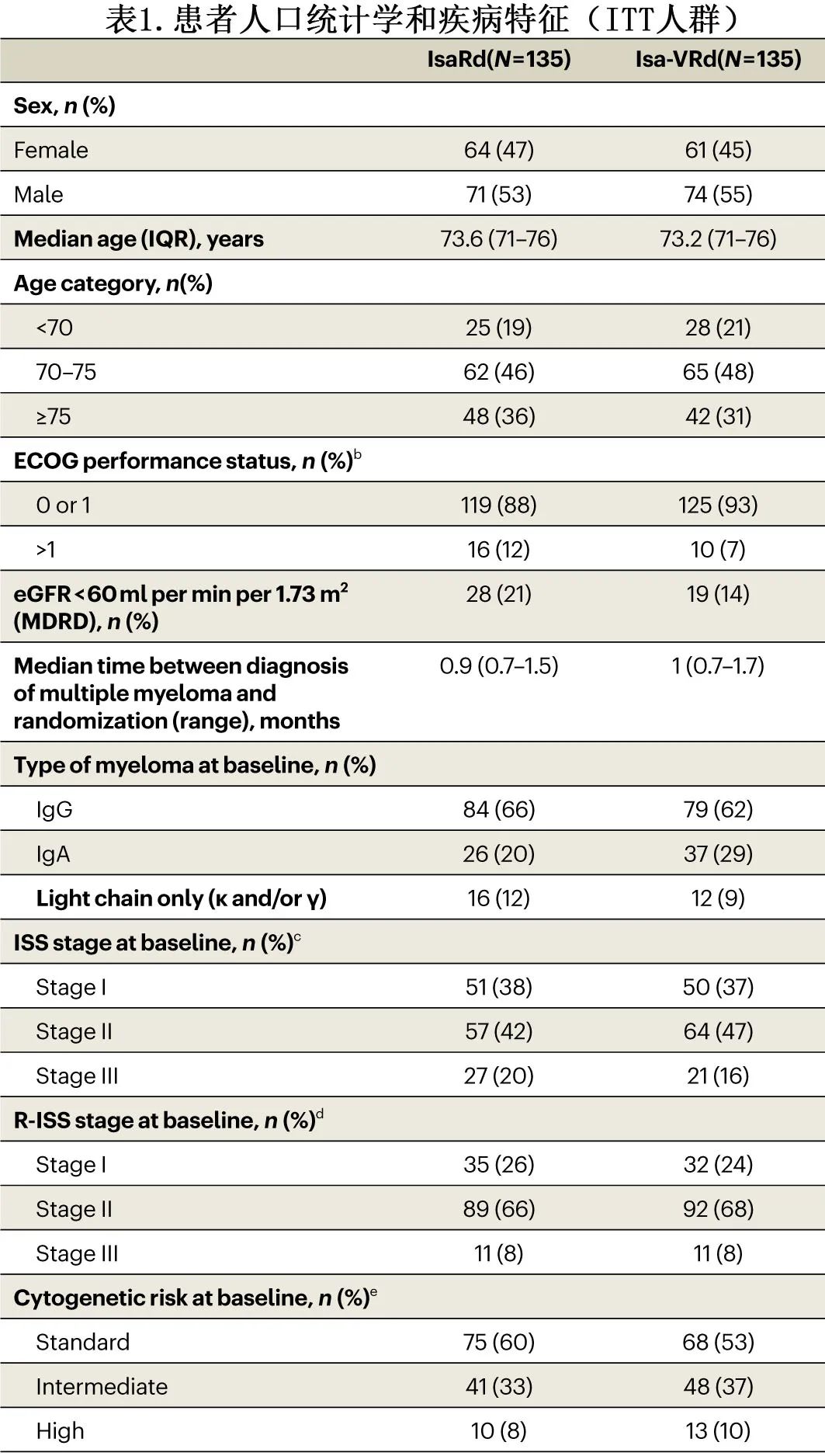
患者基线较为平衡(表1)。
数据截止时,50例(19%)患者停止研究治疗中至少一种药物,其中IsaRd组30例,Isa-VRd组20例;最常见的停药原因为疾病进展:IsaRd 21例(64%),Isa-VRd 13例(52%)。
更准确地说,49例(18%)停用艾沙妥昔单抗(IsaRd组29例和Isa-VRd组20例),49例(18%)停用来那度胺(IsaRd组29例和Isa-VRd组20例),18例(13%)停用硼替佐米。硼替佐米的中位相对剂量强度为91.6%,艾沙妥昔单抗为95.8% (IsaRd组95.8%;Isa-VRd组96.1%),来那度胺为91.1% (IsaRd组为91%;Isa-VRd组为91.7%),地塞米松为95.8% (IsaRd组为97.9%;Isa-VRd组为95.8%) (表2)。
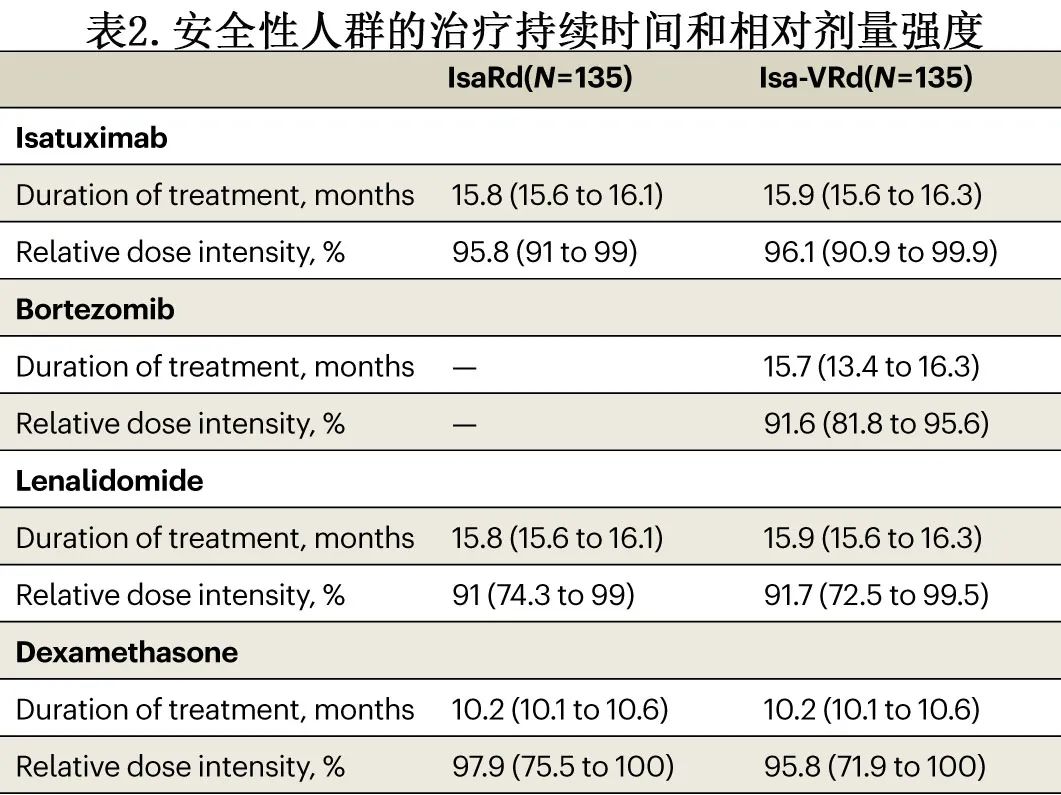
疗效
18个月时106例(39%)患者为MRD阴性(骨髓穿刺,NGS,10-5)。Isa-VRd组的18个月MRD阴性率(10-5)显著高于IsaRd组,分别有71例患者(53%)和35例患者(26%)。Isa-VRd组相对于IsaRd组的MRD阴性比值比(OR)为3.16 (P<0.0001)(图2a)。在12个月时的10-5和10-6灵敏度下,Isa-VRd的MRD阴性率也较高。预先指定的MRD亚组分析证实大多数亚组具有一致获益,包括部分预后因素较差的难治型人群(图2b)。
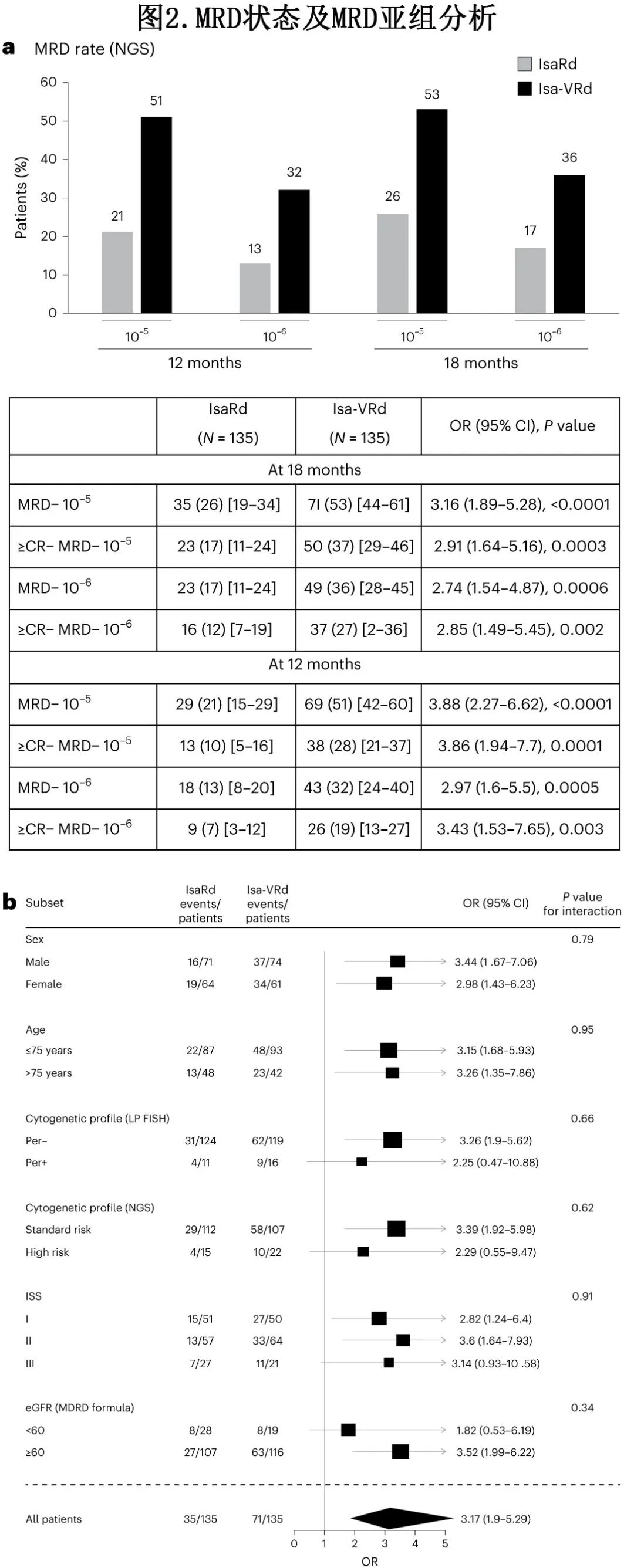
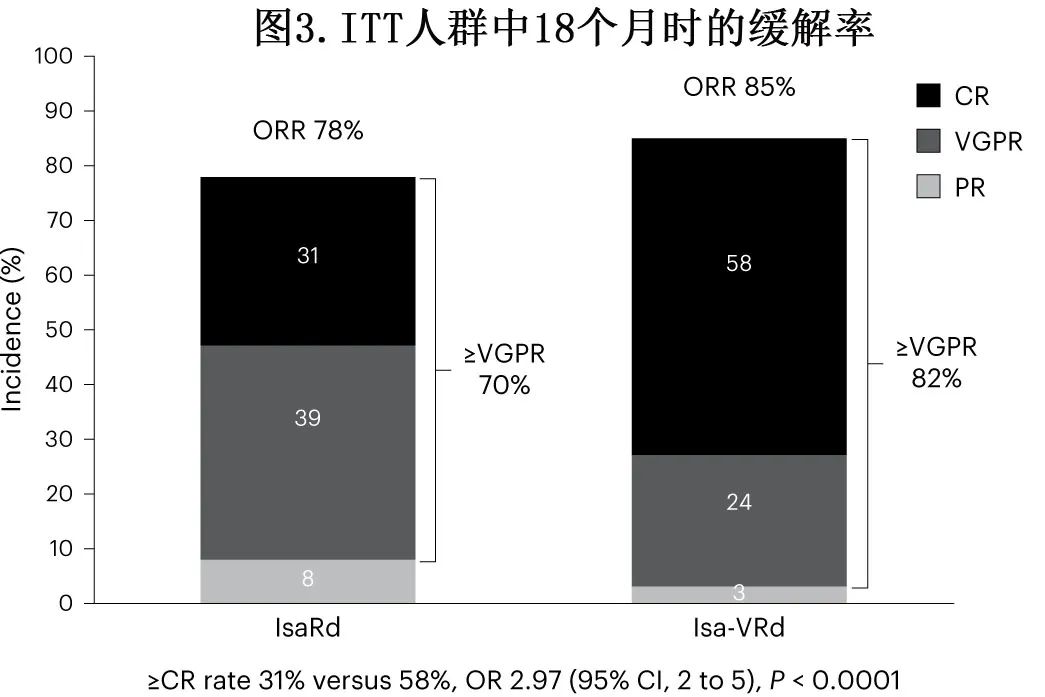
在18个月时,Isa-VRd组的≥VGPR和≥CR率均高于IsaRd,≥CR率为58% vs 31%(OR=2.97,P<0.0001;图3)。IsaRd组患者至首次≥PR(0.99个月 vs 0.95个月)和≥VGPR的时间显著短于Isa-VRd组。
中位随访23.5个月,PFS和OS数据仍不成熟;IsaRd组分别发生21例进展事件和10例死亡,Isa-VRd组分别为13例和11例。IsaRd组24个月PFS和OS分别为80.0%和91.5%,Isa-VRd分别为85.2%和91.1%。
安全性
最常见的不良事件(AE)(两组患者发生率≥10%)见表3。总体而言,最常见的事件为中性粒细胞减少(IsaRd为61%,Isa-VRd为56%)、腹泻(均为48%)和感染(39% vs 47%)。Isa-VRd组的血小板减少发生率高于IsaRd组:任何级别分别为37(27%)和19(14%),≥3级分别为16(12%)和8(5%)。
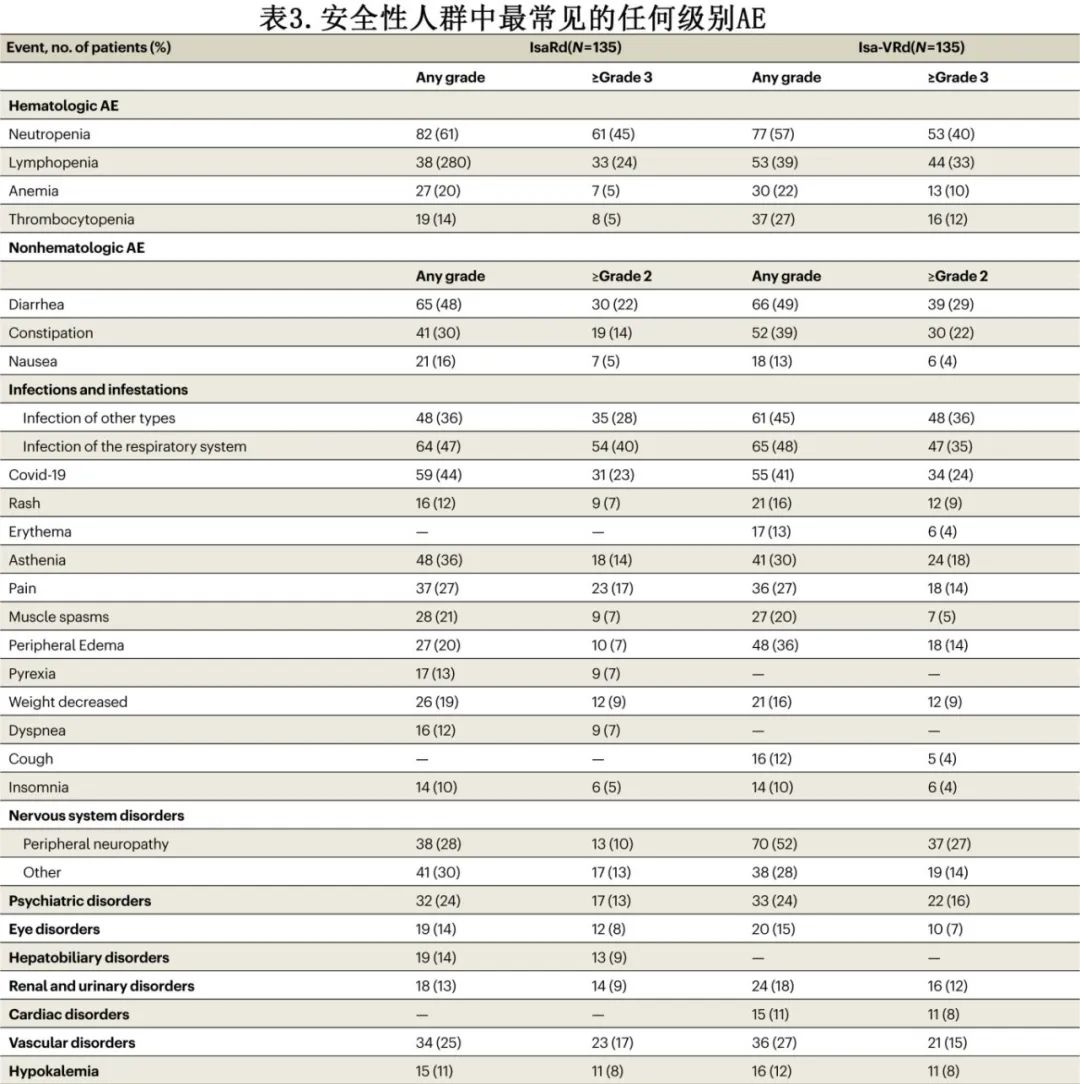
12例患者报告实体瘤作为第二原发恶性肿瘤(14种)(IsaRd组6例[4%],Isa-VRd组6例[4%])。
共报告271起神经系统障碍AE,其中163起(60%)为神经病变,发生于IsaRd组38例患者(28%)和Isa-VRd组70例(52%)患者(表3)。IsaRd组13例(10%)患者发生≥2级周围神经病变(1例为3级),Isa-VRd组37例(27%)患者发生周围神经病变(4例为3级)。16例(10%)患者因≥2级神经系统病变而停用硼替佐米。
总结
该3期研究纳入270例65-79岁的NDMM患者随机分为IsaRd组和Isa-VRd组,两组的18个月MRD阴性率分别为26%和53%(灵敏度10-5,优势比为3.16,P<0.0001)。在灵敏度10-5和10-6时,MRD获益在各亚组中一致,并且在第12个月已经观察到获益。Isa-VRd在18个月时的≥CR率更高(58% vs 31%;P<0.0001),MRD阴性伴≥CR率也是如此(37% vs 17%;P=0.0003)。中位随访23.5个月,没有观察到生存期的差异(数据尚不成熟)。此外每周添加硼替佐米对IsaRd的相对剂量强度没有显著影响。
总的来说,Isa-VRd与IsaRd相比可显著提高MRD阴性率,包括主要终点18个月阴性率(10-5)。Isa-VRd或可作为不适合移植NDMM患者新的标准治疗。
参考文献
Leleu X,et al.Isatuximab, lenalidomide, dexamethasone and bortezomib in transplant-ineligible multiple myeloma: the randomized phase 3 BENEFIT trial.Nat Med . 2024 Jun 3. doi: 10.1038/s41591-024-03050-2.
作者:聊聊血液
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#多发性骨髓瘤# #NDMM# #Isa-VRd#
5