【BCJ】24周期Dara-KRd不伴移植治疗新诊断多发性骨髓瘤的II期研究结果
2024-06-10 聊聊血液 聊聊血液
学者开展了一项单臂II期研究,旨在评估Dara-KRd(24周期)不联合ASCT治疗NDMM的疗效和安全性。研究结果近日发表于《Blood Cancer Journal》。
Dara-KRd不伴移植
对于新诊断多发性骨髓瘤(NDMM),一线自体造血干细胞移植(ASCT)仍是适合移植患者的标准方案,但真实世界中有很多患者并未接受移植。含达雷妥尤单抗的四药诱导方案可获得较深缓解,甚至MRD阴性,例如达雷妥尤单抗联合卡非佐米、来那度胺和地塞米松(Dara-KRd)的MRD阴性率为71%。但由于Dara-KRd的研究中很多患者接受了ASCT,因此无法确定Dara-KRd不伴ASCT时的缓解持续时间。
学者开展了一项单臂II期研究,旨在评估Dara-KRd(24周期)不联合ASCT治疗NDMM的疗效和安全性。研究结果近日发表于《Blood Cancer Journal》。

研究方法&结果
该研究为开放标签、单臂II期研究,纳入≥18岁NDMM患者(不考虑是否适合ASCT),给予24周期Dara-KRd治疗。可在4-6周期后采干,用于未来ASCT,24周期治疗后建议来那度胺维持治疗。C8、C12、C24用NGS评估MRD。主要终点为第8周期(C8)结束时严格意义完全缓解(sCR)和/或MRD<10-5(NGS)的比率,次要终点包括IMWG的缓解率、毒性、MRD状态(NGS)、PFS和OS;此外使用基于质谱的EXENT系统和液相色谱-质谱(LC-MS)对外周血样本进行MRD评估,作为探索性终点。
患者特征
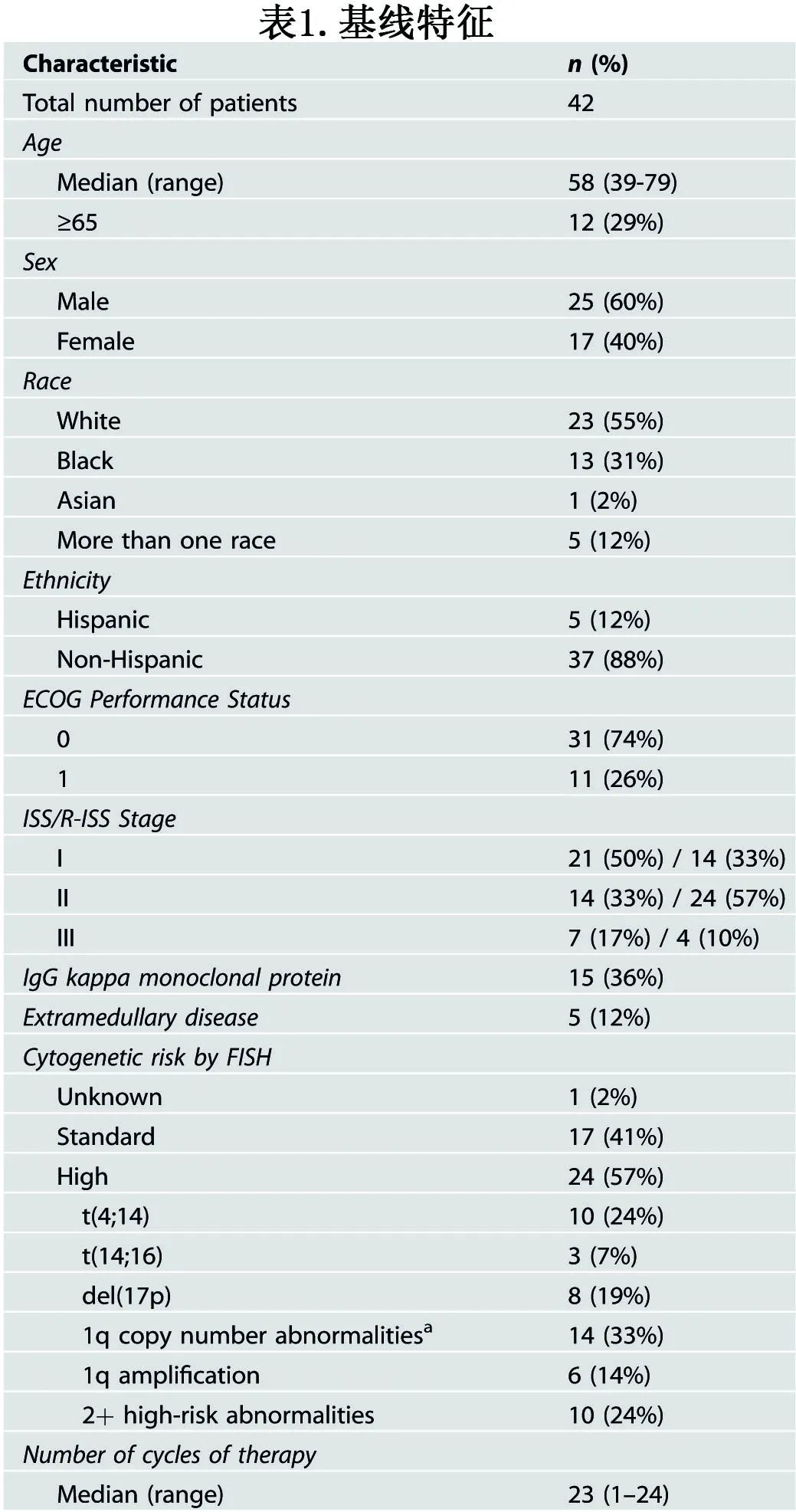
共入组42例患者,中位年龄为58岁,其中12例(29%)年龄≥65岁(表1)。根据IMWG标准,通过CD138+选择荧光原位杂交发现高危细胞遗传学异常(HRCA) 24例(57%),其中t(4;14) 10例(24%)、t(14;16) 3例(7%)、17p 缺失8例(19%)、1q拷贝数异常14例(6例[14%]为1q扩增);只有2例患者存在单独的1q获得而没有其他高危异常。10例(24%)患者存在≥2个HRCA。
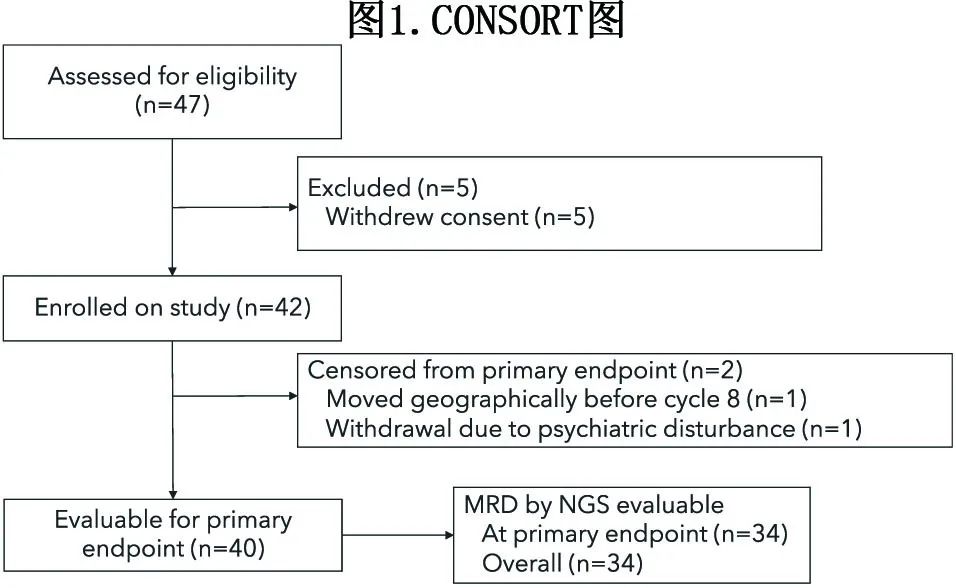
42例患者中40例(95%)在C8结束时进行了反应评估 (图1)。接受的中位周期数为23。
疗效
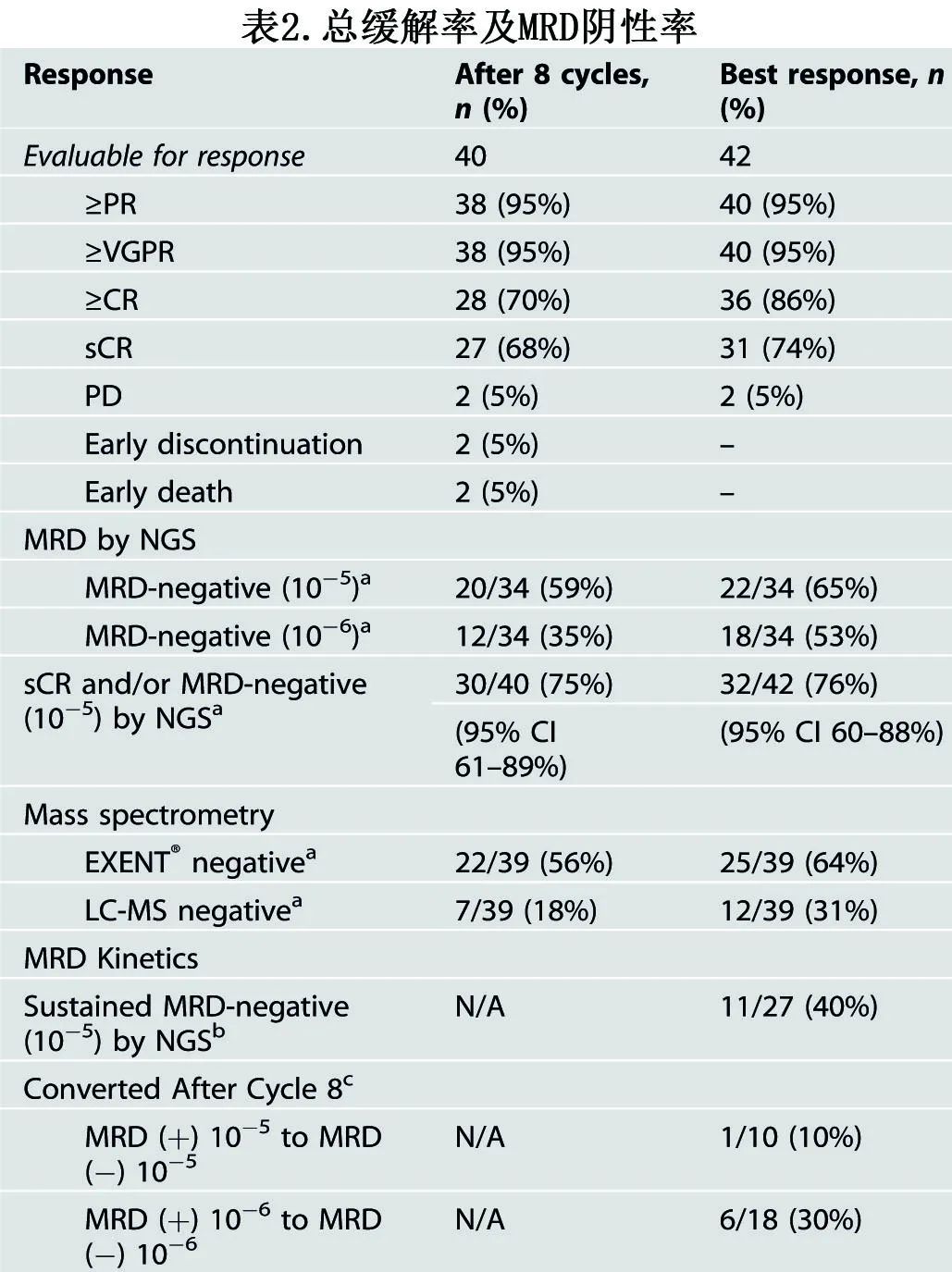
Dara-KRd治疗8个周期(n=40)后,sCR和/或MRD阴性(<10-5)的比率为30/40(75%),达到疗效的统计阈值(表2)。8个周期结束时的总缓解率为38/40(95%),其中27(68%)例达到sCR, 28(70%)例达到≥CR,38(95%)例达到≥VGPR。2例(5%)患者为原发难治性疾病;一例患者有两个HRCA,另一例患者的细胞遗传学样本不足,但诊断时循环浆细胞15%,不符合先前建立的浆细胞白血病标准(浆细胞≥20%)。在ITT人群(n=42)中,sCR作为最佳缓解的比例为31/42(74%),≥CR率为36/42(86%)。sCR和/或MRD阴性(10-5)的最佳缓解率为32/42(76%)。
患者分布
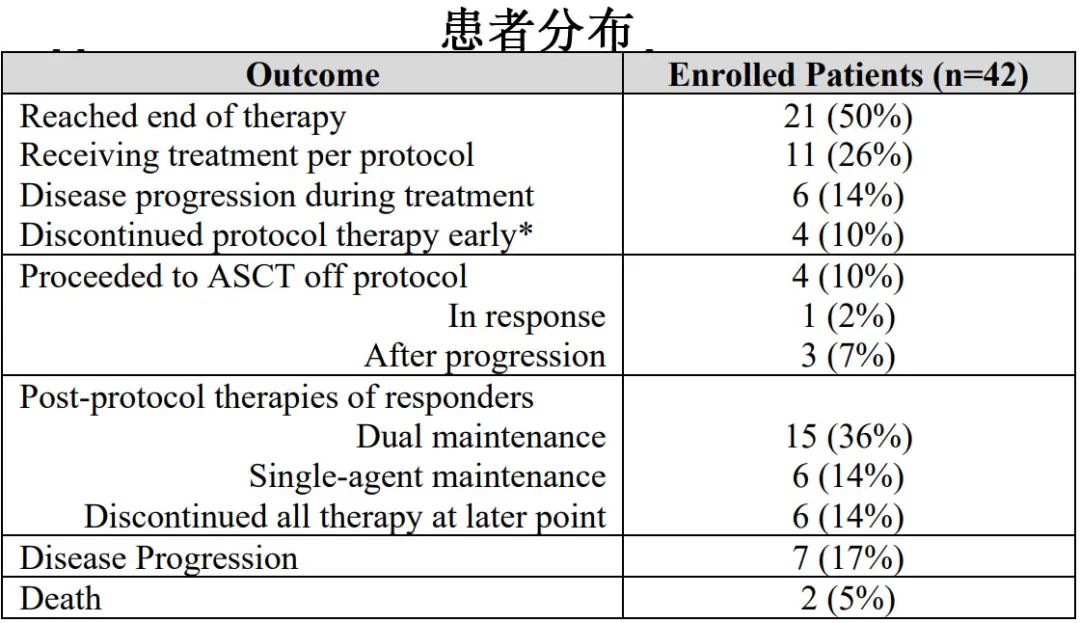
37例(88%)患者进行了干细胞采集,所有患者均使用G-CSF和普乐沙福,中位收集时间为2天,中位产量为8.26 × 106 CD34+细胞/kg。
NGS评估的MRD
34例(81%)患者进行了NGS MR D克隆型跟踪。通过MRD,20例(59%)患者在10-5阈值时达到MRD阴性,12例(35%)患者在C8结束时达到10-6阈值阴性(表2)。随着时间的推移,治疗达到C8的患者的反应逐渐加深(表2):10-5和10-6阈值下,分别有1/10(10%)和6/18(33%)的患者从C8时的MRD阳性后续转化为MRD阴性。10-5和10-6阈值下,任何时间点的MRD阴性率分别为22/34(65%)和18/34(53%)。在C8后MRD可评估的33例患者中,6例有一次MRD<10-5结果且后续随访时间不足1年,而其余27例患者中有11例(41%)持续10-5 MRD阴性(连续两次MRD阴性结果间隔≥1年)。
质谱分析
39例(93%)患者鉴定出可追踪的单克隆轻链,3例患者没有基线样本。在相同的39例可评估C8常规反应的患者中,22/39(56%)在C8结束时为EXENT阴性,25/39(64%)的最佳缓解为EXENT阴性。通过LC-MS,7/39(18%)为C8结束时LC-MS阴性,12/39(31%)的最佳缓解为LC-MS阴性 (表2;图2)。

C8时32个配对的EXENT和NGS(10-5)样本的一致性为75% (Cohen’s kappa 0.48),此外3例为NGS(+)/EXENT(−),5例为NGS(−)/EXENT(+)(图3)。在C8时配对的EXENT和NGS(10-6)样本中,一致性为69% (Cohen’s kappa 0.39),此外8例为NGS(+)/EXENT(−),只有2例为NGS(−)/EXENT (+)。在C24结束时,EXENT/NGS(10-5)和EXENT/NGS(10-6)的一致性均增加至84%。
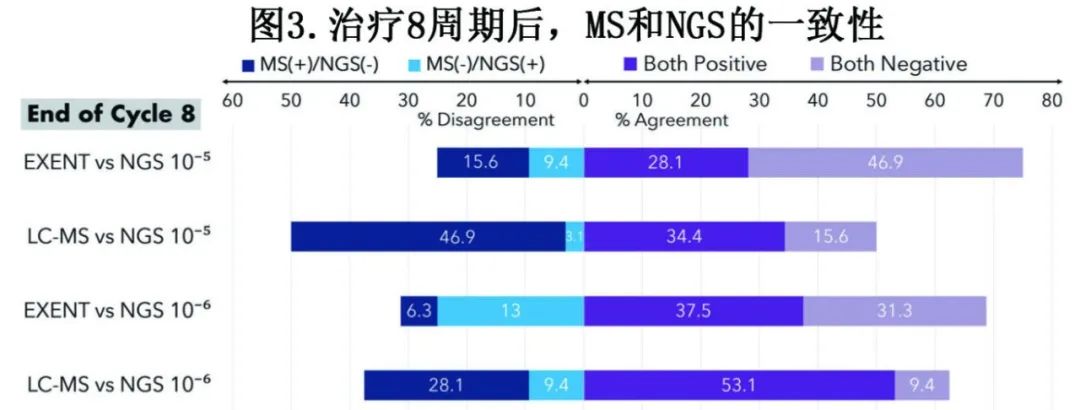
LC-MS和NGS在两个阈值上的一致性均较低。在C8时,32对LC-MS和NGS(10-5)样品之间有50%的一致性(Cohen’s kappa 0.14),其中大部分不一致性(15/16,94%)是由于NGS(−)/LC-MS(+)病例(图3)。在C8时,LC-MS和NGS(10-6)样品之间有63%的一致性(Cohen’s kappa 0.11,),其中9例为NGS(−)/LC-MS(+)、3例为NGS(+)/ LC-MS(−)。C24结束时,在10-5和10-6阈值下,分别有7/8(88%)和5/6(83%)的不一致病例为LC-MS (+)/NGS(−)。
无进展生存期和总生存期
中位随访27个月,有7例进展事件和2例死亡(均因进展)。3年PFS为85%,3年OS为95% (图4);PFS方面,标危患者为100%,1个HRCA的患者为92%,2+个HRCA的患者为60%。
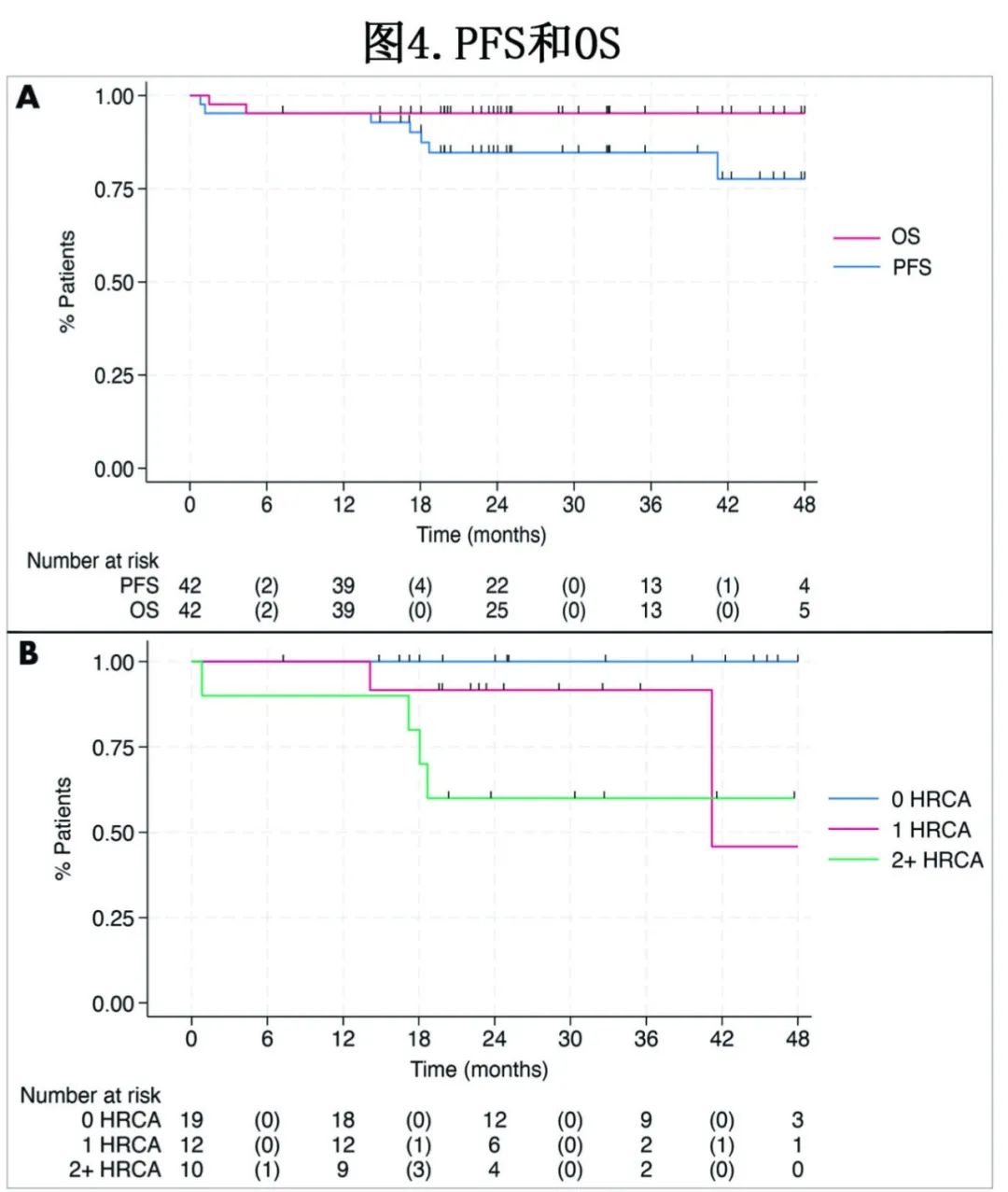
在10-5和10-6阈值下,C8 MRD与PFS均无关,C8时EXENT阴性为最佳缓解与改善相关,LC–MS阴性患者均未进展。
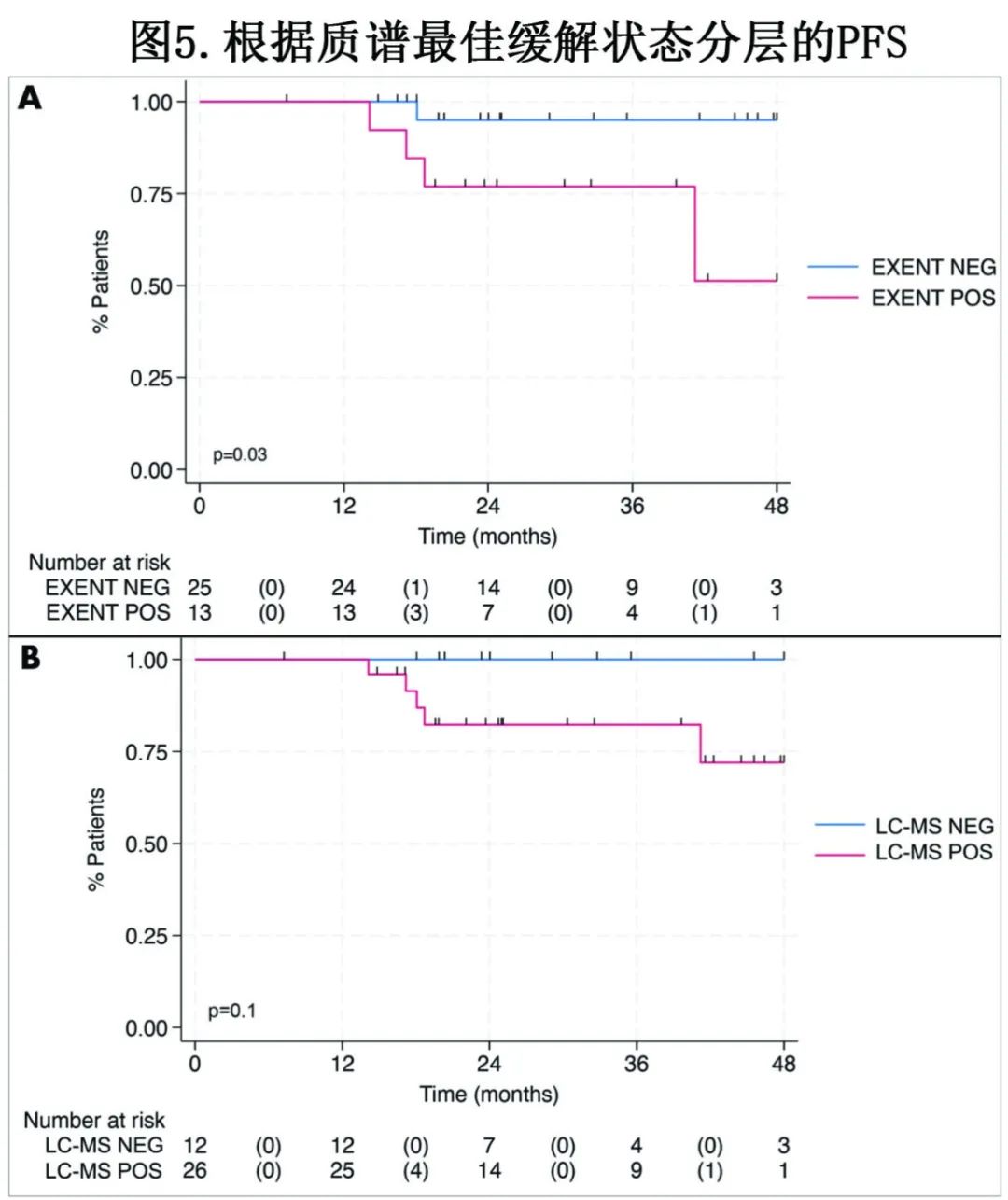
安全性和耐受性
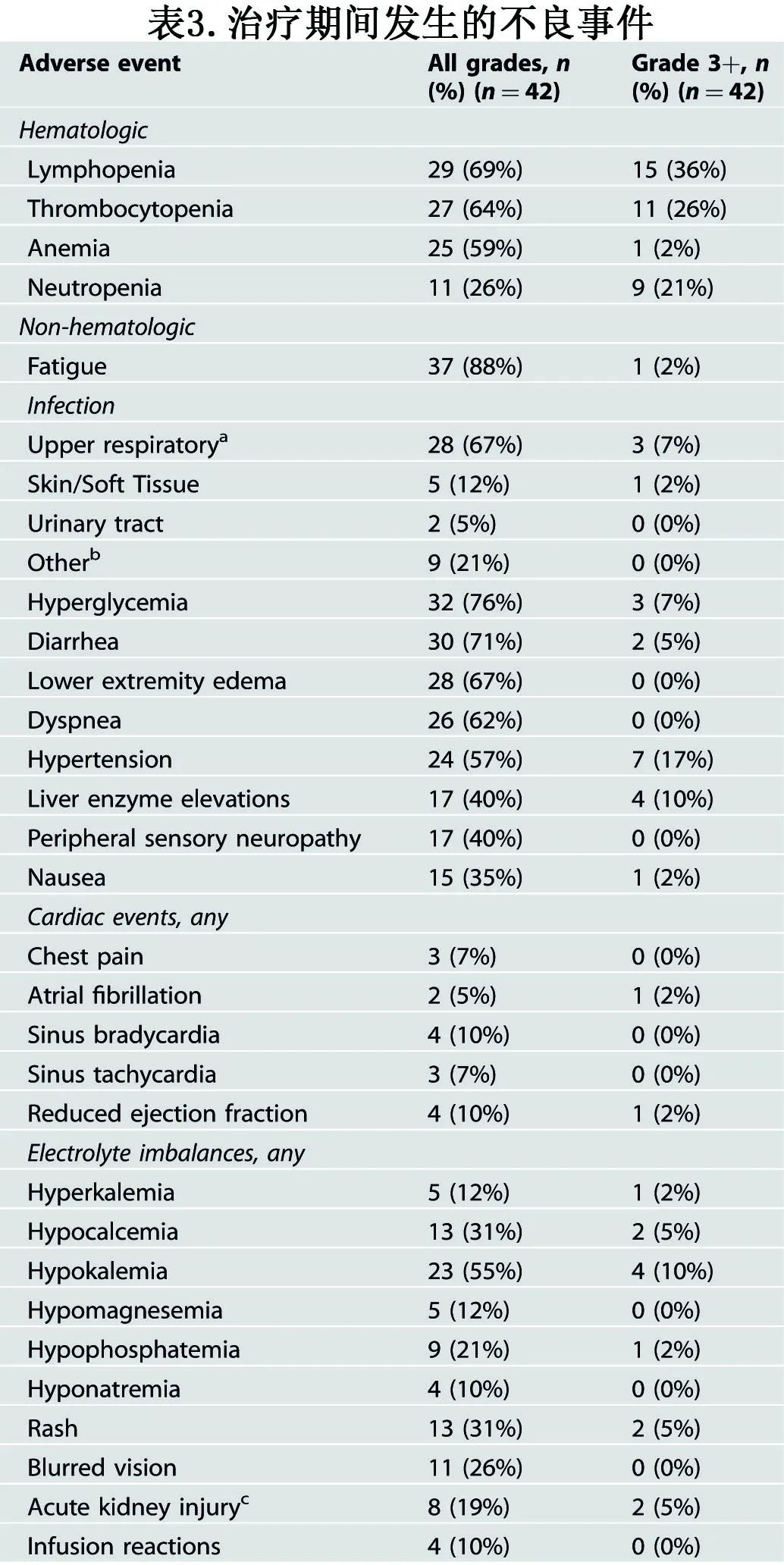
血液学不良事件(表3)包括中性粒细胞减少症(所有级别26%,G3+ 21%)、贫血(所有级别59%, G3+ 2%)和血小板减少症(所有级别64%,G3+ 26%)。最常见的非血液学不良事件为高血糖(所有级别76%,G3+ 7%)、腹泻(所有级别71%,G3+ 5%)、高血压(所有级别57%,G3+ 17%)和神经病变(所有级别40%,G3+ 0%)。上呼吸道感染28例(67%),G3+感染事件共3例(7%)。有一例血栓性微血管病变导致卡非佐米停药。G3房颤和心力衰竭各1例,均缓解。没有患者因毒性而停止治疗或死亡。
总结
研究纳入42例患者,其中40例可作为主要终点进行评估。C8后sCR和/或MRD <10-5的比率为30/40(75%),达到疗效的统计阈值。最佳缓解为MRD <10-5的比例为59%(其他四药方案的MRD阴性率:Dara-VRd 22%、Dara-VMP 28%、Dara-VTd 35%、Dara-KRd 38%、Isa-VRd 50%、Isa-KRd 45-54%、Elo-KRd 53%)。10-6 MRD阴性率随着C8以后的进一步治疗而提高。EXENT和NGS之间的一致性较高,且随着时间的推移而增加;LC-MS和NGS的一致性较低。3年PFS为85%,3年OS为95%;3年PFS是已报道的数据中最高的之一,例如Dara-VRd序贯ASCT的3年PFS为90%(虽然不能直接对比)。上呼吸道感染发生率为67%(3-4级为7%)。没有与治疗相关的死亡。
该研究首次证实扩展的24周期一线Dara-KRd诱导治疗不伴ASCT可获得高比率sCR和/或MRD阴性;C8以后MRD阴性率和深度均有改善。此外,2+个HRCA的NDMM患者仍存在挑战。
参考文献
Derman, B.A., Cooperrider, J., Rosenblatt, J. et al. Final analysis of a phase II trial of daratumumab, carfilzomib, lenalidomide, and dexamethasone in newly diagnosed multiple myeloma without transplant. Blood Cancer J. 14, 87 (2024). https://doi.org/10.1038/s41408-024-01045-3
作者:聊聊血液
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#多发性骨髓瘤# #来那度胺# #地塞米松# #Dara-KRd#
8