结肠癌术后11年肝转移,64岁女子再战恶性肿瘤:依从性较差,治疗不走“寻常路”?
2024-07-10 肿瘤医学论坛 肿瘤医学论坛
介绍一位64岁晚期结肠癌肝转移患者的治疗过程,包括多轮治疗、MDT讨论及相关问题探讨,强调MDT参与和个体化治疗的重要性。
01 病例介绍
患者基本情况
患者:女,64岁,已婚
初诊时间:2021-10-24
主诉:腹痛半月余,发现肝占位1天
既往史:2010年在郴州市第四人民医院行结肠癌根治术,术后予以化疗4周期(术后分期及方案不详),2011年诊断为2型糖尿病,一直口服阿卡波糖治疗,血糖控制可。
2021-10-23(郴州市第四人民医院)胸腹部CT:①既往结肠癌术后改变,结肠肠壁稍增厚,请结合肠镜。②肝内多发转移瘤(较大者70mm*54mm)。③双肺实质未见明显转移征象。
查体:PS 评分1分,身高158 cm,体重 54 kg ,体表面积1.53 ㎡ 全身浅表淋巴结未扪及肿大,腹部平软,剑突下压痛,无反跳痛,肝脾肋下未及,移动性浊音阴性。
2021-10-28 (湖南省郴州市第一人民医院)肠镜活检:(结肠距肛门 36cm,活检)高-中分化腺癌。
辅助检查:
血液学:CEA 27.59ng/ml,CA-199 35.77u/ml;
影像学:头颅增强MRI、ECT、腹腔其余脏器增强CT均未见明显肿瘤征象。
初次诊断:左半结肠恶性肿瘤(IV期) 肝继发恶性肿瘤
第一次 MDT 讨论
放射科:患者目前吻合口未见异常,且距离第一次结肠癌手术有11年,考虑第二原位癌可能;肝脏多发转移较多、较大,且分散在在不同肝叶,部分位置较深且临近血管,暂无局部消融治疗指征。
胃肠肿瘤外科:患者目前结肠癌并肝脏多发转移,结合放射科阅片,有潜在手术机会,建议先行转化治疗,后续根据治疗疗效再次评估。
放疗中心:患者目前无放疗指征。
胃肠肿瘤内科:晚期结肠癌,外科目前暂无手术指征,建议完善肠癌相关基因检测、MSI状态,根据检测结果选择治疗方案。
基因检查:KRAS、NRAS、BRAF 野生型,MSS
一线治疗:2021-11-06、2021-11-20、2021-12-09、2021-12-23予以西妥昔单抗760mg d1 + mFOLFOX6方案(奥沙利铂120mg*d1+亚叶酸钙600mg*d1+氟尿嘧啶600mg*d1+氟尿嘧啶3650mg civ*48h,q14d)化疗4周期。
4周期后2022-01-06复查CT:“结肠Ca”术后复查,肝多发转移瘤(较大约36mmx27mm)。PR
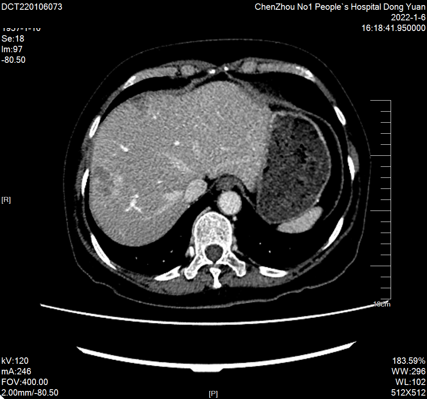
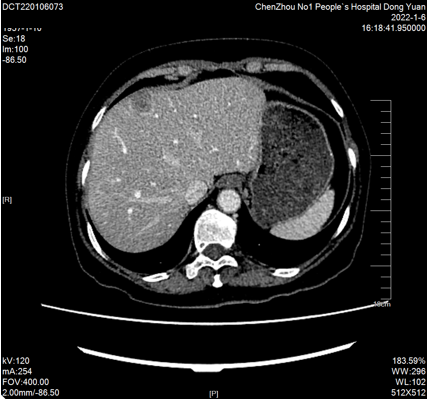
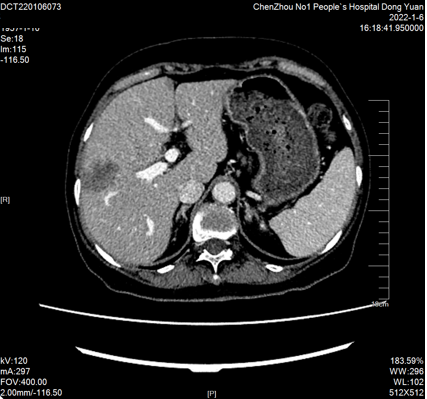
2022-01-07至2022-05-12继续予以西妥昔单抗760mg d1 + mFOLFOX6方案(奥沙利铂120mg*d1+亚叶酸钙600mg*d1+氟尿嘧啶600mg*d1+氟尿嘧啶3650mg civ*48h,q14d)化疗8周期。
8周期后2022-03-15复查CT:“结肠Ca”术后复查,与2022-01-06CT比较:肝多发转移瘤部分较前缩小长径约(33mm),余胸腹部情况较前变化不大。PR
12周期后2022-07-04复查CT:“结肠Ca”术后复查,与2022-03-15CT比较:1、肝内多发转移瘤,部分较前稍缩小。2、双肾小囊性灶,右肾小结石。3、双肺小结节,建议随诊复查。PR
2022-07-04 肝脏MRI:“肝转移瘤”治疗后复查,与前片(2022-04-20)比较:1、肝多发转移瘤较前缩小(大者约23*21mm)。2、腹腔少量积液、脂肪肝同前。
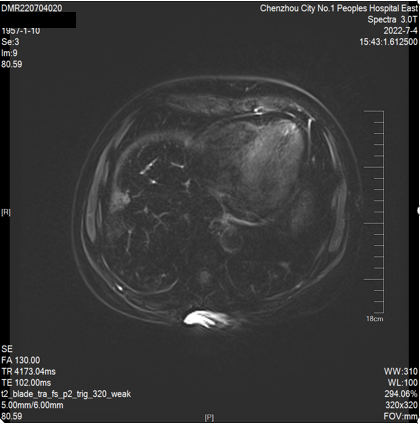
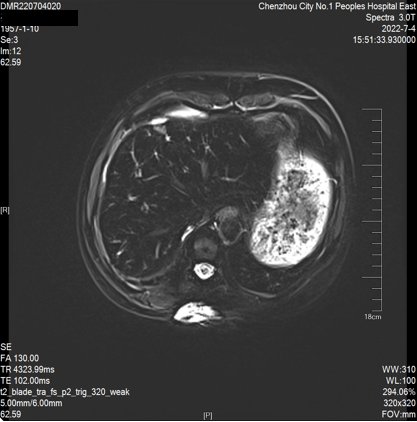
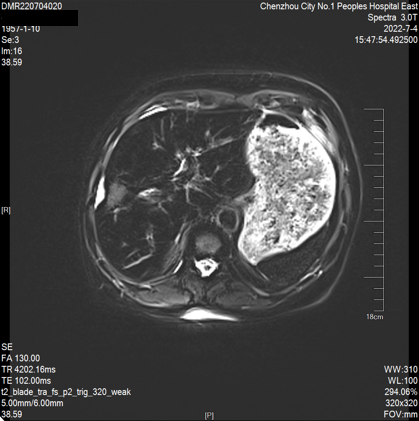
第二次 MDT 讨论
放射科:患者目前肝脏多发转移较前明显缩小,降结肠肿瘤目前CT显示不清晰。
胃肠肿瘤外科:患者目前结肠癌并肝脏多发转移,肝脏MRI目前可见5个转移瘤,其中3个可行手术,另外2个可行微波消融。同时行肠镜再次评估病情。
放疗中心:患者目前无放疗指征。
胃肠肿瘤内科:晚期结肠癌,靶向联合化疗12周期后,目前疗效评估PR,现有肝脏转移瘤局部治疗指征,肝脏局部治疗后可考虑卡培他滨维持治疗。
患者拒绝行肝脏局部治疗。
2022-06-09开始予以卡培他滨1.5g po bid q21d维持治疗,期间患者出现手足麻木,感觉异常,总体能耐受。
维持治疗期间患者每三个月复查CT,结果提示病情稳定,肿瘤标志物正常,疗效评估SD。
2023-02-06 CT:“结肠Ca”术后复查,与2022-11-17CT比较:1、肝内低密度影较前增多、增大(较大者截面约42mm×52mm),余腹部情况较前大致相仿。2、双肺微结节大致同前。CEA 9.32ng/ml,CA199 32.51 u/ml。
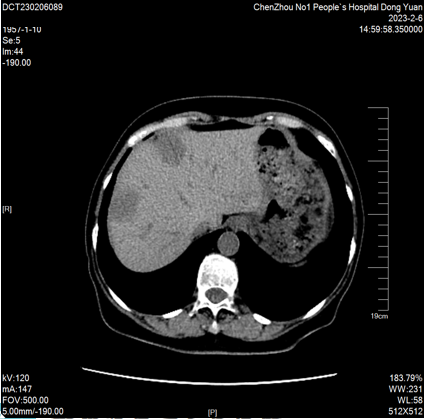
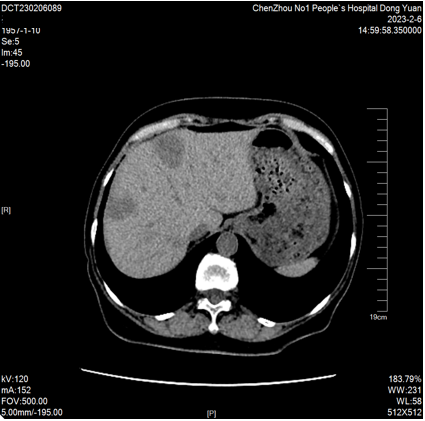
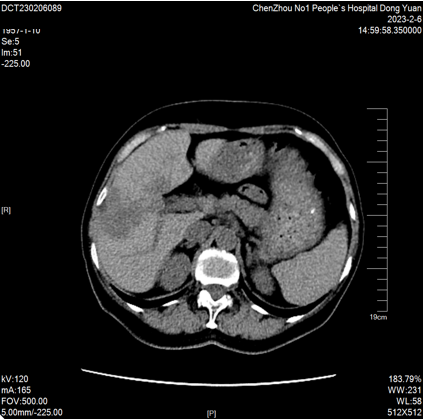
2023-02-06 肝脏MRI:对比2022-11-18MRI片,肝多发转移瘤较前增多、增大(大者长径约53mm)。双肾小囊肿。胆囊显示不清。
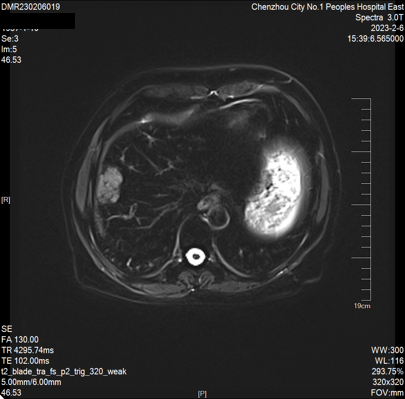
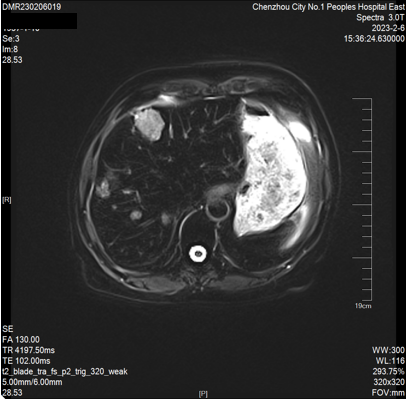
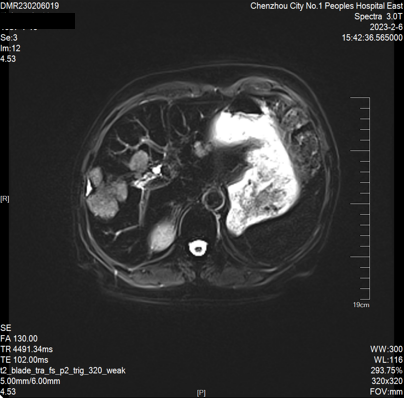
因患者原方案治疗有效,且卡培他滨维持治疗超过6个月。
建议患者原方案继续治疗或更换标准二线治疗方案,患者拒绝静脉化疗。
二线治疗:
2023-02-08予以贝伐珠单抗250mg d1+ TAS-102 50mg po bid d1-5 q2w。
治疗期间患者出现I°骨髓抑制,总体能耐受,未见明显不良反应。
2023-05-31复查CT:1、肝内低密度影较前缩小(较大者截面约40mm×24mm)。2、双肾多发小囊肿,右肾小结石。3、双肺微结节大致同前。主动脉钙化 。
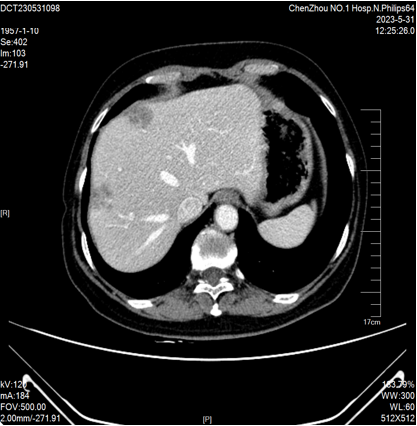
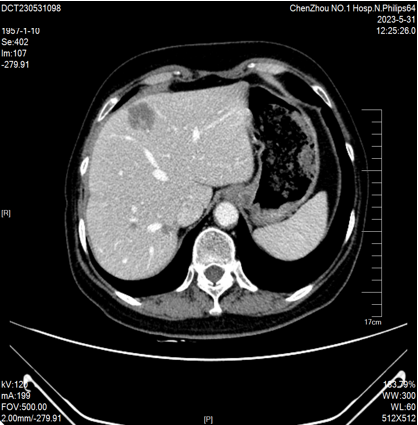
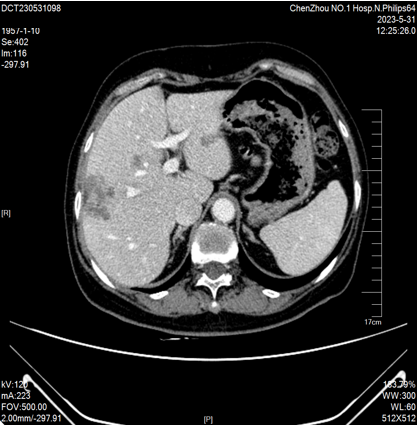
2023-11-17 CT:“结肠Ca”术后复查,对比2023-05-31日CT检查,现片示:肝内多发病灶、部分较前稍增大(较大者截面约41mm×30mm)。
后患者定期复查CT提示病情稳定,总体疗效评估PR。
2024-4-16 CT:肝多发转移瘤部分较前增多、增大(70mm*50mm)。
CEA 24.35ng/ml,CA199 654.77u/ml
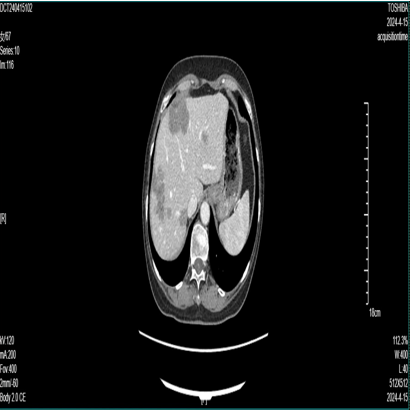
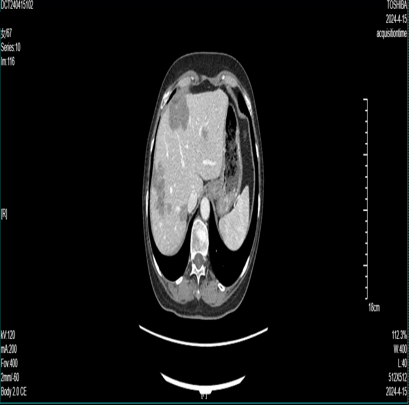
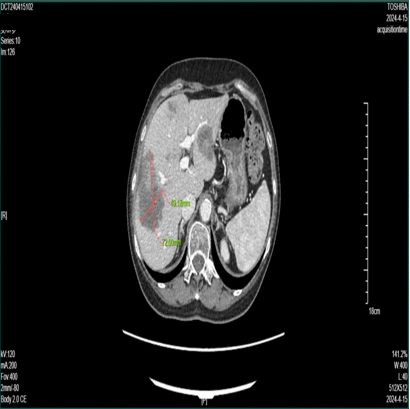
第三次 MDT 讨论
放射科:患者目前肝脏多发转移较前明显增大,考虑病情进展。
胃肠肿瘤外科:患者目前结肠癌并肝脏多发转移,建议全身治疗为主,肝脏局部可考虑介入治疗。
放疗中心:患者目前无放疗指征。
胃肠肿瘤内科:晚期结肠癌患者,现出现病情进展,可考虑靶向(西妥昔单抗/贝伐珠单抗)联合化疗(FOLFIRI/mFOLFOX6)方案,但是患者2024年2月因反复胸闷不适,在我院诊断为冠心病,心功能2级,故氟尿嘧啶类可更换成雷替曲塞。
三线治疗:
患者因经济原因选择贝伐珠单抗。
2023-04-17予以贝伐珠单抗400mg d1+ 伊立替康280mg d1 +雷替曲塞4mg q3w。
治疗期间患者出现II级腹泻,总体能耐受。
2024年5月1日患者中山大学附属肿瘤医院就诊邱教授,建议贝伐珠单抗联合伊立替康治疗。
2024-05-14予以贝伐珠单抗400mg d1+伊立替康400mg 姑息性化疗。
2024-05-23血常规:白细胞计数 1.14*10^9/L,中性粒细胞计数 0.26*10^9/L,血红蛋白量 50g/L,血小板计数 25*10^9/L;患者化疗后出现IV°骨髓抑制,白细胞减少,中性粒细胞缺乏,血小板减少,重度贫血,同时出现2级腹痛腹泻,予以下病重通知,同时予以升白、升血小板、输血小板,输红细胞及对症支持治疗。
2024-05-27复查血常规:白细胞计数 13.14*10^9/L,中性粒细胞计数 10.57*10^9/L,血红蛋白量 81g/L,血小板计数 154*10^9/L。
肿瘤标志物变化
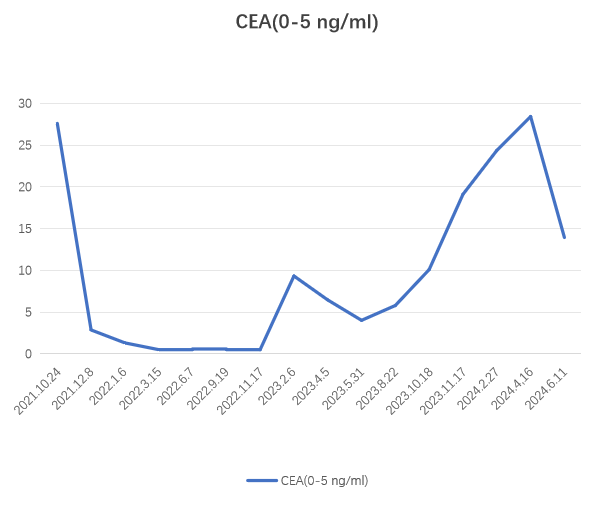
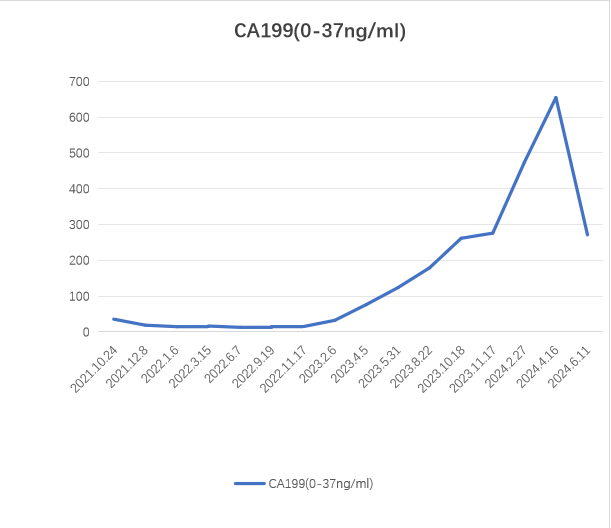
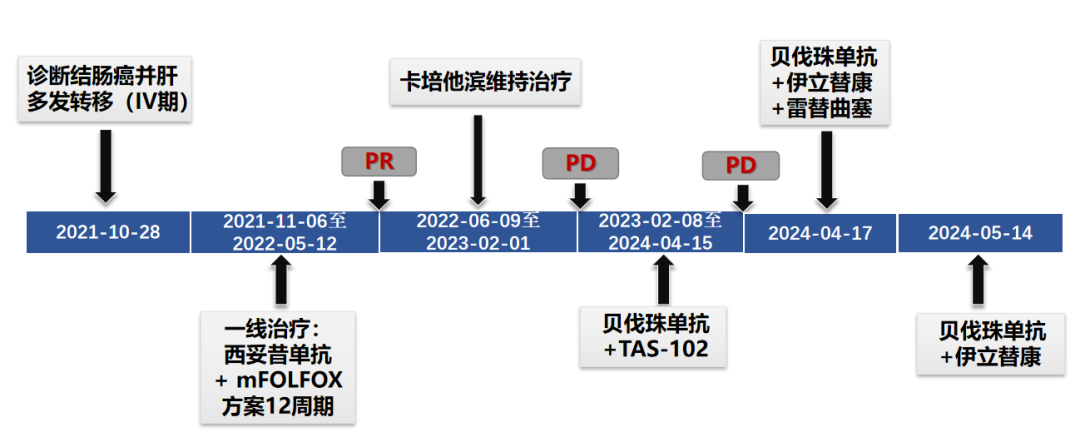
治疗过程回顾
02 病例讨论
问题 1:肠癌转化治疗的最佳手术时机是什么?
中南大学湘雅三医院-肿瘤科-彭彬:李教授分享了一个非常精彩的病例。通过多次组织MDT讨论,从治疗结果来看,患者生存时间已接近三年,整体治疗还是比较成功的。患者为初始不可切除的转移性结直肠癌,存在一定的转化治疗可能性。在一线治疗中,患者接受了西妥昔单抗联合mFOLFOX方案,每4个疗程进行一次评估。从评估结果来看,第一次评估后,肿瘤缩小程度最为显著。而在第8个疗程后的评估中,肿瘤从36mm减小到33mm,缩小程度不那么明显了。
到了第12个疗程后,患者进行了再次评估,并在此后组织了MDT,邀请外科专家评估手术切除的可能性,当时认为有手术切除的可能。但我有一个问题:对于潜在可切除的患者,转化治疗在何种程度进行手术干预最为适宜?针对这个患者,在第四个疗程时进行干预是不是最合适的?我们知道,随着化疗疗程的增加,可能会增加药物性肝脏毒性,这是否会在后续的肝脏切除手术中诱发肝功能衰竭等并发症?
中南大学湘雅三医院-肿瘤科-王琦:关于潜在可切除患者的转化治疗,我们应当在何时进行手术或介入以取得最佳疗效?这需要在MDT的指导下进行决策。对于结直肠癌肝转移的患者,原发灶的切除对于胃肠外科医生而言通常是较为常规的手术。然而,影响整体治疗效果及手术切除可能性的关键因素是肝脏转移灶的情况。因此,我们还需要听取肝脏外科医生的专业意见。
如果潜在可切除患者在经过半年以上的转化治疗后,原发灶和转移灶均无法实现R0切除,则可以认为转化治疗失败。在这种情况下,建议患者转入维持治疗阶段。
问题 2:在肠癌治疗中,如何根据患者情况合理选择药物剂量和治疗方案?
中南大学湘雅三医院-肿瘤科-王琦:对于这个病例,我有一个问题,我相信后续讨论的专家们可能也会有同样的疑问。为什么在三线治疗中将贝伐珠单抗+伊立替康+雷替曲塞的方案更改了,虽然有提到邱教授给予了这个方案,但我注意到伊立替康用了400毫克,我好奇这个剂量调整的依据是什么?这么高的剂量在这个患者身上就体现出来了特别严重的骨髓抑制。
郴州市第一人民医院-肿瘤内科-李爱娟:患者的儿子在寻求治疗建议时表现出了极高的积极性,患者在中山大学附属肿瘤医院就诊邱教授时,教授建议贝伐珠单抗联合伊立替康治疗。伊立替康单药用的剂量是300至350毫克每平米,但在联合使用雷替曲塞的情况下,剂量会相应降低,用了 280 毫克每平米。基于上级医生的建议,我认为如果伊立替康的剂量继续保持280毫克每平方米,可能不足以达到预期的治疗效果。
湘潭市中心医院-肿瘤二科-胡十齐:这位患者在接受转化治疗的过程中,发现可能无法达到根治性治疗效果,于是继续进行维持性的姑息治疗。在转化治疗过程中,我们也进行了一些探索性治疗,特别是对于较年轻、一般情况良好的患者,可能会采取更为强烈的三药联合或联合靶向治疗。通常在3到6个月后,如果疗效显著,部分肠道切除可以作为避免未来肠梗阻发生或减瘤的有效手段。
对于肝脏肿瘤,我们可能更多地采用射频消融联合肝动脉灌注化疗(HAIC)或经动脉化疗栓塞(TACE)等局部治疗方法。HAIC是一种非常优秀的介入治疗方法,通过局部使用化疗药物,减少了全身用药剂量,同时可以达到对肝脏缩瘤的显著效果。
总的来说,我们采用全程治疗方法,尽可能地利用可用的靶向化疗。目前,我们常规会在治疗初期检测HER2和错配修复(MMR)蛋白以及NTRK等。我们知道,MSI-H或dMMR患者对免疫治疗反应良好。邓艳红教授在MSI-H患者研究中发现,免疫治疗PD-1单抗联合COX-2抑制剂塞来昔布在晚期患者中甚至可以达到接近90%的完全缓解率,这是非常令人鼓舞的。因此,我们不能忽视这部分患者。
在HER2方面,我们发现在二线或三线治疗中,HER2高表达的患者使用维迪西妥单抗等ADC类药物也能取得良好的疗效。KRAS G12C、NTRK等靶点也是我们精准治疗的选择。这位患者已经取得了非常好的生存效果。我们期待在未来,局部治疗手段能有更多的选择和应用。
娄底市中心医院-放疗中心-王正安:该病例的进展相对缓慢。十多年前,患者就进行了结肠癌根治术,2021年肿瘤复发并出现肝转移。随后给予了规范的一线治疗。在二线治疗中,采用贝伐珠单抗联合TAS-102的治疗方案,患者取得了12个月的临床缓解。作为临床医生,我们更期望晚期肿瘤患者能够拥有比较高质量的生存,而不是在痛苦中度过每一天。
在经过一段时间的生存后,患者病情再次进展。李教授采用了一个典型的治疗方案,即伊立替康联合雷替曲塞,患者再次得到了很好的缓解。我们期待在这种有序的治疗下,患者能够拥有更长的生存期。
永州市中心医院-肿瘤科-唐华燕:针对这个病例,在首次MDT讨论后采用西妥昔单抗联合mFOLFOX方案治疗了12个周期。如果在这个阶段进行局部治疗,可能会进一步延长生存期,当时进行局部治疗是有意义的。但患者可能基于其他原因拒绝了局部治疗,这确实令人遗憾。考虑到第一次MDT患者有5个病灶,其中3个适合手术治疗,2个适合消融。然而,无论是消融还是手术,对患者来说都是有创性的。目前,我们也可以与患者讨论立体定向放疗,这是一种无创性治疗,患者可能更容易接受。
在完成12个周期治疗后用卡培他滨维持维持治疗,患者的疗效是比较好的,但由于可能没有定期复查,当患者再次就诊时,肝脏的最大病灶已经长到5公分,但距离上次西妥昔单抗治疗已经超过半年。在这种情况下,我认为西妥昔单抗仍有再次挑战的可能,因为患者的原发病灶位于左半结肠。我们知道,在结直肠癌中,尤其是IV期患者,治疗策略应根据分子分型和部位来选择。对于这位患者,原发病灶位于左半结肠,再次使用西妥昔单抗可能会带来益处。
正如王琦教授所提到的,临床治疗中可能还会根据个体化的选择来调整方案。目前,TAS-102在一线、二线、三线的临床研究中都有数据支持。如果再次使用西妥昔单抗联合治疗,其OS或PFS可能不会逊色于贝伐珠单抗联合TAS-102作为二线维持治疗。
中南大学湘雅三医院-肿瘤科-王琦:对于这位患者未能及时接受局部治疗,我们感到非常遗憾。实际上,在适当的时机进行局部治疗的介入,无论是手术、射频消融、TACE还是放疗,确实能够显著改善晚期肠癌肝转移患者的状况,特别是在达到NED状态后,可能会进一步延长患者的生存期并提高疗效。
在我的临床实践工作中,我发现对于肝转移瘤,外科医生对射频消融技术的认可度通常高于SBRT放疗。然而,我们放疗领域的专业人士都清楚,SBRT由于其物理特性,损伤会比射频消融好。实际上,面对这种拒绝手术的患者,我会综合考虑SBRT放疗和射频消融两种方法。所以,我在此也呼吁一下,在发现肝转移瘤的患者中,SBRT放疗也是一种非常有效的治疗手段,值得我们更多的关注和应用。
问题 3:如何结合个体化治疗和临床研究来优化晚期结肠癌的治疗策略?
中南大学湘雅三医院-肿瘤科-彭彬:根据李教授的治疗策略,在二线和三线治疗中似乎将指南推荐的方案顺序进行了调整。按照常规,二线治疗通常采用伊立替康联合贝伐珠单抗或氟尿嘧啶类药物。然而,在这位患者身上,李教授在二线治疗中使用了贝伐珠单抗联合TAS-102。根据我们的临床经验,随着治疗线的增加,患者的整体耐受性可能会降低。因此,如果将毒性更强的伊立替康放在二线治疗,而将耐受性较好的TAS-102放在三线治疗,患者的结果会不会更好一些?另外,也想问一下在座各位专家,把肠癌二、三线方案调换过来有没有相关的临床研究报道,对总体生存有没有影响?
中南大学湘雅三医院-肿瘤科-王琦:我们观察到这位患者的治疗过程中有一个明显的特点,即在二线治疗中采用了原本属于三线的治疗方案。李教授在PPT中也提到了,一些指南、研究数据支持了这种治疗方式。具体来说,患者在二线治疗中使用了TAS-102联合贝伐珠单抗,其PFS超过了一年,与三线治疗中5个多月的PFS相比,有了显著提升。
这表明,将有效的治疗方案提前至前线治疗,在患者一般状况较好时使用,可能会带来更好的治疗效果。当然这个不做大规模推广,但临床工作本身充满变数,病人的情况和需求也各不相同。只要治疗符合一定的适应症,对于某些患者,进行小范围的或个体化的治疗方案是可以参考的。不过,这种个体化治疗策略还需要我们进一步获取更充分的循证医学证据。我们期待能够开展更多关于这一方面的Ⅲ线治疗临床研究。
问题 4:对于这位患者的下一步治疗,有什么建议?
郴州市第一人民医院-放疗病区-刘欢:李教授刚刚分享了一个晚期结直肠癌的病例,治疗过程非常成功,患者至今已存活近三年。最初,患者被诊断为结直肠癌肝转移,接受了西妥昔单抗联合mFOLFOX化疗作为一线治疗,并取得了良好疗效。在整个治疗过程中,关键决策均有MDT的参与,这是治疗成功的重要因素。然而,患者依从性不佳,特别是在一线化疗结束后,如果能够及时进行局部介入治疗,可能会对病情的最终结果产生积极影响,因为后续的进展主要集中在肝脏。
患者在一线化疗后进入维持治疗阶段,但随后病情进展,且患者拒绝接受静脉化疗。使用TAS-102联合贝伐珠单抗的治疗方案取得了良好效果。值得注意的是,在2024年的CSCO指南中,TAS-102联合贝伐珠单抗已从二线治疗推荐上升为一线治疗的一级推荐,为类似患者提供了更好的治疗选择。然而,在经过TAS-102联合贝伐珠单抗治疗后,患者病情再次进展,并接受了伊立替康化疗,出现了重度骨髓抑制的问题。可能由于化疗的毒副反应,患者再次拒绝静脉化疗。在后续治疗中,可以考虑使用三线治疗方案,如呋喹替尼、瑞戈菲尼或呋喹替尼联合TAS-102等。
永州市中心医院-肿瘤科-唐华燕:在三线治疗中,除了TAS-102,我们还有呋喹替尼、瑞戈菲尼以及TKI类药物联合免疫治疗的选择。我们知道,结直肠癌通常被视为“冷肿瘤”,TKI类药物联合免疫治疗可能有助于将“冷肿瘤”转化为“热肿瘤”,对患者来说是一个可选的治疗方案。此外,基于基因检测结果,患者还可能从西达本胺去化疗的联合治疗中受益。
03 MDT小结
该病例是一位64岁的晚期结直肠癌患者,在2010年行结肠癌根治术,2021年复发肝转移。当时,经过MDT讨论,患者被诊断为初治潜在可切除,分子分型显示为RAS和BRAF基因野生型。通过西妥昔单抗联合双药化疗的转化治疗,患者达到了显著的疗效。值得称赞的是,该病例在关键治疗节点均有MDT团队的参与。
该病例是一位64岁的晚期结直肠癌患者,在2010年行结肠癌根治术,2021年复发肝转移。当时,经过MDT讨论,患者被诊断为初治潜在可切除,分子分型显示为RAS和BRAF基因野生型。通过西妥昔单抗联合双药化疗的转化治疗,患者达到了显著的疗效。值得称赞的是,该病例在关键治疗节点均有MDT团队的参与。
然而,在转化治疗成功后,局部治疗未能及时跟上,导致患者在卡培他滨维持治疗6个月后出现了病情进展。在二线治疗中,由于患者个人原因,治疗方案偏离了常规,采用了TAS-102联合贝伐珠单抗。经过仔细分析,无论是转化治疗阶段的西妥昔单抗联合双药化疗,还是二线治疗的贝伐珠单抗联合TAS-102,患者的PFS均超过了一年。与多个临床研究的中位PFS相比,这位患者的PFS均超过了中位数,表明其对药物的反应优于大部分患者。
这种对治疗的积极反应突显了个体化治疗策略的重要性,以及在关键治疗决策时MDT团队参与的必要性。
述评
湖南省肿瘤医院-消化泌尿内一科-刘振洋:首先,从病例角度来讲,我们应当尽可能参与MDT讨论。MDT的形式可以灵活多样,不一定需要多人围坐在会议桌前,配备电脑设备。实际上,通过电话咨询或召集几位专家进行快速讨论,也是一种高效的MDT模式。尽管医生工作繁忙,可能无法总是遵循标准的MDT模式,但仍需保持MDT的意识。
其次,尤其是内科医生,一定要重视局部治疗的重要性。我们观察到,在晚期结直肠癌的治疗中,系统性治疗延长患者生存时间通常是以月为单位计算的。但如果能够将患者转化为可以接受局部治疗的状态,延长的时间有时可以以年为单位计算。局部治疗不仅包括手术,还包括射频消融、立体定向放疗、粒子植入,甚至包括HAIC等治疗方式。在进行选择性、个体化治疗时,有些患者能够取得非常好的疗效。
第三,关于治疗的规范化问题,之前有专家提到了Ⅱ期临床研究或回顾性临床研究,这些研究结果是否可以应用于临床实践。实际上,临床治疗应以指南为模板,遵循规范化的指南。如果在临床实践中使用指南未推荐方案,那属于超适应症使用,理论上需要与患者沟通,并根据相关单位的规定,可能需要填写申请书等,走相应的程序。
实际上,结直肠癌治疗的药物选择相对有限。最好的办法不是反复应用某一药物进展后又使用另外的药物,而是在药物进展后参与临床研究,这是一种更好的方法。
此外,我想强调的是,许多医生存在一种倾向,即多用药而不愿意进行检查和检测,这实际上是错误的。我个人更倾向于多进行检查和检测,少用药。因为只有在进行了充分的检查和检测,掌握了治疗方向后,用药疗效才会更好。否则,使用了许多药物而没有疗效,反而增加了毒副反应。
作者:肿瘤医学论坛
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








学习了,谢谢分享
86
#结肠癌# #肝转移# #治疗过程#
108
完整详尽的病例,学习学习学习强国
87
一个特殊病例
91