T790M突变检测,实现EGFR TKI耐药患者的精准治疗
2017-08-09 佚名 肿瘤资讯
表皮生长因子受体(EGFR)突变是晚期非小细胞肺癌最重要的驱动基因之一。既往,已经有10项临床研究验证,EGFR TKI单药治疗是EGFR突变型晚期NSCLC患者的治疗首选。但非常遗憾的是,几乎所有接受EGFR TKI治疗的患者最终都将出现耐药。研究发现,EGFR第 20号外显子发生错义突变(即T790M突变)是主要的耐药机制,约占耐药患者的50%~62%。在克服耐药的探索中,开发出了一系列的三代
表皮生长因子受体(EGFR)突变是晚期非小细胞肺癌最重要的驱动基因之一。既往,已经有10项临床研究验证,EGFR TKI单药治疗是EGFR突变型晚期NSCLC患者的治疗首选。但非常遗憾的是,几乎所有接受EGFR TKI治疗的患者最终都将出现耐药。研究发现,EGFR第 20号外显子发生错义突变(即T790M突变)是主要的耐药机制,约占耐药患者的50%~62%。在克服耐药的探索中,开发出了一系列的三代EGFR-TKI,然而,最终只有奥希替尼拔得头筹,获批上市,这与其独特的药理学特征是密切相关的。奥希替尼可以高选择性地抑制EGFR敏感突变和T790M耐药突变,对野生型EGFR和IR/IGFR的亲和力很低。在AURA系列研究中,奥希替尼用于T790M耐药突变的患者表现出高效、低毒、对中枢神经系统转移有效的特征,成为T790M耐药突变的NSCLC患者治疗的“新高度、新标杆”。其中,AURA3研究深刻改变了临床实践,相比于化疗,奥希替尼组显着更优,中位 PFS达10.1个月。基于奥希替尼在中国人群的单臂II期临床研究AURA17的结果,2017年3月泰瑞沙(奥希替尼)获得中国国家食品药品监督管理总局(CFDA)审批在中国上市。开创了EGFR TKI耐药后T790M突变阳性患者的精准治疗新时代。随着泰瑞沙的上市,如何敏感、准确地检测T790M突变成为临床关注的热点。本文,我们将梳理既往的研究数据,从EGFR TKI治疗前后T790M的突变率对比和EGFR T790M突变阳性和阴性患者接受三代EGFR TKI治疗疗效的对比两个方面,系统性解读为什么所有EGFR-TKI进展的患者都需要进行T790M突变检测?
(一)EGFR TKI治疗前后T790M的突变率比较
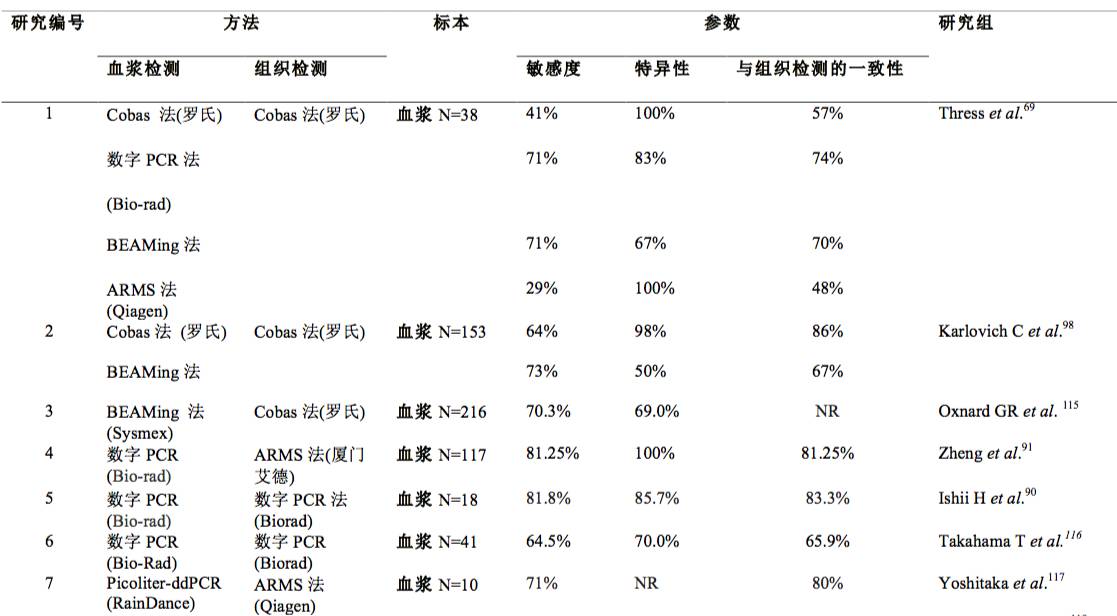
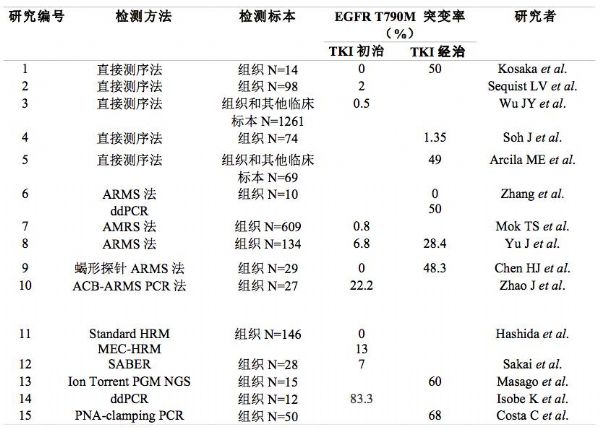
中西方人群,EGFR突变率有别。东亚NSCLC患者中,EGFR突变率为30-40%,而高加索NSCLC患者中,EGFR突变率仅为5-13%,因此,对于东亚人群,进行EGFR的突变检测尤为重要。既往的文献报道显示,对于未接受过EGFR TKI治疗的EGFR突变患者,T790M突变率低于5%,而一代EGFR TKIs耐药的患者,T790M突变率高达50%~62%。下表1和表2分别总结了晚期NSCLC患者EGFR TKI治疗前后,血浆和组织检测T790M突变的发生率。在晚期NSCLC患者中,EGFR TKI治疗前,T790M的突变率大多数的研究报道的T790M突变率<5%,仅3项研究报道,EGFR TKI治疗前有50%的患者检测到T790M突变。这3项研究中,其中1项研究的样本量较小,另两项研究均采用敏感度较高的检测方法,可以检测到非常低丰度的突变(分别为数字PCR和集落杂交法),这些可能与检测到较高的T790M突变率有关。在Xin Ye等人的报道中,使用36对EGFR TKI治疗前的配对的FFPE(福尔马林固定石蜡包埋)肿瘤样本和冻存新鲜样本采用灵敏度为0.1%的ME-PCR方法进行T790M检测,发现在FFPE样本中T790M阳性率为41.7%(15/36),但配对的新鲜样本中T790M阳性率仅为2.8%,提示FFPE样本中用超高敏感方法检测到的T790M突变可能会是福尔马林固定带来的假阳性。
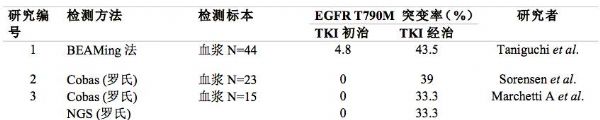
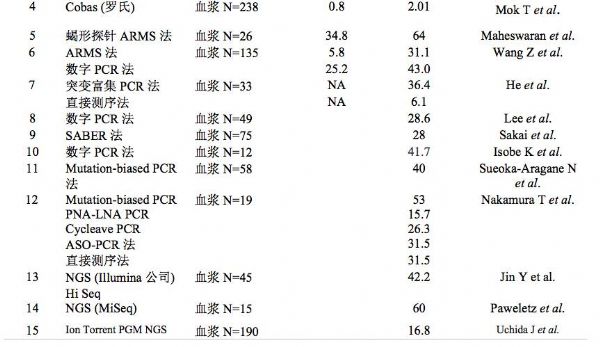
在EGFR TKI治疗进展后的患者中,T790M的突变率大多数的研究显示,大约为50%~62%。少数研究中,耐药患者T790M的突变率较低,可能与检测方法的敏感性(直接测序法)和耐药组织标本的异质性有关。耐药后T790M突变与否,与患者接受一线或二线TKI治疗的疗效持续时间直接相关。如下表1和2所示,不同研究中,采用不同的标本检测(组织或血浆标本),T790M的突变率亦存在差异。
其中,有几项研究是来自中国人群的数据,这些研究分别采用了不同的检测平台,研究入组的样本量也不同。目前仍然缺乏中国人群大样本的研究。值得期待的是, CSCO ASTRIS(该研究是一项由阿斯利康全球发起的开放性、多国、多中心的真实世界治疗研究)中心实验室检测T790M突变率的研究数据将会发表,这是第一个中国人群的大样本研究。
表1. 采用组织标本检测EGFR TKI治疗前后T790M的突变率
表2. 采用血浆标本检测EGFR TKI治疗前后T790M的突变率
(二)EGFR T790M突变阳性和阴性患者接受三代EGFR TKI治疗的疗效
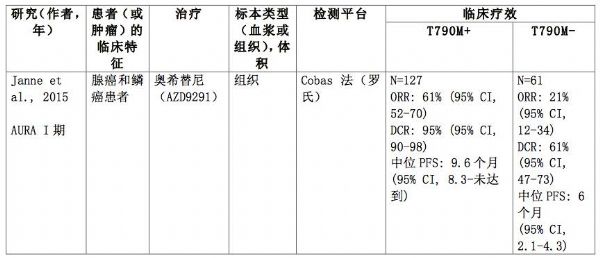
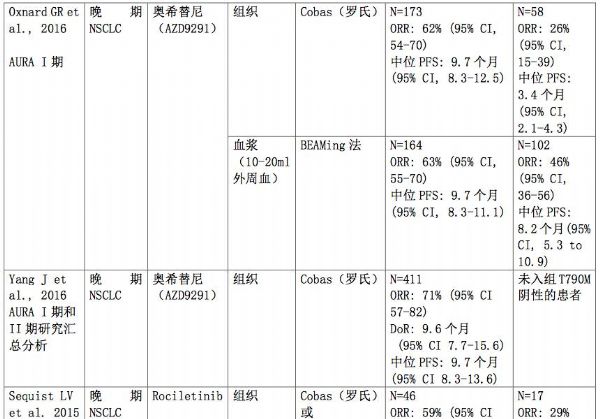
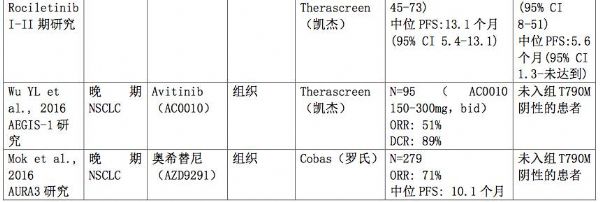
既往的研究,还报道了EGFR T790M突变阳性和阴性患者,接受三代EGFR TKI治疗的疗效,总结见下表。对于T790M阳性患者,接受三代EGFR TKI治疗的ORR为60-70%,中位PFS为9.6-10.1个月。而在组织检测T790M阴性的患者中,三代EGFR TKI治疗的ORR为20%左右,而血浆检测T790M阴性的患者,奥希替尼的ORR为46%,这可能于血浆检测存在假阴性的情况有关。因此,对于EGFR TKI耐药的患者,应该进行T790M突变检测,寻找真正能从三代EGFR TKI治疗中获益的人群,真正实现耐药后的精准治疗。
表3. EGFR T790M突变阳性和阴性患者接受三代EGFR TKI治疗的疗效
表注:ORR,客观缓解率;DCR,疾病控制率;PFS,无进展生存期;PRR,部分缓解率;SD,疾病稳定;PD,疾病进展;DoR,疗效持续时间;NR,未报道。
总结
T790M突变是EGFR TKI最主要的耐药机制,约占耐药人群的50%~62%。随着泰瑞沙在中国的上市,克服T790M突变导致的耐药成为可能。对于耐药后的患者,T790M阳性患者接受三代EGFR TKI治疗的疗效显着优于T790M阴性的患者。因此,鼓励对所有耐药患者进行T790M突变检测,真正实现耐药后精准治疗。
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
小提示:本篇资讯需要登录阅读,点击跳转登录







#耐药患者#
49
#EGFR TKI#
32
#T790M#
28
#精准治疗#
31
#TKI#
30