Eisai和Biogen正在向FDA申请aducanumab治疗阿尔茨海默症的优先审查
2020-08-09 Allan MedSci原创
制药公司百健(Biogen)和卫材(Eisai)近日表示,FDA接受了aducanumab治疗阿尔茨海默症优先审查的申请,并将目标行动日期定为明年3月7日。
制药公司百健(Biogen)和卫材(Eisai)近日表示,FDA接受了aducanumab治疗阿尔茨海默症优先审查的申请,并将目标行动日期定为明年3月7日。两家公司指出,该机构还打算举行一次咨询委员会会议,以讨论该提案,并补充说,如果可能的话,监管机构计划尽早采取行动。
Aducanumab(BIIB037)是一种研究性人类单克隆抗体,已被研究用于治疗早期阿尔茨海默氏病。根据合作开发和许可协议,Biogen从Neurimmune获得了aducanumab。自2017年10月以来,百健(Biogen)和卫材(Eisai)在全球范围内合作开展了aducanumab的开发和商业化。
EMERGE和ENGAGE是III期多中心、随机、双盲、安慰剂对照、平行组研究,旨在评估aducanumab的疗效和安全性。这项研究的主要终点是评估每月剂量的aducanumab与安慰剂相比在减少认知和功能障碍方面的功效,这是通过CDR-SB评分的变化来衡量的。次要终点是评估aducanumab与安慰剂相比对MMSE、ADAS-Cog 13和ADCS-ADL-MCI评分变化的影响。详细见:Biogen的aducanumab治疗阿尔茨海默氏病符合III期试验终点
阿尔茨海默症俗称早老性痴呆、老年痴呆,是一种发病进程缓慢、随着时间不断恶化的神经退化性疾病,此病症占了痴呆症中六到七成的成因。最常见的早期症状为丧失短期记忆(难以记住最近发生的事),当疾病逐渐进展,症状可能逐渐出现,包括语言障碍、定向障碍(包括容易迷路)、情绪不稳、丧失动机、无法自理和许多行为问题。
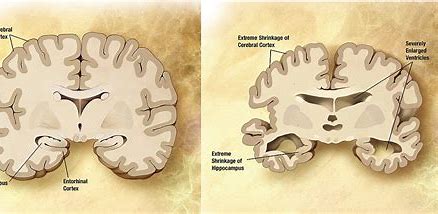
原始出处:
https://www.firstwordpharma.com/node/1747363?tsid=4
Frost CV, Zacharias M. From monomer to fibril: Abeta-amyloid binding to Aducanumab antibody studied by molecular dynamics simulation.Proteins. 2020 Jul 14. doi: 10.1002/prot.25978.
Mullane K, Williams M.Alzheimer's disease beyond amyloid: Can the repetitive failures of amyloid-targeted therapeutics inform future approaches to dementia drug discovery?Biochem Pharmacol. 2020 Jul;177:113945
作者:Allan
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#mAb#
39
#阿尔茨#
28
#Bio#
30
#阿尔茨海#
41
重点看疗效
108