中山大学邓文斌、邓冠军《AFM》:神经胶质细胞外泌体涂覆光热剂治疗恶性胶质瘤
2023-12-31 BioMed科技 BioMed科技
在本研究中,中山大学邓文斌教授、邓冠军副教授和中欧创新医药与健康研究中心蔡林涛研究员等人合成了两种具有NIR-II荧光发射的AIE光热剂(Fs和Fo)。
免疫检查点阻断(ICB)治疗癌症疗效显著,但对胶质母细胞瘤(GBM)疗效不佳。一方面是因为药物难以穿透血脑屏障(BBB)进入GBM,另一方面是GBM微环境中缺乏足够的预先存在的细胞毒性CD8+T细胞。
在本研究中,中山大学邓文斌教授、邓冠军副教授和中欧创新医药与健康研究中心蔡林涛研究员等人合成了两种具有NIR-II荧光发射的AIE光热剂(Fs和Fo)。随后,作者通过基因工程技术构建了工程化小胶质细胞外泌体AIE纳米颗粒(EE@Fs-NPs)。工程化小胶质细胞外泌体赋予EE@Fs-NPs穿过血脑屏障并靶向GBM的能力,成功地将抗LAG3递送到GBM,增强肿瘤细胞的热敏性。因此,AIE光热剂EE@Fs-NPs可产生温和的光热疗法以破坏肿瘤细胞并改善细胞毒性CD8+T细胞在GBM中的浸润,从而可增加ICB疗法的反应性。因此,EE@Fs-NPs产生强大的温和光热免疫协同治疗效果,将为GBM的有效治疗提供理想的平台。相关工作以“Engineered Microglia-Exosomes Coated Highly Twisting AIE Photothermal Agents to Efficiently Cross Blood-Brain-Barrier for Mild Photothermal-Immune Checkpoint Blockade Therapy in Glioblastoma”为题发表在Advanced Functional Materials。

【文章要点】
光热治疗(PTT)中经常会遇到两个瓶颈。首先,肿瘤细胞产生热休克蛋白(HSPs)以启动PTT中的热应激耐受,这使肿瘤细胞对热效应不敏感。另一个瓶颈是光热剂的热转换效率。光热剂的高光热转换效率也是开发温和PTT的关键因素。为此,在本研究中,作者设计了新型高效光热剂。如图1所示,作者通过基因工程技术在小胶质细胞外泌体(MG-Exo)上表达免疫检查点LAG3抑制性抗体(抗LAG3),设计了工程化小胶质细胞外泌体(工程化MG-Exo)。然后通过“冻融循环”膜融合方法将工程化的MG-Exo与AIE光热剂纳米颗粒(Fs-NPs)融合,制备了工程化的小胶质细胞外泌体AIE纳米颗粒(EE@Fs-NPs)。
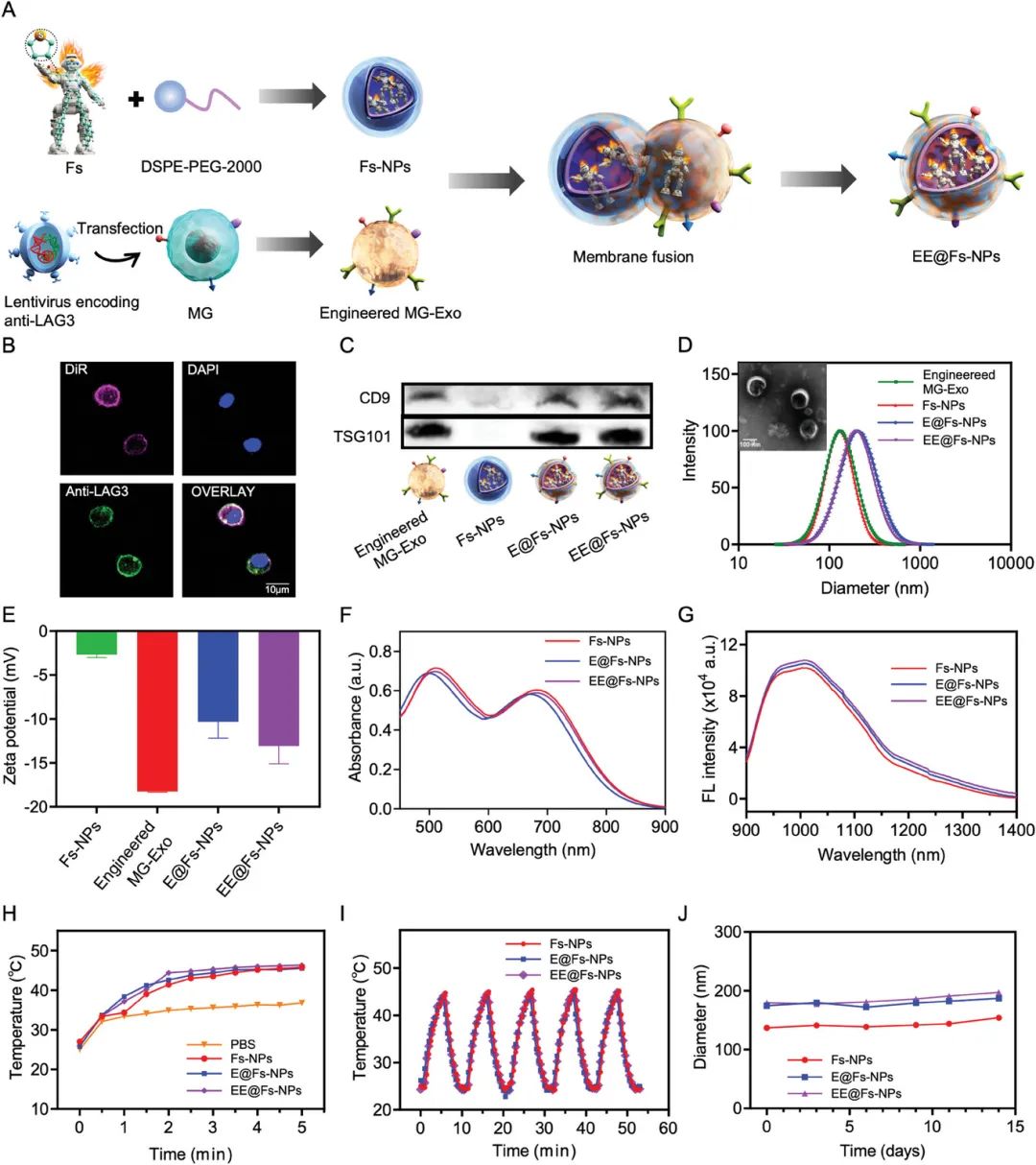
图1 EE@Fs-NPs的构建
研究显示,通过简单地将一个O原子变为S原子可增加AIE光热制剂的分子扭曲,从而可将Fs光热转化效率提高到48%。而抗LAG3可高度逆转T细胞耗竭,并产生TNF-α,从而抑制热休克蛋白的表达。而位于EE@Fs-NPs核心的AIE光热剂进一步引发温和的PTT并发射NIR-II荧光。温和的PTT还释放肿瘤抗原以刺激肿瘤特异性T细胞的产生,这增加了T细胞在GBM中的浸润,从而改善了ICB治疗的反应(图2)。这种温和的光热ICB疗法为提高GBM的治疗效果提供了巨大的潜力,并有望成为一种有效治疗该疾病的新方法。。
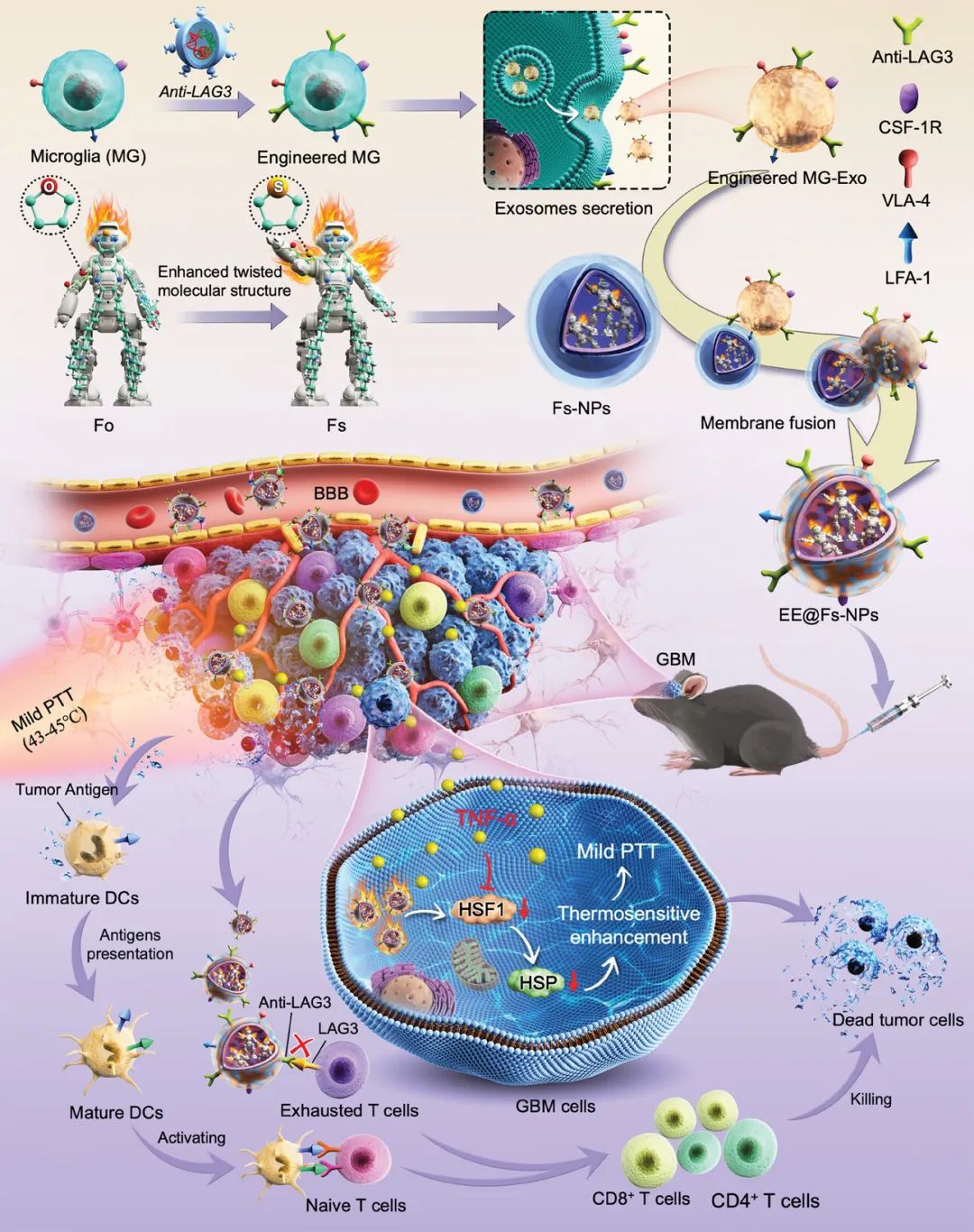
图2 抗GBM治疗示意图
作者:BioMed科技
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#胶质母细胞瘤# #光热治疗# #神经胶质细胞外泌体#
57