Nature Cell Biology:亮氨酸tRNA合成酶是乳腺癌的肿瘤抑制因子
2022-03-19 nagashi “生物世界”公众号
癌症因其复杂性和难治性,一直是医学界的一道难以跨越的天堑。癌症的发生与许多因素相关,从分子生物学的角度来看,肿瘤的发生发展都涉及转录组和翻译组的改变,但与转录控制不同,翻译控制在癌症中的研究较少。
癌症因其复杂性和难治性,一直是医学界的一道难以跨越的天堑。癌症的发生与许多因素相关,从分子生物学的角度来看,肿瘤的发生发展都涉及转录组和翻译组的改变,但与转录控制不同,翻译控制在癌症中的研究较少。
值得注意的是,转运RNA(tRNA)丰度的增加和氨基酸偶联通常会促进肿瘤发生的增加。
近日,美国洛克菲勒大学和加州大学旧金山分校的研究人员在 Nature Cell Biology 期刊发表了题为:Leucyl-tRNA synthetase is a tumour suppressor in breast cancer and regulates codon-dependent translation dynamics 的研究论文。
这项研究表明,在乳腺癌中,亮氨酰tRNA合成酶(LARS)是一种重要的抑癌因子,LARS缺失或表达下调会促进肿瘤的发生发展。

癌细胞的翻译组变化主要体现在蛋白质合成活性的整体增加和特定mRNA的选择性翻译,这些mRNA编码的蛋白质涉及细胞增殖、迁移、生存、转化、血管生成和恶性进展的其他生理驱动因素。
这些翻译组变化又与mRNA翻译因子的过表达相关。令人惊讶的是,在这些因子中,有一些是进化上最保守的蛋白质合成因子——氨酰-tRNA合成酶(ARSs),它将氨基酸与它们各自的tRNA配对生成氨酰-tRNA,随后通过延伸因子传递到核糖体进行肽链合成。因此,ARSs在翻译中起着至关重要的作用。
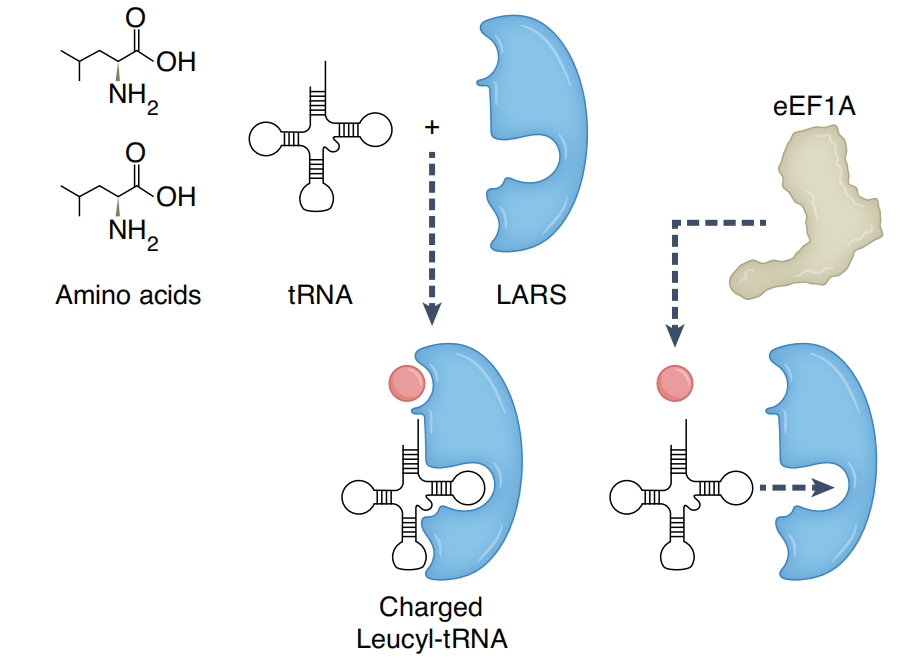
氨酰-tRNA合成酶(ARSs)催化氨酰-tRNA的合成
近年来,科学家们发现某些ARSs除了生成氨酰-tRNA之外,还在促进血管生成、炎症和肿瘤发生等方面发挥着重要作用。这刺激了新治疗药物的实验性开发,包括小分子药物,可以抑制癌症治疗中的某些ARS。
在这项最新研究中,研究?团队描述了一种全新的、ARS促进肿瘤发生的机制:一种特定的tRNA合成酶,即亮氨酸-tRNA合成酶(LARS)的活性有助于细胞转化的早期程序,并对肿瘤的发生发展有重要的抑制作用。
研究团队首先通过查询美国国家癌症研究所(NCI)的癌症基因组图谱(TCGA)数据库,比较正常和乳腺癌的mRNA表达水平,来确定人类乳腺癌中所有20个tRNA合成酶的mRNA表达水平。他们惊奇地发现,在三阴性乳腺癌(TNBC)细胞系和病人样本中,4种ARSs(LARS、KARS、 QARS和DARS)的表达量下降,而其余16种ARSs的表达增加。
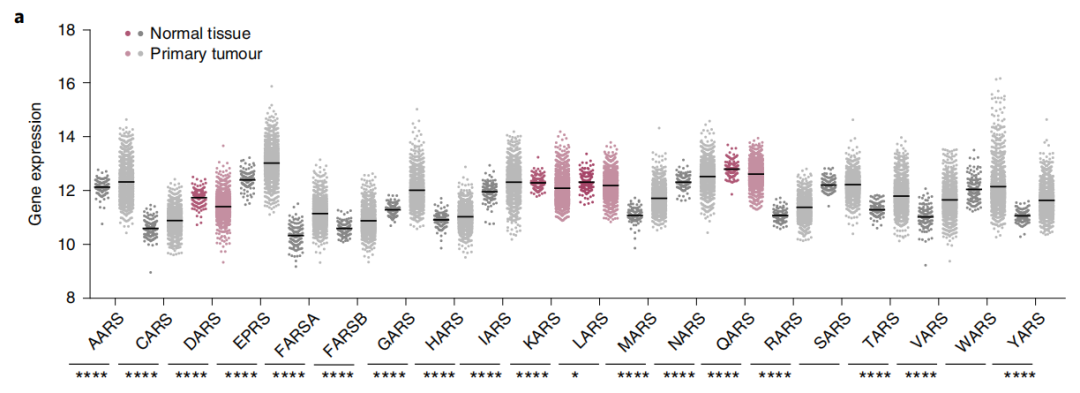
在三阴性乳腺癌中,4种ARSs(LARS、KARS、 QARS和DARS)的表达量下降
研究团队进一步探究了这四种ARSs是否作为肿瘤抑制因子发挥作用。研究团队首先证明,在这4种ARSs中,LARS在人乳腺癌和小鼠乳腺癌细胞株和肿瘤发展期间显示出最一致的下调。不仅如此,研究人员还构建了LARS缺失的乳腺癌小鼠模型(MMTV-PyMT),结果表明,LARS的减少导致肿瘤数量和负担显着增加。
为了确定LARS的肿瘤抑制作用是否源于其合成酶活性,研究团队从LARS缺失的MMTV-PyMT小鼠中生成了Cre阳性的类器官,证明野生型LARS表达可以挽救肿瘤抑制表型。此外,缺乏亮氨酸结合能力的LARS突变体(F50A/Y52A)或缺乏催化位点活性的LARS突变体(K716A/K719A)的表达并不能挽救肿瘤抑制表型。
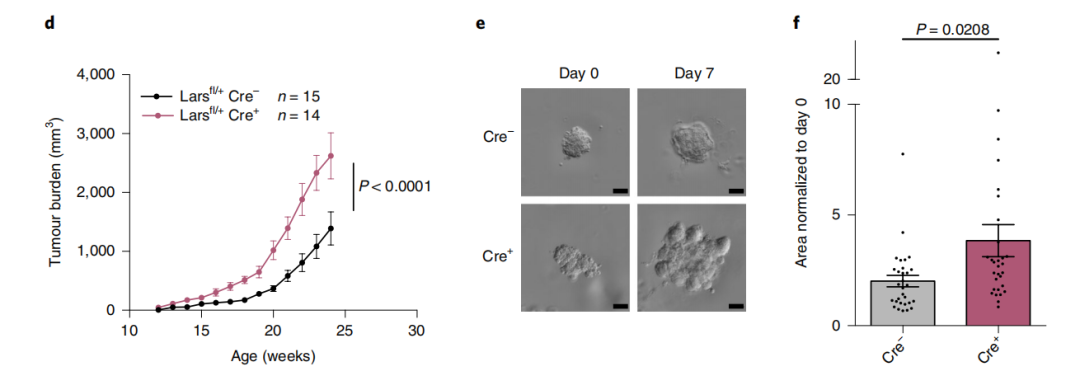
野生型LARS可抑制肿瘤的发生和增殖
亮氨酸具有多种密码子,鉴于只有具有催化活性的LARS才能抑制肿瘤生长,作者研究了LARS肿瘤抑制是否涉及特定亮氨酸-tRNA水平的改变。研究结果显示,随着LARS耗竭,tRNA-LeuCAG的减少最为显着。
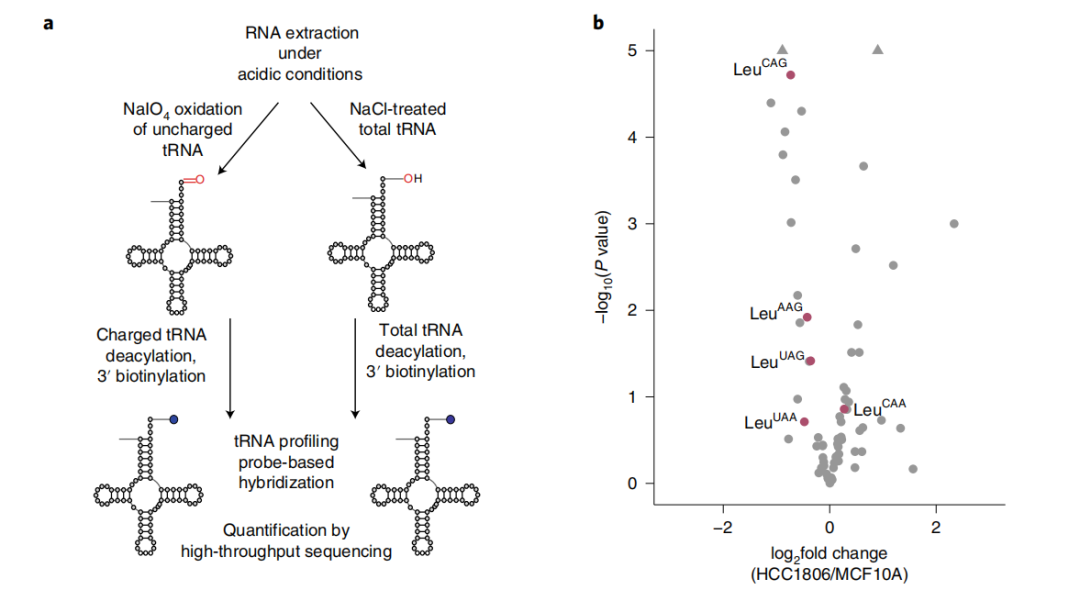
随着LARS耗竭,tRNA-LeuCAG的减少最为显着
接下来,研究团队进行了全基因组研究,他们发现LARS表达下调主要导致Leu-CUC和Leu-CUG密码子密度较高的mRNA翻译量减少,而这些mRNA编码的蛋白中就有两种肿瘤抑制蛋白——EMP3(编码上皮膜蛋白3)和GGT5(编码γ谷氨酰转移酶5),它们的缺失促进了肿瘤的生长。
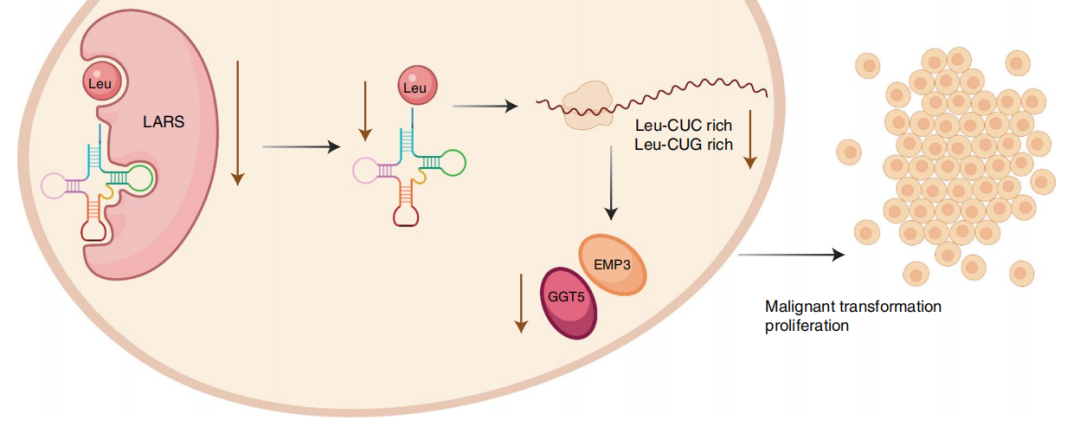
LARS表达下调导致肿瘤抑制蛋白EMP3和GGT5的减少
总而言之,这项研究揭示了一种乳腺癌发生发展的新机制——亮氨酰-tRNA合成酶(LARS)的表达下调,将导致EMP3和GGT5等肿瘤抑制蛋白的减少,从而促进乳腺癌的发生发展。

研究模式图
当然,这项研究提出了几个重要的问题:
1)LARS在正常细胞和癌细胞中是如何调节的?
2)为什么LARS在乳腺癌中下调但是在肾癌、肺癌和其他器官癌症中过表达呢?
3)核糖体在同源tRNA-LeuCAG密码子停留时间的增加如何影响mRNA的选择性翻译?
这些过程和具体机制仍需要进一步的研究去发掘。
原始出处:
Maria C. Passarelli, et al. Leucyl-tRNA synthetase is a tumour suppressor in breast cancer and regulates codon-dependent translation dynamics. Nature Cell Biology volume 24, pages 307–315 (2022).
作者:nagashi
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#Biol#
60
#肿瘤抑制因子#
54
#Nat#
34
#Bio#
35
#肿瘤抑制#
54