Nat Commun:炎症性肠病和肥胖的肠道微生物共丰度网络具有特异性
2020-08-17 网络 网络
肠道微生物参与营养物质的消化和降解,维持消化道的完整性,刺激宿主免疫系统和调节宿主代谢。近年来,肠道微生物与某些疾病(包括糖尿病、心血管疾病、肥胖和慢性胃肠道疾病(如炎症性肠病)之间的关系已被确认。
肠道微生物参与营养物质的消化和降解,维持消化道的完整性,刺激宿主免疫系统和调节宿主代谢。近年来,肠道微生物与某些疾病(包括糖尿病、心血管疾病、肥胖和慢性胃肠道疾病(如炎症性肠病)之间的关系已被确认。多数与人类疾病相关的因素是微生物多样性降低、微生物组成改变以及某些微生物丰度和通路。然而,肠道微生物群是一个复杂的生态系统,微生物可以通过复杂的生态相互作用来交换或竞争营养物质、信号分子或免疫逃避机制。因此,这些微生物之间的相互作用是研究的重点。
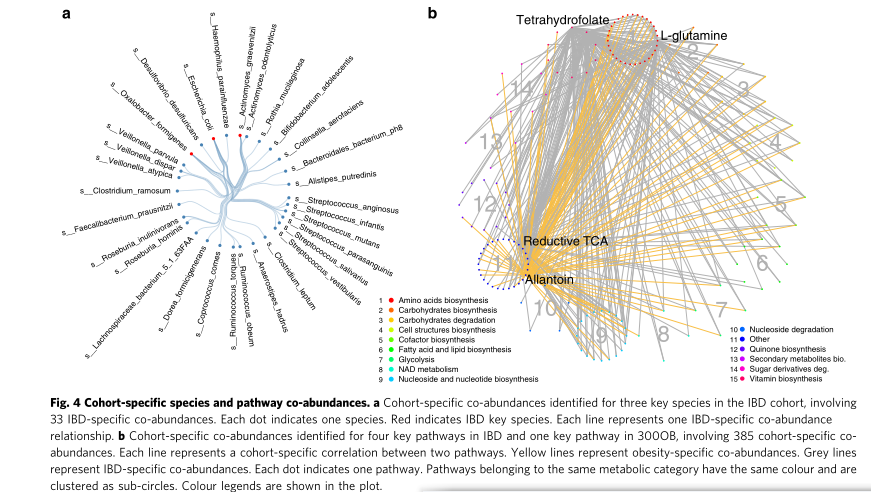
本研究对来自荷兰的四个人类队列的2379个基因组进行构建并比较了相互之间的微生物共丰度网络,包括炎症性肠病(IBD)队列、肥胖队列和两个基于人群的队列。研究发现,38.6%的微生物种类丰度的和64.3%的通路共丰度在队列间差异显著,其中113个菌种丰度和1050个通路丰度显示IBD队列特异性效应,281个通路丰度显示肥胖特异性效应。在IBD中发现了3个菌种和4个通路,以及300个肥胖相关中的1个通路,它们在疾病特异性共丰度网络中起关键作用。在肥胖中,allantoin degradation通路是一个关键通路,肥胖特异性共丰度与85个通路相关,主要与草酰乙酸/天冬氨酸氨基酸的生物合成呈负相关,与胰岛素分泌和葡萄糖代谢有关。
这项研究基于元基因组测序进行微生物网络分析,以检测微生物菌种和功能通路。肠道微生物的失调可以通过丰度水平的改变和微生物相互作用的水平进行评估。IBD和肥胖特异性的菌种和通路可能在疾病中调节微生物生态系统中发挥重要作用,这些疾病特异性微生物相互作用扩展了目前对微生物组在疾病中作用的认识。
原文出处:
Lianmin Chen, Gut microbial co-abundance networks show specificity in inflammatory bowel disease and obesity, Nature communication,2020,11:4018
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





#COMMUN#
74
#Nat#
63
#特异性#
74
👍🏻
116
!
123