PNAS:演化中丢失的基因,让人类备受心血管疾病困扰
2019-07-24 佚名 中国生物技术网
近日,美国加州大学圣地亚哥分校医学院的一项研究发现,我们的祖先在二、三百万年前丢失了一个基因,结果导致人类这个物种患心血管疾病风险增加,同时显示该基因的缺失使吃红肉也会给人类带来了进一步的风险。该研究7月22日已发表在《美国国家科学院院刊(PNAS)》上。
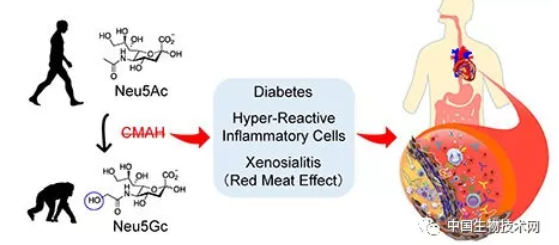
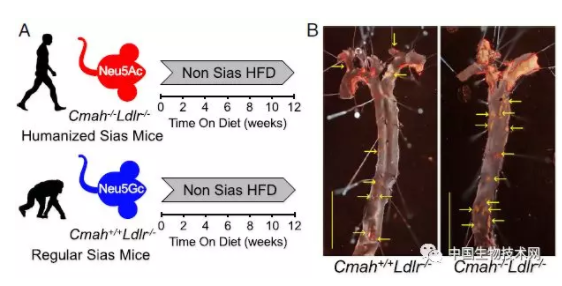
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言



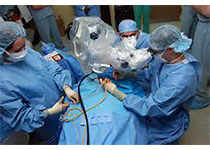

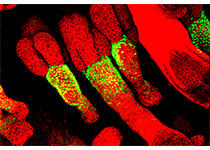


心血管疾病的治疗。
68
#PNAS#
33
心血管疾病的影响。
78
人类备受心血管疾病困扰。
59
人类备受心血管疾病困扰。
72