Mol Cancer:无需活检,抽血即可检测,采用免疫治疗的胃癌患者的福音!
2020-12-16 MedSci原创 MedSci原创
胃癌是全球的第五常见恶性肿瘤,也是癌症相关死亡的第三原因。免疫检查点抑制剂(ICI),主要是抗PD-1抗体,已被推荐用于转移性胃腺癌患者的姑息治疗,相关的预后生物指标有微卫星不稳定(MSI)状态、PD
胃癌是全球的第五常见恶性肿瘤,也是癌症相关死亡的第三原因。免疫检查点抑制剂(ICI),主要是抗PD-1抗体,已被推荐用于转移性胃腺癌患者的姑息治疗,相关的预后生物指标有微卫星不稳定(MSI)状态、PD-L1表达的联合阳性评分(CPS)和EB病毒(EBV)状态。然而,在临床上,晚期胃癌患者可能缺乏新鲜的肿瘤组织,只能通过有创性再活检获取组织样本进行预后评估。
据报道,循环肿瘤细胞DNA(ctDNA)可用于鉴定遗传改变和预测预后,分析靶向治疗的耐药性以及监测胃癌的复发或进展。而且,ctDNA可以提供对肿瘤特异性遗传特征的纵向和动态监视,而无需重复进行侵袭性肿瘤活检。但目前ctDNA在胃癌遗传特征分析中的研究了了。
因此,本研究旨在探索ctDNA对采用免疫治疗的胃癌患者的预后的预测价值。
2018年10月-2019年12月,共招募了46位接受PD-1抗体免疫治疗和425个基因二代测序(NGS)测序的进展期胃癌患者,其中38位患者有组织样本,43位有基础血液样本。
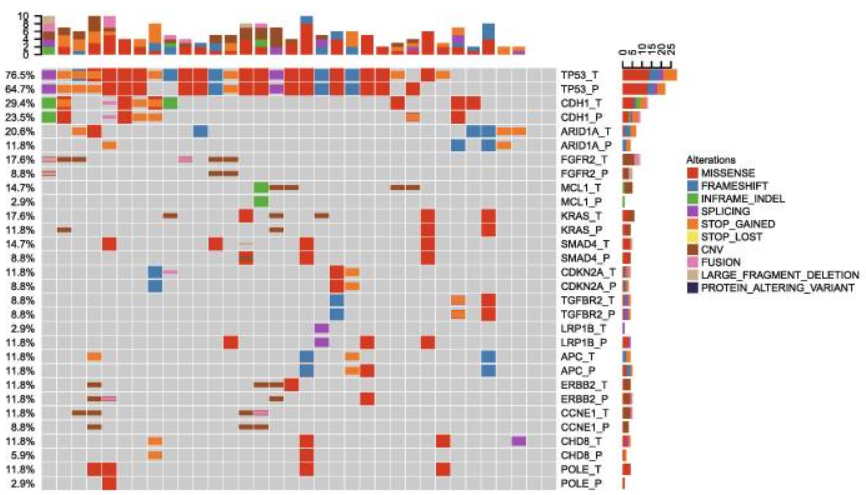
34对组织样本和血液样本中检测出的高频变异
评估了43位患者基础血液样本的ctDNA,88.4%的患者至少携带一个胚系突变,且与组织样本的测序结果保持一致。
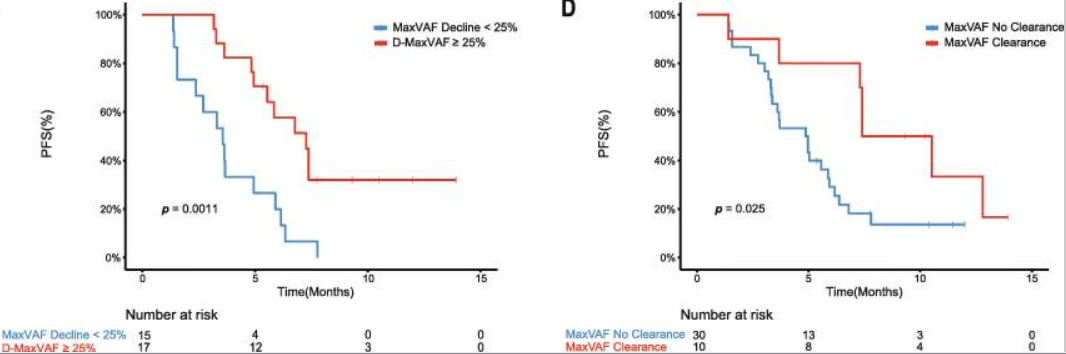
maxVAF的降低情况与患者的PFS的相关性
最大体细胞变异等位基因频率(maxVAF)下降25%以上的患者的无进展生存期(PFS)较长,药物治疗缓解率较高(maxVAF>25% vs maxVAF<25%的患者:7.3个月 vs 3.6个月,p=0.0011;53.3% vs 13.3%,p=0.06)。治疗后检测不到ctDNA和可检出的患者的中位PFS分别为7.4个月和4.9个个月(p=0.025)。
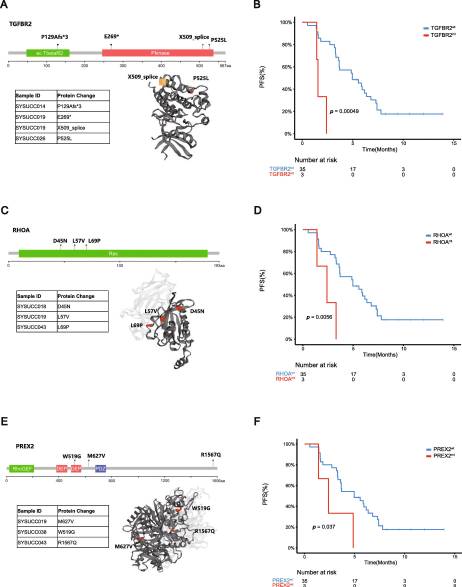
TGFBR2、RHOA和PREX2基因突变对免疫治疗预后的影响
基础ctDNA中TGFBR2、RHOA和PREX2的突变状态会影响免疫治疗的疗效(p<0.05)。携带CEBPA、FGFR4、MET或KMT2B基因突变的患者发生免疫相关不良事件(irAE)的可能性更大。
综上所述,ctDNA可作为进展期胃癌免疫治疗应答的潜在生物标志物,其预测irAE的潜在作用值得进一步探讨。
原始出处:
Jin Ying,Chen Dong-Liang,Wang Feng et al. The predicting role of circulating tumor DNA landscape in gastric cancer patients treated with immune checkpoint inhibitors.[J] .Mol Cancer, 2020, 19: 154.
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言






#胃癌患者#
69
学习了,获益匪浅
125
#胃癌#CtDNA广泛应用还是有点难度的
182
#活检#
60
ctDNA可作为进展期胃癌免疫治疗应答的潜在生物标志物
129