首例:携带罕见BRAF p.N486_N490del突变的非小细胞肺癌获益达拉非尼联合曲美替尼
2024-05-15 苏州绘真医学 苏州绘真医学
本文介绍了一名既往接受过治疗的转移性肺腺癌患者,该患者携带BRAF p.N486_N490del突变,随后接受了达拉非尼+曲美替尼的联合治疗,取得了临床缓解。
BRAF是一种丝氨酸/苏氨酸蛋白激酶,在MAPK通路中发挥着至关重要的作用,该通路控制细胞增殖和存活。BRAF突变(特别是V600E)长期以来一直被认为是多种肿瘤的驱动因素。使用靶向治疗阻断由该突变引起的异常信号级联已获证可以改善多种肿瘤预后,包括恶性黑色素瘤、甲状腺未分化癌和结直肠癌。BRAF突变约在 4% 非小细胞肺癌(NSCLC)中检出;然而,50% 是非V600突变。BRAF突变根据其对激酶活性、RAS依赖性和二聚化状态的影响分为 3 类。I类突变发生在V600密码子处,并以不依赖RAS的方式通过BRAF单体激活来激活激酶活性。II类突变也通过不依赖RAS的方式通过BRAF二聚化激活激酶活性。许多非V600突变,包括本文患者中描述的突变,都属于II类。III类突变也称为“激酶死亡”(kinase-dead)突变,其激酶活性与野生型BRAF相比非常低。尽管达拉非尼联合曲美替尼(分别针对BRAF和MEK的药物)已在携带I类BRAF突变(特别是V600E)的转移性非小细胞肺癌中表现出良好的活性,但其在治疗II类和III类突变中的作用尚不清楚。
本文介绍了一名既往接受过治疗的转移性肺腺癌患者,该患者携带BRAF p.N486_N490del突变,随后接受了达拉非尼+曲美替尼的联合治疗,取得了临床缓解。据研究人员所知,这是首个报道携带这种罕见突变的NSCLC患者,并对靶向BRAF/MEK通路的药物有反应。

病 例
患者女,79 岁,在接受多西他赛三线治疗时出现新的恶性腹水。一年前,患者被发现患有恶性胸腔积液,之后确诊患有IV期非小细胞肺癌。当时患者肿瘤细胞的PD-L1肿瘤比例评分(TPS)为 90%,靶向突变panel没有发现基因变异,表明可以使用FDA批准的药物进行治疗。然而,更大的基因panel检测分析发现了一种罕见的BRAF p.N486_P490del插入缺失,预计会产生具有活性激酶的BRAF蛋白(图S1)。患者最初接受了帕博利珠单抗单药治疗,但由于再次接受帕博利珠单抗治疗后出现 2 级结肠炎复发而终止。随后患者接受了卡铂和培美曲塞治疗,随后接受培美曲塞维持治疗,直至出现肝转移和腹膜病变进展。值得注意的是,患者在确诊为NSCLC时偶然间发现左上叶和左下叶存在栓塞,考虑到贝伐珠单抗会使静脉栓塞发生率增加,在讨论后,将贝伐珠单抗从患者的二线治疗方案中移除。随后,患者改用多西他赛并接受了 3 个周期治疗,出现恶性腹水症状,需要重复进行腹腔穿刺术引流。在疾病进展时,患者的腹水检测显示转移性肺腺癌(图S2),NGS再次检测到BRAF p.N486_N490del。检测到的其它突变包括IDH1(p.R132C)、TET2(p.N71fs)和TP53(p.G245S)致病性突变,以及ATR(p.I859K)意义不明变异。根据BRAF突变可能对功能产生的影响,以及其它肿瘤类型对BRAF/MEK通路抑制剂敏感性的报告(表S1),研究人员向患者提供了达拉非尼联合曲美替尼跨适应症治疗。在开始使用达拉非尼+曲美替尼时,对患者的胸部、腹部和骨盆进行分期CT扫描,结果显示有大量肺部肿块、局限性右侧胸腔积液、纵隔淋巴结肿大、腹膜结节和腹水(图1)。脑部核磁共振检查显示没有明确的转移性病灶。
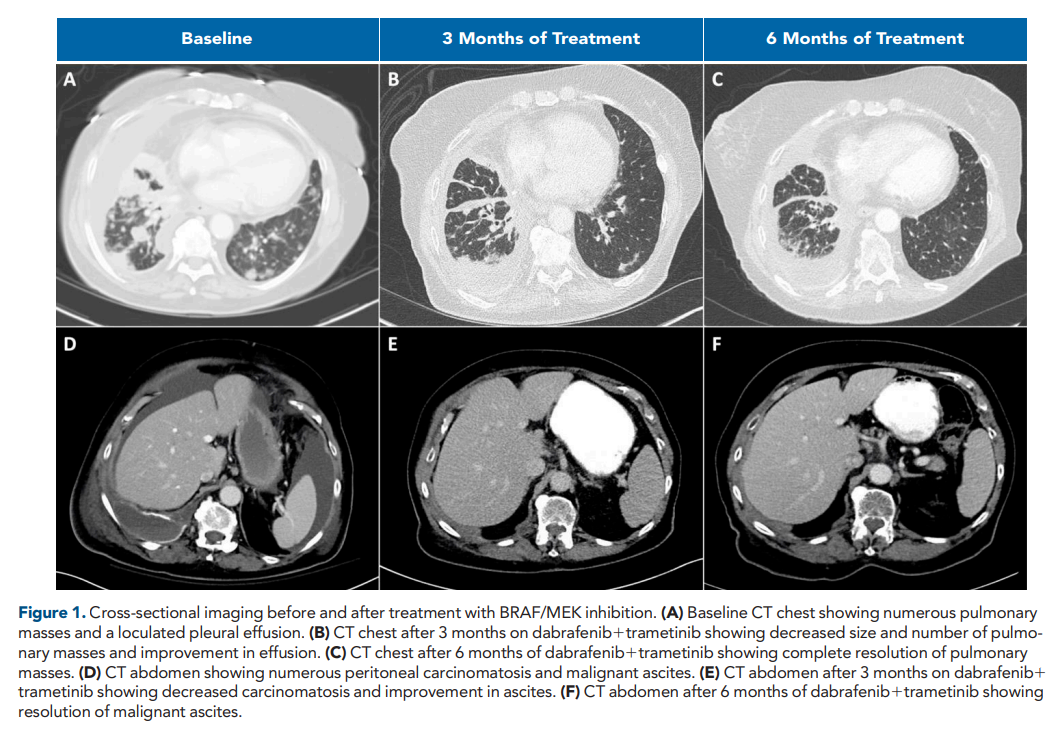
▲图1 BRAF/MEK抑制剂治疗前后的横截面成像
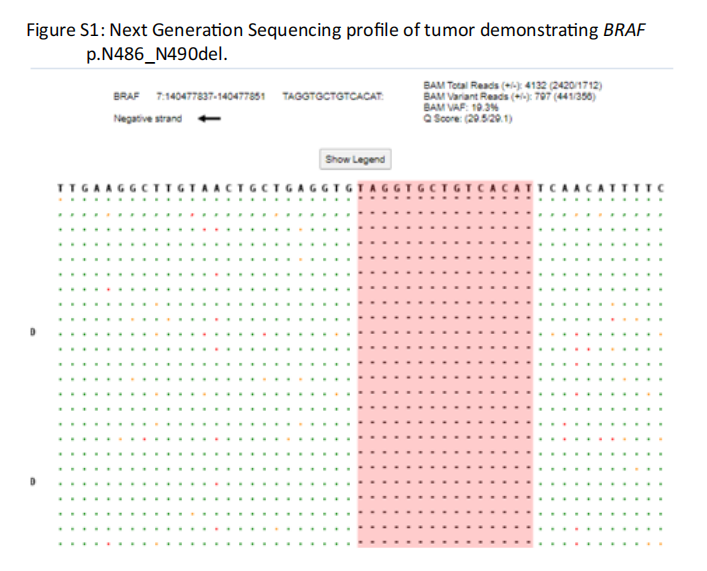
▲图S1 NGS证实肿瘤携带BRAF p.N486_N490del突变
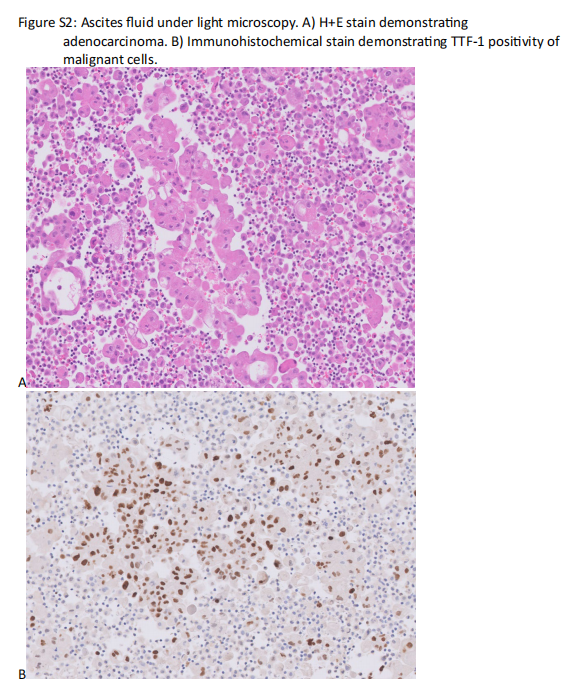
▲图S2 光镜下的腹水检查结果
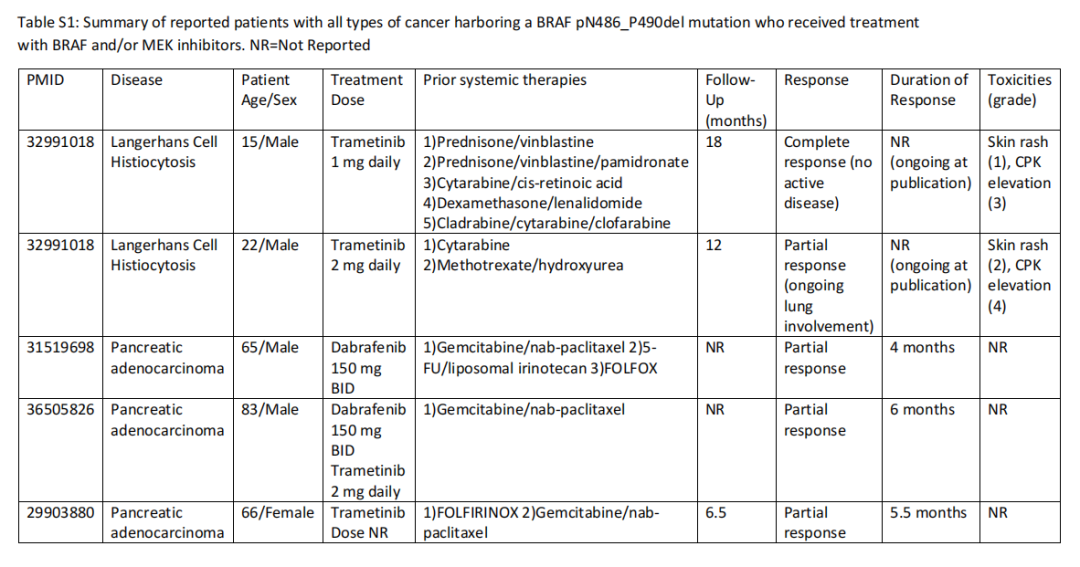
▲表S1 文献中所有接受BRAF和/或MEK抑制剂治疗的、携带BRAF pN486_P490del突变的患者汇总
患者此前需要每月进行腹腔穿刺术来控制恶性腹水。但在开始达拉非尼+曲美替尼治疗后不久,患者不再需要腹腔穿刺术,并且没有进一步的腹水临床证据。治疗 3 个月后,影像学检查显示出现治疗反应,多发性肺部肿块的大小和数量减少,腹水得到改善(图1)。治疗 6 个月后,CT扫描显示患者对达拉非尼+曲美替尼有持续反应。患者在治疗 9 个月后继续接受治疗。显著的不良反应包括不发热且不需要生长因子支持治疗的短暂性 3 级中性粒细胞减少症,以及不伴出血且不需要输血的 1 级血小板减少症。
讨 论
据研究人员所知,本文报告了首例携带BRAF p.N486_P490del突变的NSCLC患者,该患者对达拉非尼和曲美替尼联合治疗持续产生深度和持久的反应。本文病例强调需要继续扩大BRAF非V600突变和NSCLC患者其它靶向突变的了解。自从它们被认为是可靶向的基因变异以来,检测非小细胞肺癌中是否存在致癌基因“驱动”突变和重排已成为制定最佳管理策略的必要条件。然而,许多突变和变异的临床相关性和治疗意义仍未明确,因此需要不断确定哪些变异可以真正预测靶向治疗的反应。
BRAF突变NSCLC靶向治疗的作用主要集中在I类突变,主要是V600E。BRAF和MEK抑制治疗的作用是在一项非随机II期研究中确定的,该研究中患有转移性BRAF V600E突变的 NSCLC患者接受了达拉非尼和曲美替尼联合治疗。8 名患者被分为未接受治疗和既往治疗组。总共有 36 名未接受治疗的患者和 57 名既往接受过治疗的患者入组。在长期随访中,23 名初治患者(63.9%)达到了研究者评估的客观缓解,而既往接受治疗的患者中有 39 名(68.4%)达到了客观缓解。基于这一结果,达拉非尼+曲美替尼联合治疗携带BRAF V600E突变的转移性NSCLC的适应症获得批准。该领域也有其它正在进行的研究,例如探索恩考芬尼(encorafenib)+比美替尼(binimetinib)在携带V600突变(包括V600E、V600K和V600D)的转移性NSCLC患者中的活性。尽管试验仍在进行中,但携带BRAF V600E突变患者的数据已于近期公布。其临床疗效在未接受过治疗(n=59)和既往接受过治疗(n=39)的患者中均得到证实。初治患者的客观缓解率为 75%(95% CI,62%–85%),既往接受过治疗的患者为 46%(95%CI,30%–63%),中位缓解持续时间分别为不可评估(95%CI,23.1 个月-不可评估)和 16.7 个月(95% CI,7.4 个月-不可评估)。这一组合为携带I类BRAF V600E突变的患者提供了另一种可行的治疗选择。
另一方面,II类突变是罕见且异质的,其治疗意义尚不完全清楚。然而,就本文患者中观察到的特定II类突变而言,体外研究表明,它通过BRAF蛋白的β3/αC-螺旋环部分的改变导致BRAF的组成型激活(constitutive activation),该部分在功能上通过创建Glu501/Lys483盐桥将蛋白质锁定在其αC螺旋活性构象中。这反过来又暴露了多个氨基酸残基,以参与 2 个BRAF突变蛋白Arg506/Asp449和Arg509/Thr508之间的同二聚化。结果激活了BRAF二聚蛋白,驱动细胞生长和增殖。有趣的是,临床前研究表明,用达拉非尼治疗携带p.N486_P490del突变的细胞系会产生不同的结果,其中一项研究表明对达拉非尼敏感,而另一项研究则显示没有明显的细胞生长停滞。然而,在该项结果阴性的研究中,曲美替尼治疗显著抑制了细胞增殖。这些观察结果表明抗肿瘤药物作用可能发生在突变蛋白水平或下游,但准确的机制仍不明确。需要进一步的相关研究来开发BRAF/MEK靶向疗法在该突变中的疗效机制模型。
同样缺乏强有力的临床证据来指导携带BRAF非V600 II类和III类突变NSCLC患者的治疗。不幸的是,接受非靶向治疗时,与携带I类突变的患者相比,携带II类或III类BRAF突变的NSCLC患者的无进展生存期和总生存期较差。这些发现强调需要针对II类突变(例如本文患者中发现的p.N486_N490del突变)“量身定制”治疗方法。尽管I类和II类突变之间的分子生物学不同,但它们共享肿瘤发生的致病性过度激活激酶机制,这为靶向BRAF/MEK抑制提供了理论基础。事实上,这种治疗策略与携带这种p.N486_N490del突变的其它肿瘤的临床反应相关(表S1)。已发表多例携带BRAF p.N486_N490del突变的转移性胰腺癌病例报告,其中有病例通过使用BRAF和/或MEK抑制剂实现了临床缓解,持续长达 6 个月。同样,2 名携带p.N486_N490del的朗格汉斯细胞组织细胞增多症患者成功接受曲美替尼治疗,临床缓解长达 1 年以上。
尽管可用于指导BRAF非V600突变患者治疗的临床数据有限,但目前正在进行研究,可能很快就会找到最佳策略。几项前瞻性临床试验正在评估BRAF/MEK靶向疗法对携带BRAF非V600突变的晚期恶性肿瘤的疗效(NCT04439279、NCT04620330、NCT04488003和NCT03839342)。研究人员目标是新增有关II类BRAF p.N486_N490del突变的文献。据研究人员所知,这是首例携带BRAF p.N486_N490del的转移性NSCLC患者对 BRAF/MEK靶向治疗有反应的报告。这种对靶向治疗的反应值得注意,因为非V600 II类和III类BRAF突变患者的最佳治疗策略仍不清楚。
结 论
本文介绍了一名携带非典型II类BRAF p.N480_N490del突变的NSCLC患者,该患者对达拉非尼+曲美替尼联合治疗产生了持续的临床反应,这也是研究人员所知的第一个此类病例。尽管存在针对携带I类BRAF突变的NSCLC的靶向药物,但NSCLC中大约一半的BRAF突变是II类或III类,因此对靶向药物的需求仍未得到满足。本文携带BRAF p.N486_N490del突变的患者对达拉非尼+曲美替尼的强烈反应表明,靶向V600E突变的治疗药物可能会为该人群带来获益,尽管需要进一步的前瞻性研究来解决这个问题。
参考文献:
Sharp JA, Jones D, Rotow JK, Fidias PM, Bertino E, Owen DH. Response to Dabrafenib Plus Trametinib in a Patient With an Uncommon Activating BRAF Mutation: A First in Non-Small Cell Lung Cancer. J Natl Compr Canc Netw. 2024 Mar 13;22(3):e247009. doi: 10.6004/jnccn.2024.7009. PMID: 38479107.

作者:苏州绘真医学
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#非小细胞肺癌# #曲美替尼# #达拉非尼#
6