NMPA批准BYVASDA(贝伐单抗生物仿制药)治疗复发性胶质母细胞瘤
2020-12-31 Allan MedSci原创
BYVASDA®(贝伐单抗生物仿制药)已获得中国国家药品监督管理局(NMPA)的正式批准,用于治疗复发性胶质母细胞瘤(GBM,最常见的恶性原发性脑肿瘤)。
生物制药公司Innovent Biologics近日宣布,BYVASDA®(贝伐单抗生物仿制药)已获得中国国家药品监督管理局(NMPA)的正式批准,用于治疗复发性胶质母细胞瘤(GBM,最常见的恶性原发性脑肿瘤) ,这是BYVASDA®在中国获得的第三个适应症。
BYVASDA®于2020年6月17日首次获得中国国家药品监督管理局(NMPA)批准。BYVASDA®先前获得批准的适应症包括晚期非小细胞肺癌和转移性结直肠癌。
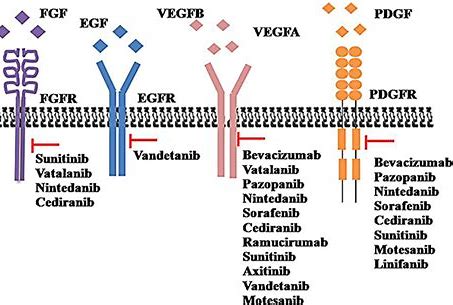
近年来,中国的癌症负担一直在不断增加。根据世界卫生组织(WHO)国际癌症研究机构的报道,2018年中国新诊断癌症患者为428.5万人,癌症死亡286.5万人。在恶性肿瘤中,胶质母细胞瘤是最常见和侵袭性脑恶性肿瘤,其特点是高发病率、高复发率、高死亡率和低治愈率。当前胶质母细胞瘤的主要治疗方案包括手术切除、放疗和化学疗法。中位生存时间仅为12到15个月,在过去十年中没有明显变化。因此,胶质母细胞瘤患者迫切需要更多新的治疗方法。
原始出处:
作者:Allan
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#母细胞瘤#
100
#胶质母细胞#
75
#ASD#
84
#复发性#
61
#仿制药#
71