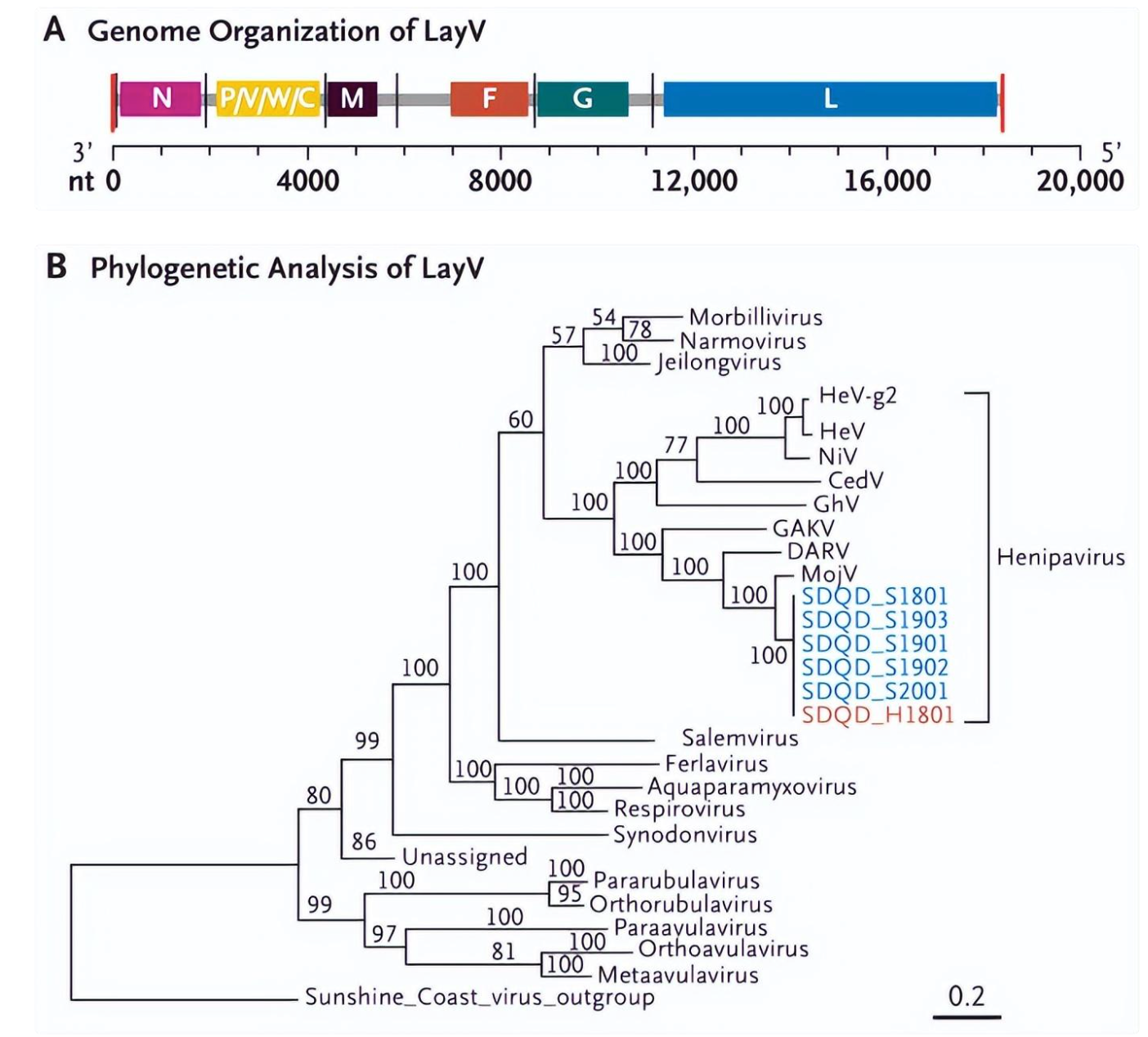
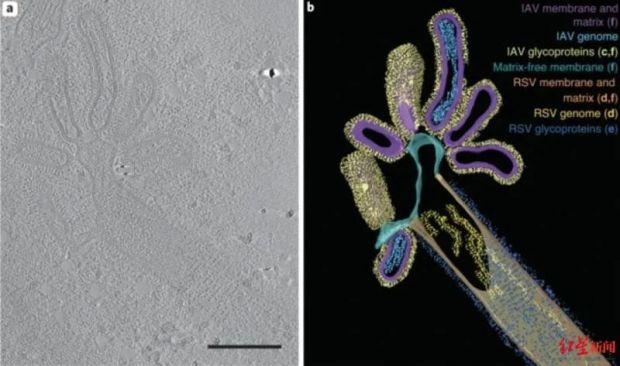
Cell:诺奖得主最新Cell论文:大量病毒存在CRISPR系统,从中挖掘更小更高效的Cas酶
2022-11-24 王聪 “生物世界”公众号
在噬菌体和细菌/古菌的“军备竞赛”中,究竟有多少噬菌体进化出了自己的 CRISPR-Cas 系统,目前还缺少系统性研究。
2012年6月28日,Jennifer Doudna、Emmanuelle Charpentier 等人在 Science 期刊发表了一篇具有划时代意义的论文[1]。揭示了 CRISPR-Cas 系统的详细作用机制,并指出了其作为基因组编辑工具的潜力。此后,在张锋、George Church、亓磊、刘如谦等人的推动下,CRISPR基因编辑技术快速发展,成为最简单高效的基因编辑工具,在基因功能研究、药物靶点筛选、遗传疾病治疗、癌症研究、作物育种等领域取得了突破性成就。
CRISPR-Cas 系统最为人所知的是它作为基因组编辑工具,但它实际上是在自然界中广泛存在的一类免疫系统。40%的细菌和85%的古菌具有 CRISPR-Cas 系统,这些原核生物可以捕获入侵病毒(噬菌体)或质粒的基因组片段,并将其存储到自己基因组中的CRISPR阵列中。当这些病毒再次入侵时,CRISPR阵列作为模板转录RNA,引导Cas酶切割入侵病毒的相应DNA,从而抵御入侵病毒。
有趣的是,病毒有时候也会“窃取”宿主细胞的基因组片段,如果这些被“窃取”的DNA能给病毒带来竞争优势,它们就可能被保留下来并逐渐修饰以更好地服务于病毒。例如,2013年的一篇 Nature 论文显示,一种感染霍乱弧菌的噬菌体就具有 CRISPR-Cas 系统,并用来逃逸霍乱弧菌的先天免疫系统[2]。
在噬菌体和细菌/古菌的“军备竞赛”中,究竟有多少噬菌体进化出了自己的 CRISPR-Cas 系统,目前还缺少系统性研究。
2022年11月23日,诺奖得主、CRISPR基因编辑先驱 Jennifer Doudna 等人在 Cell 期刊发表了题为:Diverse virus-encoded CRISPR-Cas systems include streamlined genome editors 的研究论文[3]。该研究在发现 CRISPR-Cas 系统的巨大多样性方面向前迈出了重要一步。
加州大学伯克利分校 Jennifer Doudna 实验室和 Jillian Banfield 实验室通过基因组解析宏基因组学对来自自然界、人类和动物的微生物组进行分析,从而全面研究噬菌体中的 CRISPR-Cas 系统,他们惊讶地发现了大约6000种具有 CRISPR-Cas 系统的噬菌体(占已知噬菌体的0.4%),涵盖了所有已知的六种 CRSIPR-Cas 系统类型(Ⅰ-Ⅵ型,例如Cas9属于Ⅱ型,Cas12属于Ⅴ型,Cas13属于Ⅵ型)。
重要的是,其中一些来自噬菌体的 Casλ 酶(属于Ⅴ型,仅700多个氨基酸大小)能够编辑植物和人类细胞基因组,并且兼顾了小型化和高编辑效率的优点。
该研究还发现,这些噬菌体中的 CRISPR-Cas 系统在结构上存在着广泛的变异,一些系统缺少组件,一些系统非常紧凑。即使携带 CRISPR-Cas 系统的噬菌体很罕见,但考虑到噬菌体的高度多样化和广泛分布,因此噬菌体 CRSIPR-Cas 系统的绝对数量将非常可观。这也提示了我们,大自然总是充满了惊喜。

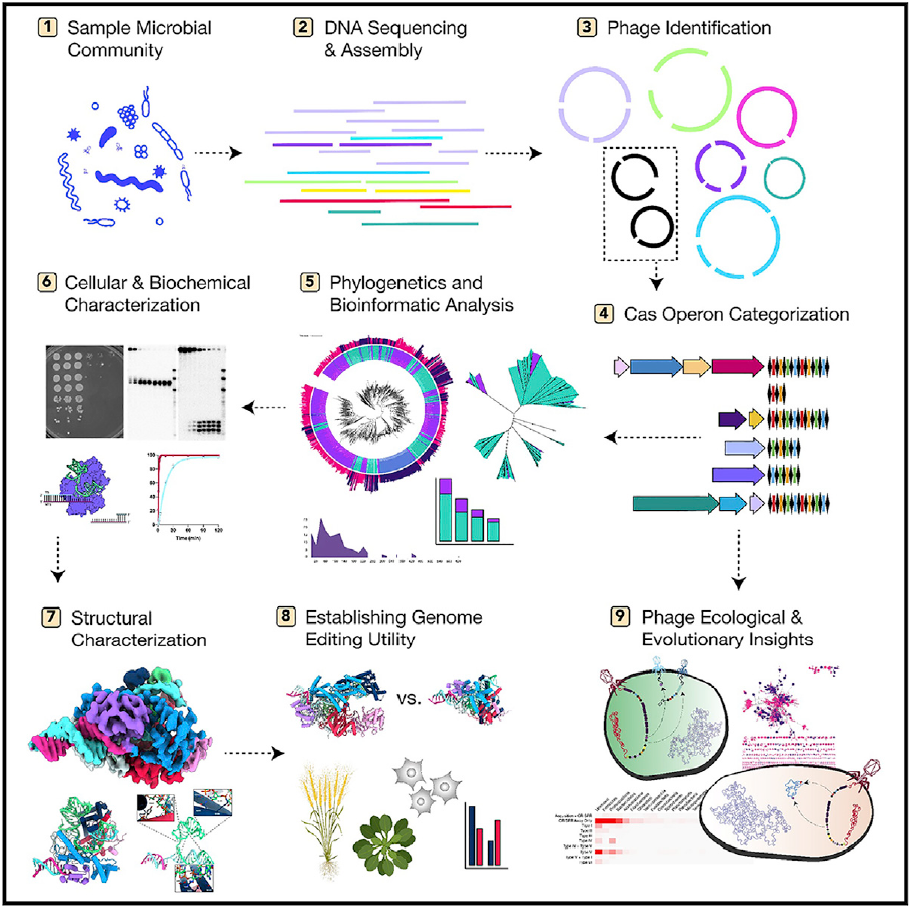
相对于细菌/古菌基因组,病毒(噬菌体)基因组要紧凑得多,因此,一些噬菌体的 CRISPR-Cas 系统很小,而小型化 CRSIPR-Cas 系统正是科学家们梦寐以求的。对于基因编辑而言,小型化系统可以被更好地通过腺相关病毒(AAV)载体进行递送,从而用于体内基因编辑。
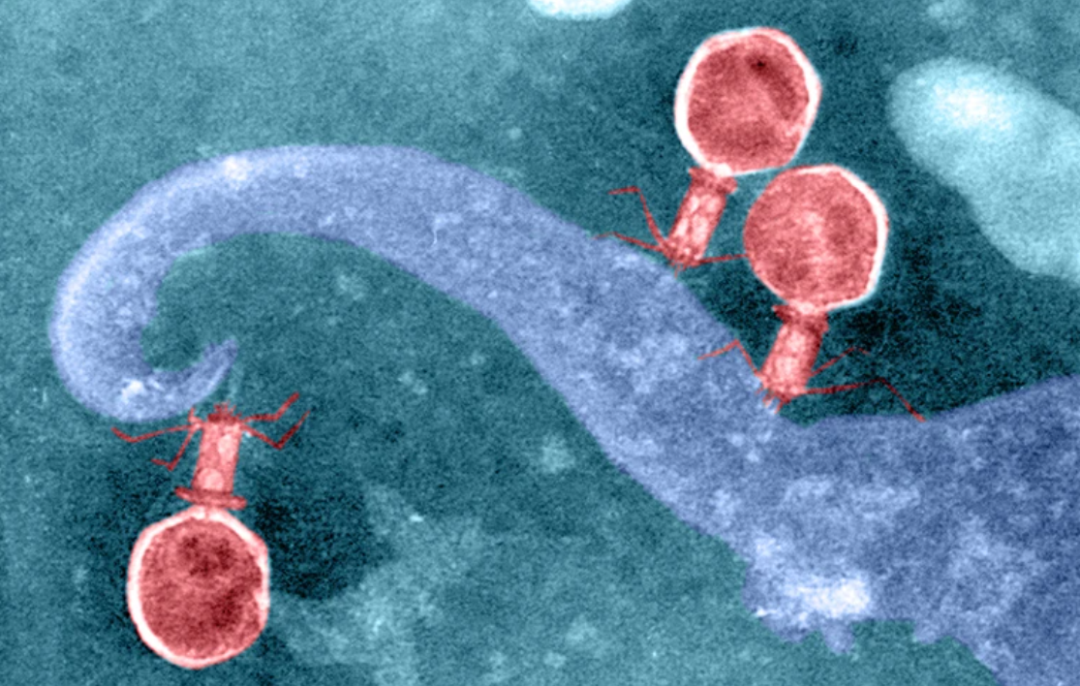
噬菌体
在该研究中,Jennifer Doudna 实验室专注于新发现的一类叫做的 Casλ 的小型化 Cas 酶,他们发现其中一些 Casλ 酶可以用来编辑拟南芥、小麦,以及人类细胞的基因组。
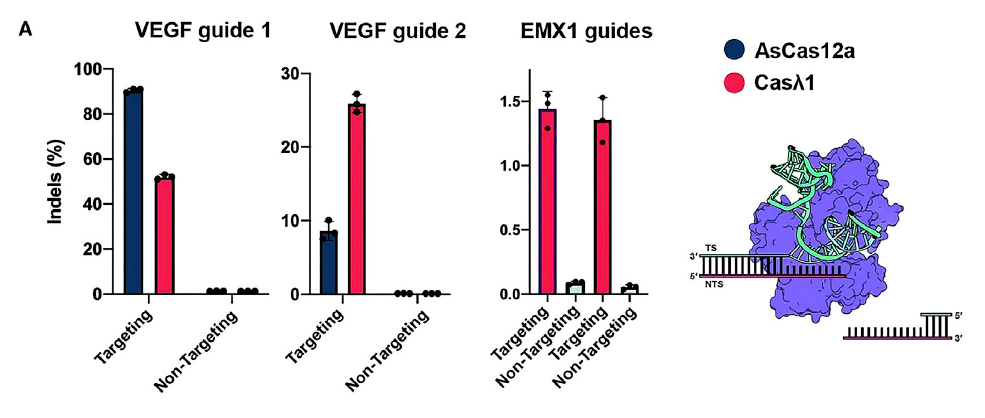
Casλ与Cas12a编辑人类细胞基因组的对比
近年来,许多研究团队致力于从自然界中的细菌和古菌中挖掘新型基因编辑工具,也发现了不少小型化的 Cas 酶,然而,迄今为止,这些新发现的小型化 Cas 酶通常在实际基因编辑应用中相对低效。相比之下,该研究中发现的一些来自噬菌体的 Casλ 酶具有小型化和高效率的双重优点。这些发现表明了病毒(噬菌体)是发现新型基因编辑工具的重要来源。
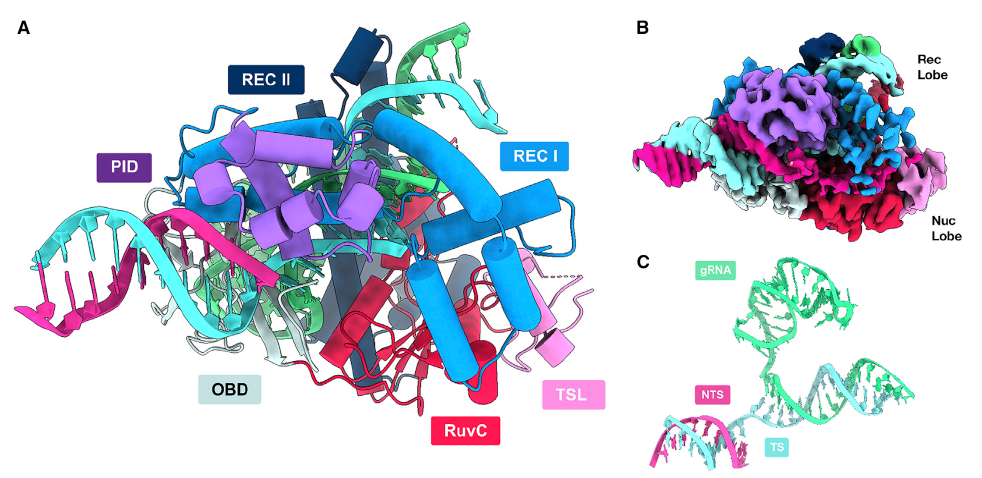
Casλ-gRNA-DNA复合物的结构
除了噬菌体外,质粒也是入侵细菌/古菌的遗传元件,因此,这些在微生物之间转移的质粒也可能会捕获宿主的 CRISPR-Cas 系统,它们也可能是发现新型 CRISPR-Cas 系统的源泉。
原始出处:
1) Seed K,Lazinski D,Calderwood S, et al. A bacteriophage encodes its own CRISPR/Cas adaptive response to evade host innate immunity. Nature 494, 489–491 (2013). https://doi.org/10.1038/nature11927.
2) MARTIN JINEK, KRZYSZTOF CHYLINSKI, INES FONFARA,et al. A Programmable Dual-RNA–Guided DNA Endonuclease in Adaptive Bacterial Immunity. SCIENCE, 28, Jun 2012, Vol 337, Issue 6096, pp. 816-821.
3) Basem Al-Shayeb, et al. Diverse virus-encoded CRISPR-Cas systems include streamlined genome editors. Cell, 2022.
作者:王聪
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言