易庆团队《自然·通讯》:发现LILRB1为多发性骨髓瘤治疗的新靶点
2024-07-17 BioMed科技 BioMed科技
该团队发现在MM细胞中,膜蛋白LILRB1通过协助MM细胞摄取低密度脂蛋白,维持细胞内胆固醇合成通路中具有抗氧化作用的代谢物角鲨烯的含量,从而保护MM细胞不发生铁死亡,促进多发性骨髓瘤的恶性进展。
多发性骨髓瘤(multiple myeloma, MM)是仅次于非霍奇金淋巴瘤的第二大常见血液系统恶性肿瘤,其特点是骨髓中浆细胞的恶性增殖。近几十年来,随着骨髓移植及蛋白酶体抑制剂等治疗手段的不断发展,MM病人的存活率有显著提高,但MM依然是不可治愈的疾病。2020年的统计数据显示,MM每年在全球范围内导致约10万人的死亡1。部分MM患者的病情进展迅速,存活时间短。而导致MM发生高危进展的机制尚未明确,需要进一步寻找在MM恶性进展中起到关键作用的基因及相关机制,以便开发新的MM治疗靶点。
2024年7月9日,康奈尔医学院&休斯顿卫理公会研究所的易庆团队在Nature communications期刊上发表题为Leukocyte immunoglobulin-like receptor B1 (LILRB1) protects human multiple myeloma cells from ferroptosis by maintaining cholesterol homeostasis的研究,为骨髓瘤的治疗发掘了全新靶点。该团队发现在MM细胞中,膜蛋白LILRB1通过协助MM细胞摄取低密度脂蛋白(LDL),维持细胞内胆固醇合成通路中具有抗氧化作用的代谢物角鲨烯(squalene)的含量,从而保护MM细胞不发生铁死亡,促进多发性骨髓瘤的恶性进展。
为了寻找MM潜在的治疗靶点,研究人员首先对比了预后良好(从诊断起存活时间≥4年)和预后不良(从诊断起存活时间<2年)的MM患者中MM细胞的基因表达谱(GEP),找到了超过7000个表达有显著差异的基因(P<0.05)。在预后不良的相关基因里,LILRB1是表达差异最为显著的基因之一。LILRB1在多种免疫细胞中介导了免疫抑制反应,但在肿瘤生物学中的作用及相关机制尚不明确。进一步的分析发现LILRB1在MM患者中的表达高于正常人体内浆细胞的表达,在MM Ⅲ期患者中的表达高于Ⅰ期患者,在复发性MM患者中的表达高于非复发性MM患者。这些结果都显示LILRB1的高表达与MM的恶性程度及病人的预后不良密切相关,是值得进一步研究的潜在治疗靶点。
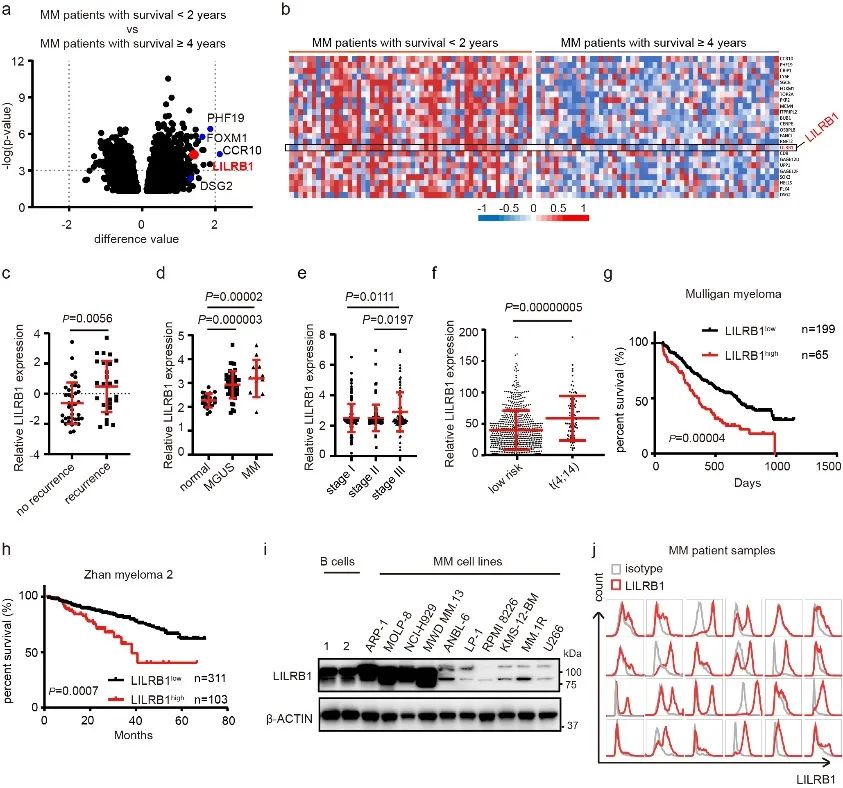
图一.LILRB1的高表达与多发性骨髓瘤病人的恶性进展和预后不良密切相关
随后,研究人员对LILRB1在MM中的作用进行了实验验证。实验结果发现,敲除(knock down,KD)LILRB1在体外并不引起明显的细胞凋亡,而在免疫缺陷小鼠体内能显著抑制肿瘤细胞的增长。同时,过表达LILRB1能促进MM细胞在免疫缺陷小鼠体内的增长。以上结果说明LILRB1能在肿瘤微环境的压力中保护多发性骨髓瘤细胞,并促进其存活和扩增。为进一步探索微环境中哪一类因素抑制了MM细胞的增殖,LILRB1又是通过影响哪些信号通路保护了MM细胞,研究人员将小鼠骨髓中的LILRB1-KD细胞和对照组CTR-KD细胞进行了RNAseq分析,发现敲除LILRB1会引起氧化应激的增强、脂质稳态的降低和LDL/胆固醇的减少,并且在LILRB1-KD细胞中铁死亡相关通路被激活。铁死亡是一种铁离子依赖的,由于脂质过氧化物堆积导致的细胞死亡2。进一步的实验表明,LILRB1-KD 细胞对铁死亡相关压力更加敏感;铁死亡抑制剂能够逆转LILRB1的敲除在体外和体内引起的细胞死亡。此外,LILRB1表达量低的MM原代细胞对铁死亡诱导剂更加敏感。这些实验结果说明,LILRB1能在肿瘤微环境中保护MM细胞,抑制MM细胞发生由脂质过氧化引起的铁死亡。
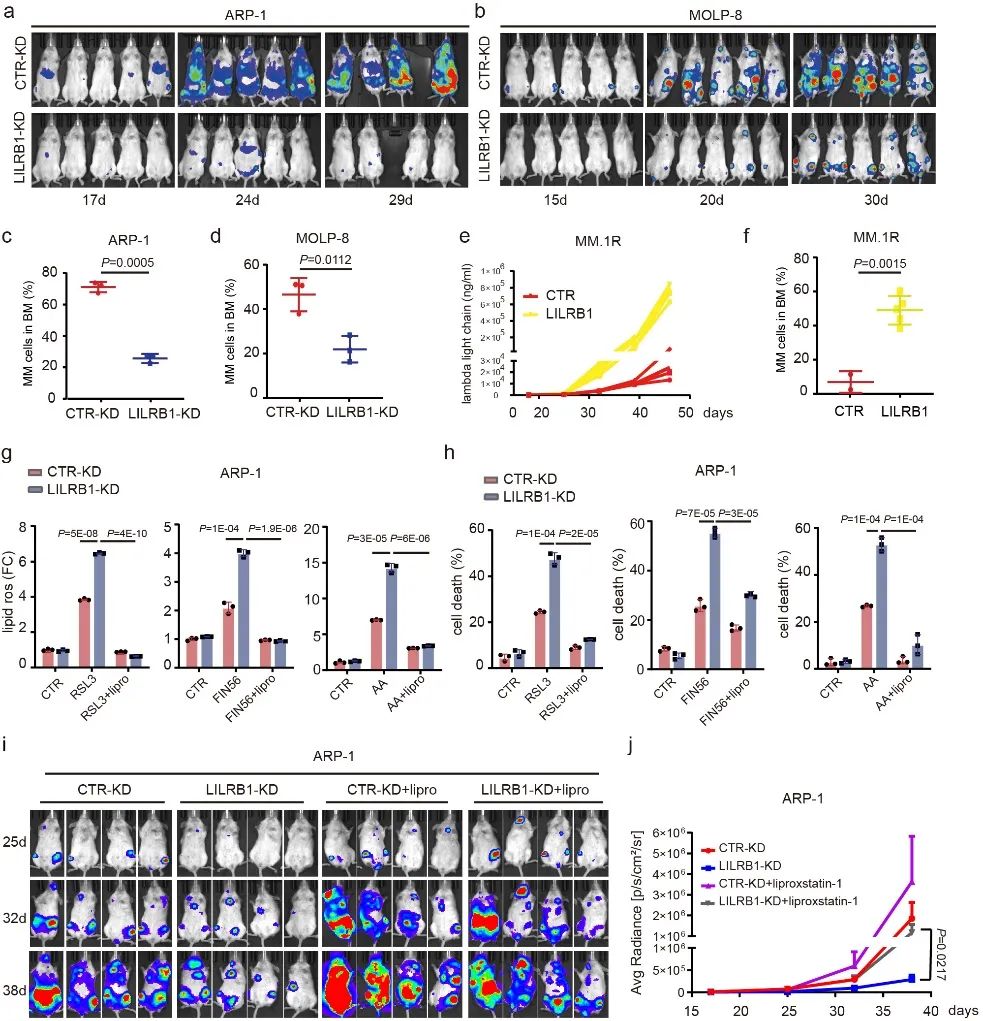
图二.LILRB1的敲除在体内和体外促进骨髓瘤细胞发生铁死亡
那么LILRB1是通过怎样的作用机制发挥了对MM细胞的保护作用呢?鉴于LILRB1已知的功能与铁死亡没有明确关联,研究人员推测:LILRB1会与其他蛋白结合发挥尚未被报道的功能。通过质谱分析,研究人员鉴定到了约300个可能与LILRB1结合的蛋白,结合RNAseq结果中脂质稳态和胆固醇相关通路的变化,将目光聚焦于与这些通路相关的蛋白low-density lipoprotein receptor adaptor protein 1 (LDLRAP1)。进一步的实验结果证明了LILRB1能够同时与low-density lipoprotein receptor(LDLR)和LDLRAP1结合,并能促进MM细胞对LDL的摄取。敲除LILRB1会导致LDLR与LDLRAP1结合的减弱,抑制MM细胞对LDL的摄取,扰乱MM细胞中的胆固醇代谢;同时,为了维持细胞中胆固醇的含量,LILRB1-KD MM细胞的反馈调节作用会激活胆固醇合成途径,引起胆固醇合成路径中的限速酶SQLE表达的上升;SQLE的底物是具有抗氧化作用的代谢物squalene,SQLE的升高导致MM细胞中squalene的含量下降,使MM细胞更容易发生铁死亡。
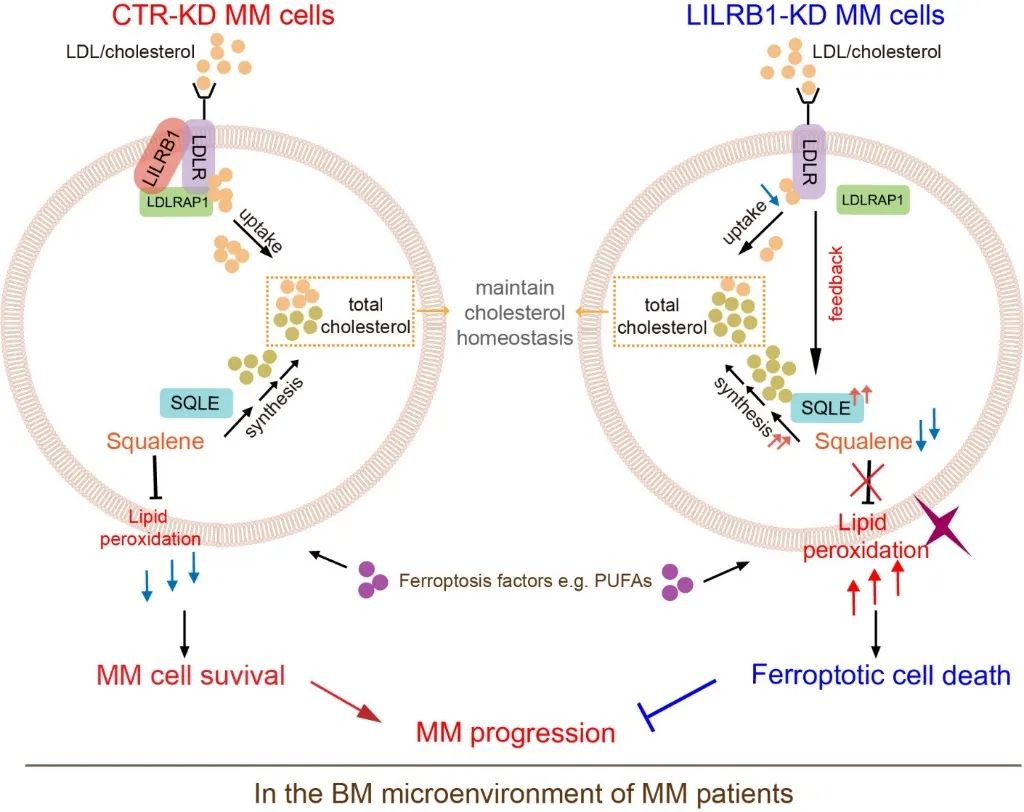
图三.LILRB1在骨髓瘤细胞中的功能及相关机制
综上,这项研究通过对MM病人临床数据的分析找到了在MM进展中有关键作用的蛋白LILRB1,并且发现了LILRB1在促进胆固醇摄取和抑制铁死亡中的全新功能及相关作用机制。LILRB1是在免疫细胞中被熟知的免疫抑制受体蛋白,但其在肿瘤细胞中所发挥的功能和相关机制未有深入研究和报道。易庆团队的研究发现了LILRB1能促进LDL/胆固醇的摄取、维持胆固醇稳态并抑制MM细胞发生铁死亡, 为LILRB1作为MM患者的全新治疗靶点提供了重要支撑数据,为MM患者治疗策略的进一步研究提供了新思路。
美国康奈尔医学院&休斯顿卫理公会研究所的鲜苗博士和王强博士为该论文的第一作者,易庆教授为该论文的通讯作者。
参考文献:
1、Siegel RL, Miller KD, Jemal A. Cancer statistics, 2020. CA Cancer J Clin 70, 7-30 (2020).
2、Dixon SJ, et al. Ferroptosis: an iron-dependent form of nonapoptotic cell death. Cell 149, 1060-1072 (2012).
原文链接:
https://www.nature.com/articles/s41467-024-50073-x
作者:BioMed科技
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#多发性骨髓瘤# #LILRB1#
69