Cell Stem Cell:发动造血干细胞的增殖“引擎”需要一关键分子
2016-06-28 佚名 生物谷
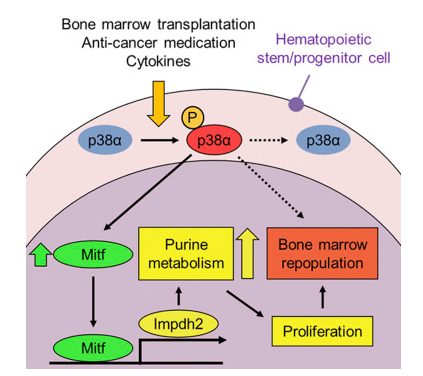
近日,来自日本的科学家们发现在骨髓移植等应激情况下,造血干细胞和祖细胞内(HSPC)的p38MAPK能够激活嘌呤代谢推动细胞进入细胞周期促进细胞增殖,从而对应激产生应答反应。该研究加深了人们对于造血应激情况下造血干细胞和祖细胞内代谢活动如何变化以及细胞增殖如何启动的认识。之前研究表明,在正常情况下造血干细胞通过激活糖酵解等一些特定代谢途径保持休眠状态,但是在骨髓移植等应激造血过程中,这些代谢活动如
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#Cell#
27
#stem cell#
33
#CEL#
33
#造血干细胞#
25
#STEM#
0