JNNP:面部运动与A型肉毒杆菌毒素结合对泰国成人面肌痉挛的健康相关生活质量的影响:一项随机对照交叉试验
2020-09-16 MedSci原创 MedSci原创
A型肉毒杆菌毒素(BTX-A)是治疗面肌痉挛(HFS)的一种选择,其短暂作用约为3-4个月。 注射后立即进行积极的肌肉锻炼可能会增强其功效。 一项针对面部运动异常的面部锻炼和BTX-A联合进行的小型随
A型肉毒杆菌毒素(BTX-A)是治疗面肌痉挛(HFS)的一种选择,其短暂作用约为3-4个月。 注射后立即进行积极的肌肉锻炼可能会增强其功效。 一项针对面部运动异常的面部锻炼和BTX-A联合进行的小型随机对照试验(RCT)报告说,面部肌肉痉挛的严重程度和频率并没有明显减少,但是,仅包括四名HFS患者。因此,作者进行了一项先导性,随机,交叉试验,以探讨面部运动与BTX-A注射相结合的的有效性和安全性 。
方法:治疗分为两组,成人面部运动联合BTX-A注射(治疗组A)与单独BTX-A注射(治疗组B),单中心,随机,交叉设计进行了HFS患者实验组。招募了每16周接受BTX-A定期治疗的18-80岁HFS的任何严重程度的参与者。排除标准为中风,眼睑痉挛,痴呆,失明,身体依赖性,服用抗凝药以及在视频指导下无法进行面部锻炼。符合条件的参与者被随机分组进行临床试验。两组均注射了肉毒杆菌毒素A。面部运动包括7分钟主动和被动面部肌肉挤压,注射BTX-A后在视频引导下立即进行一次。所有参与者均不得按摩,挤压或接受针灸治疗。主要评估结果是面肌痉挛评分30(HFS-30)。患者可以自行填写HFS-30表格。次要结果为患者报告的HFS高峰时间,作用持续时间。在每个16周治疗周期开始时和之后1个月收集基线HFS-30和三星医疗中心(SMC)等级。在每个治疗周期开始后1个月收集起效时间,不良事件(AE),并在每个16周治疗周期结束时收集起效时间。
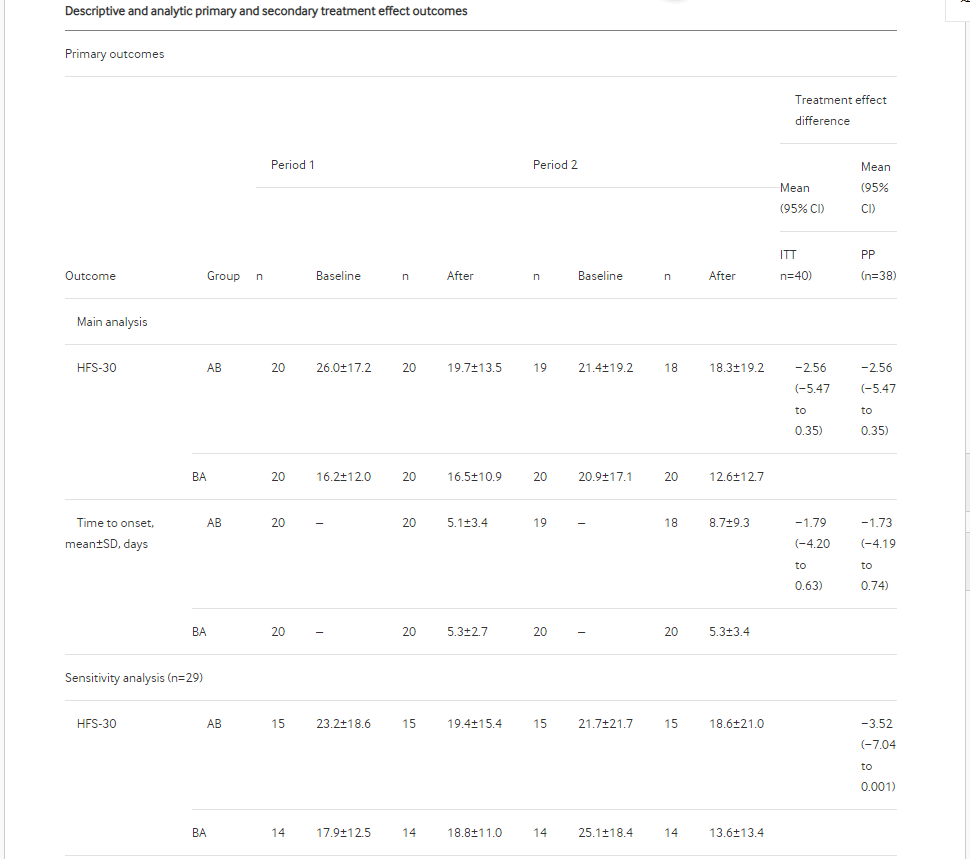
结果:筛选了42名参与者。 38名参与者完成了研究方案。治疗意向分析显示HFS-30得分的平均差异和起效时间分别为-2.56分(95%CI -5.47至0.35)和-1.79天(95%CI -4.20至0.626) 。 事后敏感性分析,该数据显示HFS-30得分的平均差异为-3.52分(95%CI -7.04至0.001)。峰期效应的治疗平均差为-1.98天(95%CI -4.88至0.92),持续时间为0.18周(95%CI -0.65至1.01)。治疗组之间的不良事件无显着差异,并且没有参与者因不良事件而退出
面部锻炼和BTX-A注射剂的结合治疗对成年HFS患者显示出有意义的帮助。
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







谢谢
40
#A型肉毒杆菌毒素#
48
#对照#
39
#面肌痉挛#
37
#痉挛#
48