Prostate:转移性前列腺癌相关的P62能够抑制自噬流和促进上皮间质转化
2018-02-18 AlexYang MedSci原创
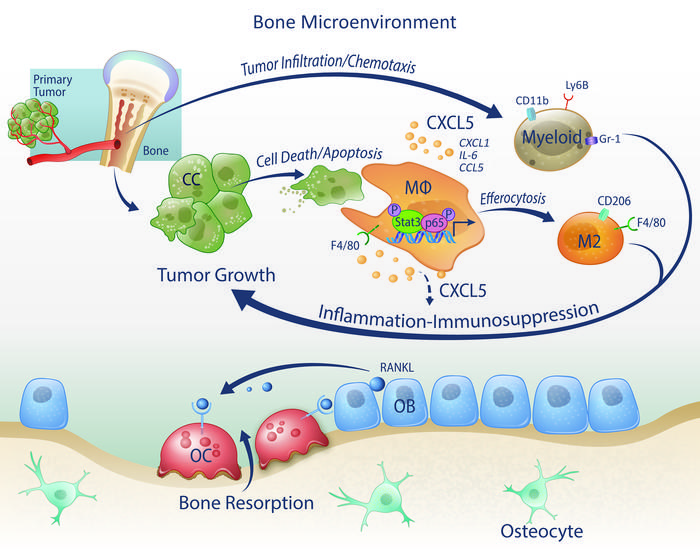
P62可以通过多种路径参与细胞自噬。P62在自噬体中与自噬体相关的LC3-II和泛素化蛋白聚合体互作从而吞噬聚合物,还可与HDAC6互作来抑制它的脱乙酰酶活性来维持乙酰化α-微管蛋白水平和微管的稳定性来增强自噬体转运,并且还可以调节自噬起始和细胞生存。最近,有研究人员在来源于前列腺癌病人的前列腺组织中进行了P62免疫组化染色,发现P62在患有前列腺腺癌(PCA)的病人中的水平要比那些患有良性前列腺
作者:AlexYang
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





#上皮间质转化#
74
#ROS#
79
#转移性#
63
#转移性前列腺癌#
72
#PRO#
78