Science子刊:上海交通大学张诗宜/罗洁等合作发现表皮生长因子受体抑制剂诱导皮疹的潜在机理及应对策略
2024-06-21 iNature iNature
该研究分析了暴露于EGFRi 阿法替尼(afatinib)的大鼠皮肤样本的高通量转录组测序,并确定角化细胞活化是EGFRi诱导皮疹的早期病理改变。
表皮生长因子受体抑制剂(EGFRis)用于治疗许多癌症,但由于可能出现严重的皮疹,其使用变得复杂,限制了其使用并对患者的生活质量产生不利影响。大多数关于EGFRis诱导的皮疹的研究都集中在这种皮肤病的完全发展阶段,早期病理变化尚不清楚。
2024年6月19日,上海交通大学张诗宜、罗洁及同济大学徐楠共同通讯在Science Translational Medicine 在线发表题为“Topical JAK inhibition ameliorates EGFR inhibitor–induced rash in rodents and humans”的研究论文,该研究分析了暴露于EGFRi 阿法替尼(afatinib)的大鼠皮肤样本的高通量转录组测序,并确定角化细胞活化是EGFRi诱导皮疹的早期病理改变。机制上,S100钙结合蛋白A9 (S100A9)的诱导发生在皮肤屏障破坏之前,并导致角质形成细胞活化,导致特异性细胞因子、趋化因子和表面分子如白细胞介素6 (Il6)和C-C基元趋化因子配体2 (CCL2)的表达,通过激活Janus激酶(JAK) -信号转导和转录激活因子(STAT)途径来招募和激活单核细胞,进一步招募更多的免疫细胞。
局部抑制JAK抑制了阿法替尼治疗的表皮EGFR缺失大鼠和小鼠的免疫细胞募集,改善了皮疹的严重程度,而对荷瘤小鼠的EGFRi效果没有影响。在一项试点临床试验(NCT05120362)中,11例EGFR诱导皮疹患者接受delgocitinib软膏治疗,根据MASCC EGFR抑制剂皮肤毒性工具(MESTT)标准,其中10例患者的皮疹严重程度至少改善了一级。这些发现为更好地理解EGFRi诱导的皮疹的早期病理生理学提供了帮助,并提出了一种治疗这种疾病的策略。

表皮生长因子受体(EGFR)的激活突变和过表达与多种癌症有关,这突出了EGFR作为抗癌治疗的重要分子靶点。EGFR抑制剂(EGFRis)是针对EGFR细胞外结构域的特异性抗体,或结合细胞内EGFR催化位点的小分子酪氨酸激酶抑制剂(TKIs)。
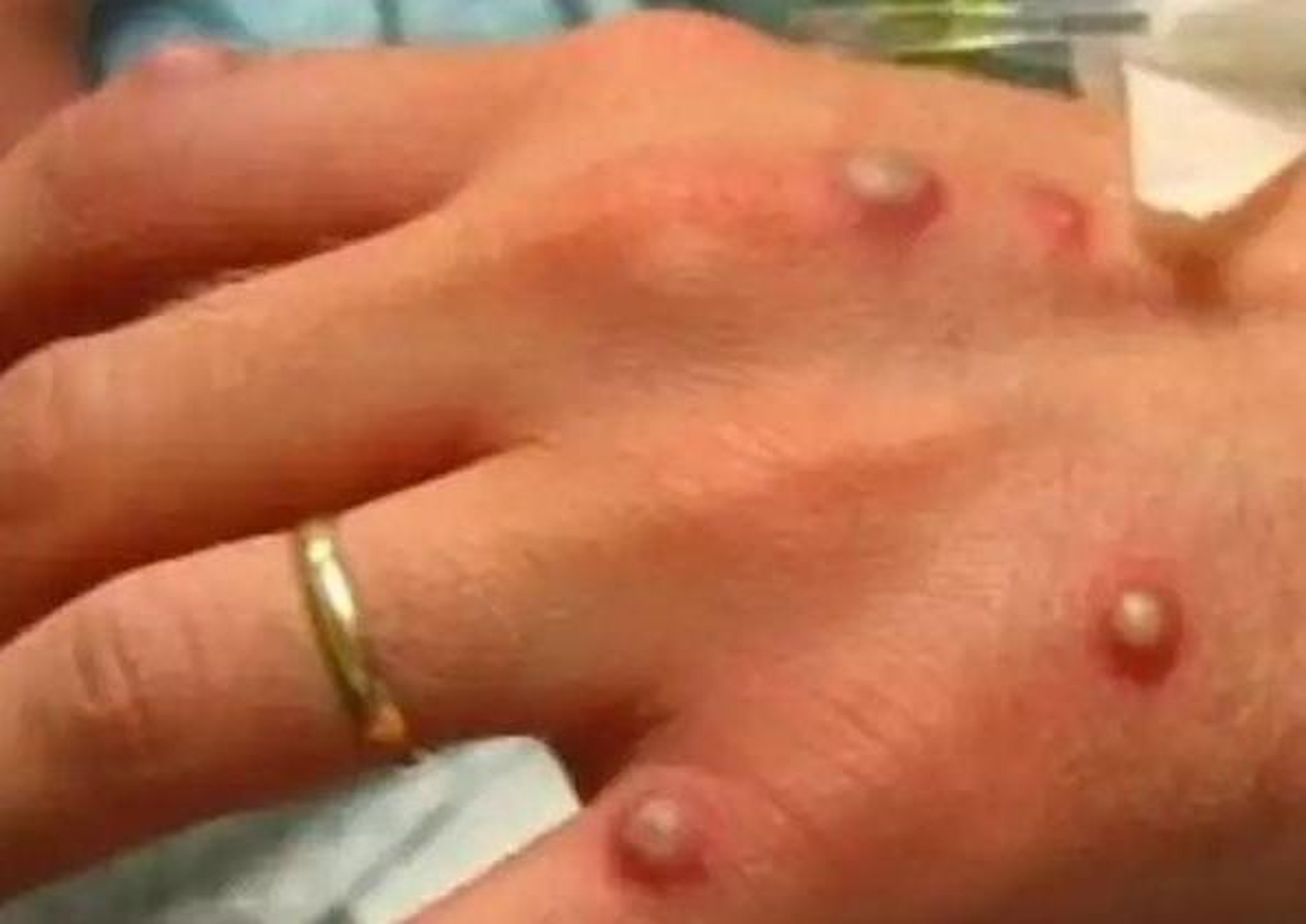
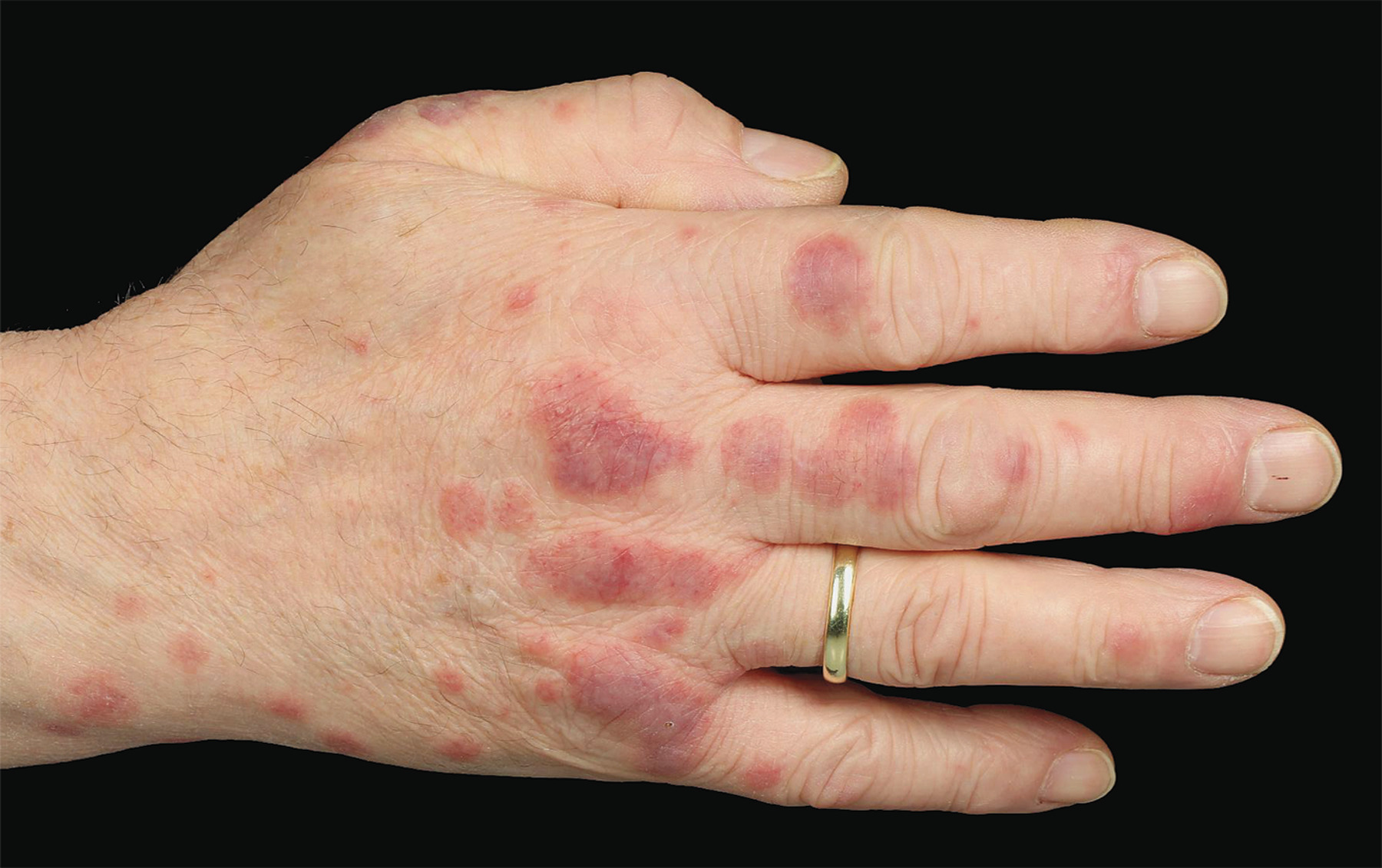
使用EGFRi治疗与皮肤毒性的频繁发生有关,特别是通常在EGFRi治疗后3至10天内出现丘疹;更频繁地影响面部、胸部和背部;可能疼痛或瘙痒;并可能伴有继发性细菌重复感染。EGFRi-诱导皮疹的发生率高达92.4%。EGFRi -诱导皮疹可引起患者身体和心理社会不适,需要停止治疗或减少剂量,最终可能对临床反应产生不利影响。
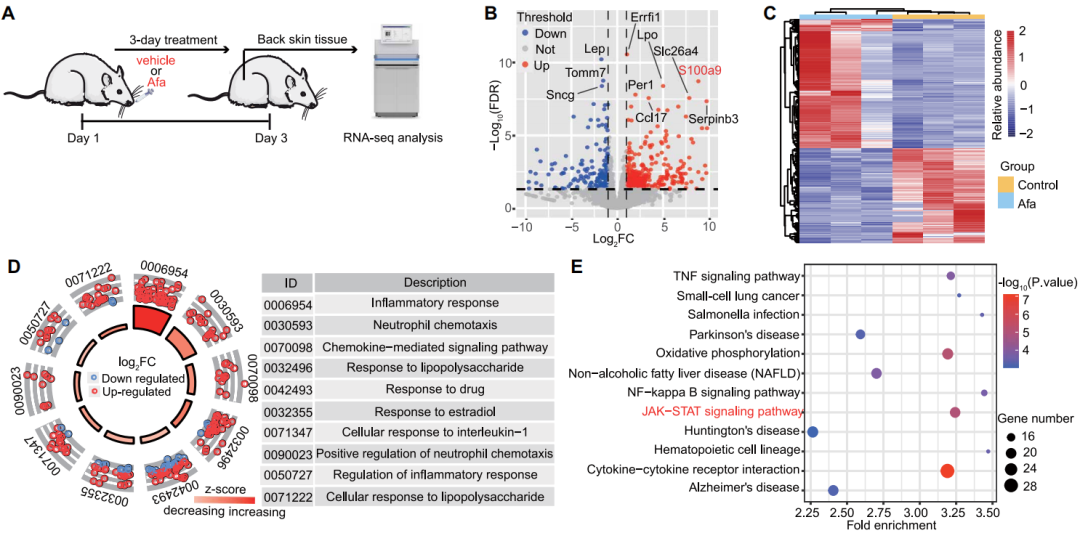
皮肤炎症是阿法替尼治疗大鼠的早期病理改变(图源自Science Translational Medicine )
大量的临床和实验数据表明,EGFRi诱导的皮疹是一种炎症性皮肤疾病。接受EGFRi治疗的患者皮肤样本显示大量免疫细胞浸润和炎症介质表达增加。用EGFRi或表皮中敲除EGFR处理的动物模型显示出类似的炎症性皮肤表型。角质形成细胞是表皮中表达EGFR的主要细胞类型。一些体外研究也表明,在角质形成细胞中阻断EGFR与趋化因子的表达增加有关,但炎症是皮肤病变的触发因素还是皮肤病变的继发反应尚不清楚。
经验疗法,如广谱抗生素、皮质类固醇或保湿剂,目前被用于治疗EGFRi引起的皮疹,但这些疗法的效果有限。为了设计出更有针对性、更有效的治疗方法,需要彻底了解EGFRi诱导皮疹发病机制。
以往的研究主要集中在EGFR抑制或缺乏引起的皮肤疾病的晚期。该研究通过对啮齿动物模型的高通量转录组学分析,探讨了EGFRi诱导皮疹的早期病理改变。在这些结果的基础上,该研究在啮齿动物模型和中试临床试验中评估了Janus激酶(JAK)抑制对EGFRi诱导皮疹的影响。
参考消息:
https://www.science.org/doi/10.1126/scitranslmed.abq7074
作者:iNature
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#皮疹# #表皮生长因子受体抑制剂#
36