喜讯!FDA加速批准安进BiTE免疫疗法Blincyto治疗儿科Ph-急性淋巴细胞白血病(ALL)
2016-09-02 佚名 生物谷
美国生物技术巨头安进(Amgen)BiTE免疫疗法Blincyto(blinatumomab)近日在美国监管方面传来喜讯,FDA加速批准Blincyto用于费城染色体阴性(Ph-)复发性或难治性前体B细胞急性淋巴细胞白血病(ALL)儿科患者的治疗。Blincyto是全球首个双特异性T细胞免疫疗法。之前,Blincyto已分别于2014年底和2015年底获美国FDA和欧盟EMA加速批准,用于费城染色
美国生物技术巨头安进(Amgen)BiTE免疫疗法Blincyto(blinatumomab)近日在美国监管方面传来喜讯,FDA加速批准Blincyto用于费城染色体阴性(Ph-)复发性或难治性前体B细胞急性淋巴细胞白血病(ALL)儿科患者的治疗。
Blincyto是全球首个双特异性T细胞免疫疗法。之前,Blincyto已分别于2014年底和2015年底获美国FDA和欧盟EMA加速批准,用于费城染色体阴性(Ph-)复发性或难治性前体B细胞急性淋巴细胞白血病(ALL)成人患者的治疗,这是儿童和成人群体中一种罕见、进展迅速的血液癌症。
此次批准,是基于一项I/II期单组临床研究Study 205的数据,该研究表明,Blincyto在具有临床意义数目的儿科费城染色体阴性(Ph-)复发性或难治性前体B细胞急性淋巴细胞白血病(ALL)患者诱导了完全缓解。该研究中,Blincyto在儿科群体中的严重不良事件与Blincyto已知的安全性一致。
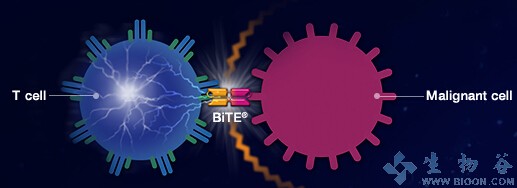
Blincyto(blinatumomab)是全球首个BiTE免疫疗法,基于安进最先进的双特异性T细胞衔接系统(BiTE)开发,这是一种双特异性抗体,能够通过将肿瘤细胞上的CD19蛋白呈递给T细胞特异表达的CD3蛋白,进而激活免疫系统识别并杀灭肿瘤细胞。
BiTE抗体技术代表了一种创新的免疫治疗方法,能够在很低浓度下起作用。安进于2012年耗资12亿美元收购Micromet公司后获得了BiTE技术。目前,安进正在广泛的难治性肿瘤类型中,探索BiTE创新疗法的潜力。此前,FDA和EMA均已授予blinatumomab治疗多种类型血液癌症的孤儿药地位及突破性疗法认定,包括急性淋巴细胞白血病(ALL)、慢性淋巴细胞白血病(CLL)、毛细胞白血病(HCL)、幼淋巴细胞白血病(PLL)和惰性B细胞淋巴瘤、套细胞白血病(MCL)等。
原始出处:
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#Blincyto#
45
#BiTE免疫疗法#
42
#淋巴细胞白血病#
45
#淋巴细胞#
41
#ALL#
29