南京传奇生物已暂停CAR-T疗法LB1901的I期临床试验
2022-02-17 Allan MedSci原创
南京传奇生物制药公司(Legend Biotech)近日表示,FDA 已告知该机构已暂停其自体 CAR-T 疗法 LB1901 的 I 期试验。
南京传奇生物制药公司(Legend Biotech)近日表示,FDA 已告知该机构已暂停其自体 CAR-T 疗法 LB1901 的 I 期试验。LB1901是该公司的自体嵌合抗原受体T细胞(CAR-T)治疗药物,用于治疗成人复发性或难治性T细胞淋巴瘤(TCL)。
根据传奇生物的说法,到目前为止,只有一名参与者被给药。它指出,即使在 FDA 就暂停事宜联系传奇生物之前,公司就因“患者外周血中 CD4+ T 细胞计数低”而暂停了试验,并通知了 FDA。传奇生物补充说:“患者没有经历过与药物相关的严重不良事件,并且正在按照协议进行监测”。该公司预计将在 3 月中旬左右收到 FDA 的正式通知。
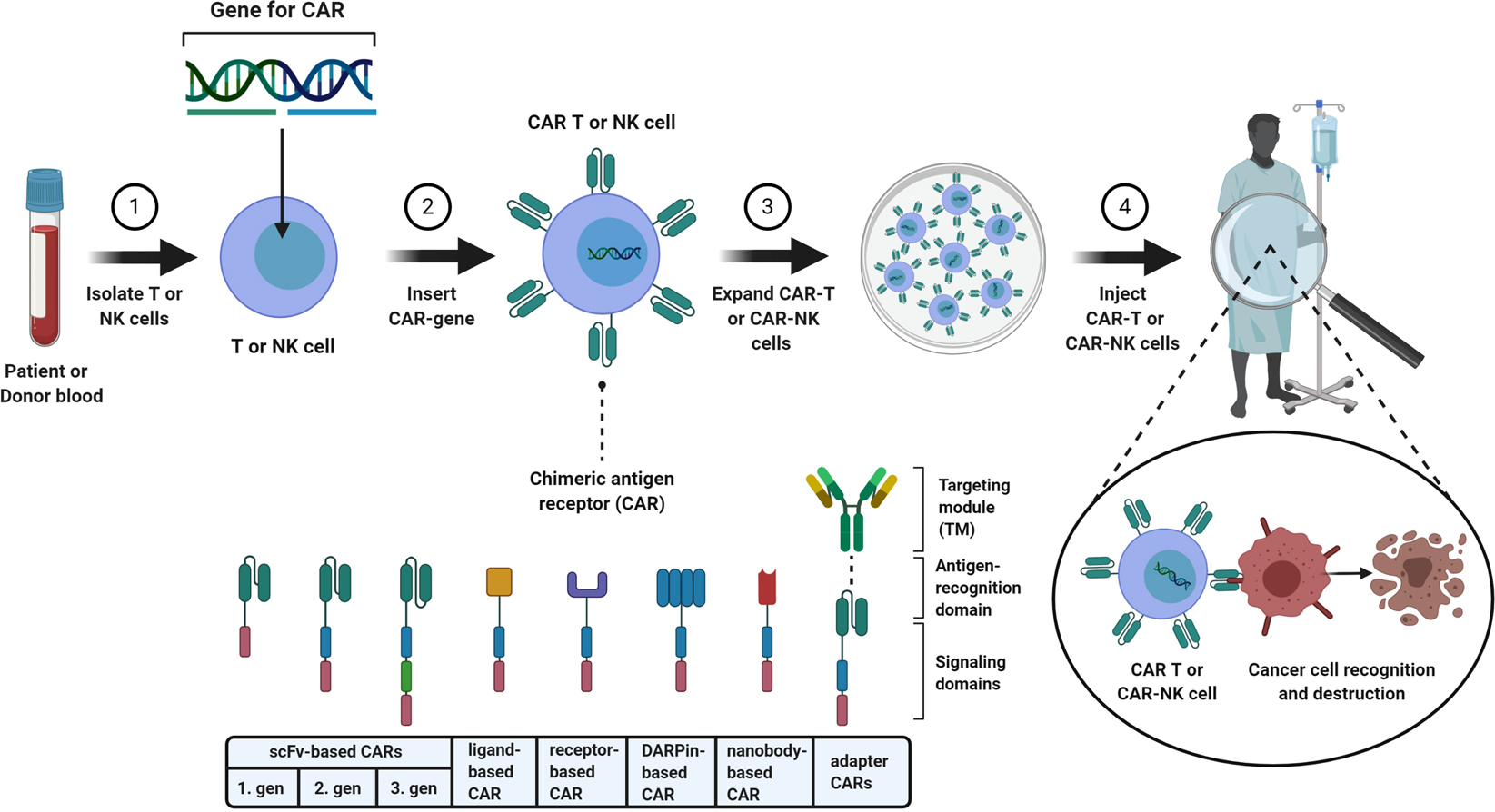
同时,传奇生物正在与强生合作开发靶向 BCMA 的 CAR-T 疗法ciltacabtagene autoleucel(cilta-cel)。
CAR-T 细胞疗法是一种用经特殊转化的 T 细胞来更特异性地靶向癌细胞的新免疫疗法。医生先从患者的血液中提取出 T 细胞,随后对这些 T 细胞进行基因改造,从而让这些 T 细胞膜的表面上生成嵌合抗原受体(CARs)的特殊结构。当这些 CAR-T 细胞被重新注射到患者体内时,这些受体就能够帮助 T 细胞识别、攻击人体内的癌细胞。尽管绝大多数的患者不会经历与化疗相关的常见副作用,如掉发、恶心、呕吐,但是接受 CAR-T 细胞疗法的患者有可能会经历严重的副作用,如细胞因子释放综合征(Cytokine release syndrome)和神经毒性。
原始出处:
作者:Allan
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#I期临床试验#
86
#CAR-#
77
#I期临床#
0
因外周血中CD4+Tcell计数减少而暂停试验
75
新的疗法已经在见证奇迹,安全探索,造福人类。
68