Lancet Rheumatol:托珠单抗生物类似药 BAT1806/BIIB800 对甲氨蝶呤反应不足的中重度类风湿性关节炎患者安全有效
2024-01-27 MedSci原创 MedSci原创
BAT1806/BIIB800在对甲氨蝶呤反应不足的中至重度类风湿关节炎患者中的临床Ⅲ期研究结果近日在国际风湿病学领域顶级期刊The Lancet Rheumatology《柳叶刀-风湿病学》(影响因
BAT1806/BIIB800在对甲氨蝶呤反应不足的中至重度类风湿关节炎患者中的临床Ⅲ期研究结果近日在国际风湿病学领域顶级期刊The Lancet Rheumatology《柳叶刀-风湿病学》(影响因子IF = 25.4)上发表。北京协和医院风湿免疫科冷晓梅教授为本文章的第一作者,北京协和医院风湿免疫科曾小峰教授为通讯作者。
文章发表的研究结果来自一项全球多中心、随机、双盲、阳性对照的Ⅲ期临床研究(ClinicalTrials.gov,NCT03830203;EudraCT,2018-002202-31)中初始治疗期(TP1)的结果。该研究在全球5个国家(中国、乌克兰、波兰、格鲁吉亚、保加利亚),共54家中心开展,其中包括24周的初始治疗期(TP1)和随后24周的二次治疗期(TP2)。
一共621例对甲氨蝶呤反应不足的中至重度类风湿关节炎患者被纳入研究。试验期间对受试者进行试验药物治疗,起始剂量为8mg/kg,每4周静脉输注一次BAT1806/BIIB800或原研托珠单抗。试验分为2个治疗阶段(TP1和TP2),在TP2阶段50%的对照组受试者转为接受BAT1806/BIIB800治疗至第48周。主要终点为第12周(欧洲EMA要求)或第24周(美国FDA和中国NMPA要求)达到ACR20的患者比例。使用预先指定的等效范围来计算临床等效性(欧洲EMA:95% CI-14.5% ~ +14.5%;美国FDA:90% CI-12.0% ~ +15.0%;中国NMPA:95% CI-13.6% ~ +13.6%);使用国际人用药品注册技术协调会(ICH)E9(R1)指导原则以及应对并发事件的策略来评估疗效差异。
在本次The Lancet Rheumatology报道的TP1结果中, BAT1806/BIIB800与原研托珠单抗疗效等效。
-
在TP1阶段,309例受试者被分配至原研托珠单抗组,312例受试者被分配至BAT1806/BIIB800组。
-
第12周时,原研托珠单抗组和BAT1806/BIIB800组的ACR应答率分别为64.8%和69.0%(疗效差异4.1%,95% CI -3.6 ~ 11.9);第24周时,原研托珠单抗组和BAT1806/BIIB800组的ACR应答率分别为67.9%和69.9%(疗效差异1.9%,90% CI -4.0 ~ 7.9,95% CI -5.2 ~ 9.1)。所有置信区间均落在预先指定的等效范围内(图2)。
-
在TP1阶段,BAT1806/BIIB800在缓解疾病活动度方面(DAS28)与原研托珠单抗也高度相似(图3)。
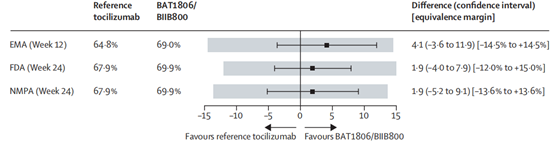
图2. 监管机构指定时间节点 (EMA:第12周;FDA、NMPA:第24周)的ACR20应答率(主要终点)
注:灰色框表示每个监管机构指定的等效范围
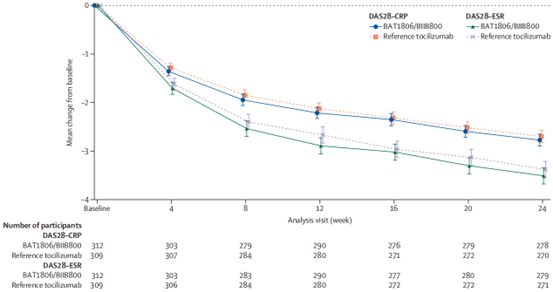
图3. DAS28-ESR和DAS28-CRP相对于基线的平均值(95% CI)随时间推移的变化(全分析集)
此外, 该国际多中心临床研究也观测到BAT1806/BIIB800与对照的原研托珠单抗具有可比的安全性、免疫原性和药代动力学等。该研究的TP2阶段的相关结果的单独发表也在进行中。
本研究证明了托珠单抗生物类似药BAT1806/BIIB800与原研托珠单抗相比,对于甲氨蝶呤反应不足的活动性类风湿关节炎患者具有相似的疗效、安全性、免疫原性和药代动力学特征,为该药物在国内和国外其他国家和地区的获批上市提供了重要的证据。
施瑞立®(BAT1806/BIIB800)(美国商品名:TOFIDENCE™)是国内首个获NMPA批准上市的托珠单抗生物类似药,也是第一个由中国本土药企自主研发、生产且获得美国FDA上市批准的单克隆抗体药物。
关于施瑞立®(TOFIDENCETM)
施瑞立®(TOFIDENCE™)(托珠单抗)是一款由百奥泰参照雅美罗®(托珠单抗)开发的生物类似药,是一款靶向白介素-6受体(IL-6R)的重组人源化单克隆抗体,可与可溶性及膜结合型IL-6受体(sIL-6R和mIL-6R)特异性结合,并抑制由sIL-6R和mIL-6R介导的信号传导。
2023年1月,施瑞立®获得中国NMPA批准上市,获批适应症为类风湿关节炎(RA)、全身型幼年特发性关节炎(sJIA)、细胞因子释放综合征(CRS)。
2023年9月,TOFIDENCE™获得美国FDA批准上市,成为美国首款托珠单抗生物类似药,同时也是第一个由中国本土药企自主研发、生产且获得美国FDA上市批准的单克隆抗体药物,获批适应症为类风湿关节炎(RA)、多关节型幼年特发性关节炎(pJIA)和全身型幼年特发性关节炎(sJIA)。
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#类风湿关节炎# #甲氨蝶呤# #托珠单抗# #生物类似药# #曾小峰#
33
谢谢分享
24