FDA加速批准非共价BTK抑制剂pirtobrutinib上市,用于复发或难治性套细胞淋巴瘤
2023-01-28 MedSci原创 MedSci原创
1月27日,礼来宣布,美国FDA加速批准Jaypirca(pirtobrutinib, 100mg和50mg片剂)上市,用于既往接受过至少二线系统治疗的复发或难治性套细胞淋巴瘤(MCL)成人患者,包括
1月27日,礼来宣布,美国FDA加速批准Jaypirca(pirtobrutinib, 100mg和50mg片剂)上市,用于既往接受过至少二线系统治疗的复发或难治性套细胞淋巴瘤(MCL)成人患者,包括布鲁顿酪氨酸激酶(BTK)抑制剂。Jaypirca是FDA批准的首个也是唯一一款非共价(可逆)BTK抑制剂。
目前临床上已有多款BTK小分子抑制剂上市,如伊布替尼等。但是,现有上市BTK抑制剂主要是通过与BTK活性位点的半胱氨酸残基形成共价键产生酶抑制作用,然而共价结合易产生耐药突变,成为临床治疗中的一大问题。C481S突变是第一代不可逆BTK抑制剂已知的耐药机制。
Jaypirca是一种口服有效和可逆的高选择性BTK抑制剂,既能抑制野生型也能抑制C481S突变型BTK。可以在先前使用共价BTK抑制剂(伊布替尼, 阿卡替尼或泽布替尼)治疗的MCL患者中重建BTK抑制,并延长靶向BTK途径的益处。
FDA此项批准是基于一项代号为BRUIN的开放标签,单臂,国际,I/II期研究的缓解率数据。120例接受Jaypirca(200mg,每日1次)治疗MCL患者的客观缓解率(ORR)为50%,完全缓解率(CR)为13%。
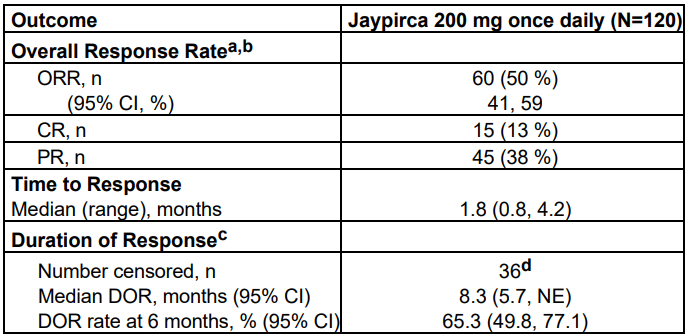
在全部BRUIN研究人群(583例恶性血液病患者)中评估了每日服用Jaypirca(200mg)作为单一药物的安全性。在汇总的安全性分析人群中,Jaypirca治疗最常见(≥20%)的不良反应(ARs)包括中性粒细胞计数降低、血红蛋白降低、血小板计数降低、疲劳、肌肉骨骼疼痛、淋巴细胞计数降低、挫伤和腹泻。
美国City of Hope医院血液学和造血干细胞移植系淋巴瘤科临床副教授 Tycel Phillips 医学博士讨论了 FDA 批准 pirtobrutinib (Jaypirca) 在套细胞淋巴瘤 (MCL) 中的意义。
2023 年 1 月 27 日,FDA 批准pirtobrutinib用于先前接受过 BTK 抑制剂治疗的 MCL 患者。 监管决定是基于 1/2 期 BRUIN 试验 (NCT03740529) 的结果,该试验研究了该药物作为一种单一疗法,每天一次的剂量为 25 毫克、50 毫克、100 毫克、150 毫克、200 毫克、250 毫克、 和 300 毫克。
在 BRUIN 中,pirtobrutinib在 BTK 预处理患者和 BTK 初治患者中的总缓解率 (ORR) 分别为 51% 和 82%。 此外,在既往接受过干细胞移植的患者中,ORR 为 64%,而在接受过 CAR T 细胞治疗的患者中,ORR 为 50%。 反应也很持久,60% 的反应患者在中位随访 8.2 个月时经历持续反应。
Phillips 说,未经 BTK 治疗的人群获得的 ORR 与使用共价 BTK 抑制剂依鲁替尼 (Imbruvica)、acalabrutinib (Calquence) 和 zanubrutinib (Brukinsa) 时的反应率相似,具有良好的毒性特征。 所有剂量和队列中任何级别的常见不良反应包括疲劳、腹泻、中性粒细胞减少和挫伤。 没有报告剂量限制性毒性,也没有达到最大耐受剂量。 此外,Phillips 指出,该药物在接触 BTK 的人群中引起了强烈的反应,这在历史上几乎没有有效和可获得的选择。
Phillips 解释说,在 pirtobrutinib 获批之前,BTK 难治性 MCL 患者唯一获批的选择是 brexucabtagene autoleucel (Tecartus),这是一种 CAR T 细胞产品。 由于 CAR T 细胞疗法通常需要在特定的医疗中心才能实施,而这款药物可以在所有的肿瘤治疗中心进行治疗。
目前确证性3期临床试验正在招募中 (NCT04662255; BRUIN MCL-321) 。
现在,Pirtobrutinib在礼来手中大放异彩;彼时,也曾经历多次辗转。Pirtobrutinib原名RXC005,最早由Redx Pharma研发,2017年公司濒临破产,无奈以4000万美元的价格出售RXC005的全部权益。Loxo Oncology则是那个眼光独到的买主,RXC005随之更名为LOXO-305。2019年初,礼来80亿美元现金收购了Loxo Oncology,囊获Pirtobrutinib在内的一系列肿瘤新药。
2022年,礼来与信达生物深化合作,后者收获Pirtobrutinib未来在中国大陆商业化权利的优先谈判权,可见实力者从不乏拥趸。
参考资料:
https://www.onclive.com/view/dr-phillips-on-the-fda-approval-of-pirtobrutinib-in-mcl
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#FDA#加速批准非共价#BTK抑制剂##pirtobrutinib#上市,用于复发或难治性#套细胞淋巴瘤#,相信适应症会快速扩展。 百悦泽(#泽布替尼#)适应症包括既往至少接受过一种治疗的#套细胞淋巴瘤#(MCL)、#慢性淋巴细胞白血病#/#小淋巴细胞淋巴瘤#(CLL/SLL)和#华氏巨球蛋白血症#(WM)成人患者。
101