Diabetes 空军军医大学西京医院孙冬冬教授团队揭示Rnd3在糖尿病心肌微血管损伤中的作用及机制
2025-01-16 论道心血管 论道心血管
该研究揭示了Rnd3在糖尿病心肌微血管损伤中的关键作用及调控机制。
糖尿病是一种常见的慢性代谢性疾病,其对心血管系统的危害日益受到关注。心肌微血管损伤是糖尿病引起心血管并发症的重要病理生理基础之一,内皮功能障碍是其主要特征。由于糖脂代谢紊乱、胰岛素抵抗等因素的影响,糖尿病患者的心肌微血管内皮细胞功能受损,导致血管舒张功能障碍、血管通透性增加、血小板聚集和血栓形成等一系列病理变化。这些变化会进一步加重心肌缺血缺氧,导致细胞损伤和死亡,最终影响心脏功能。然而,关于糖尿病心肌微血管损伤的病理机制仍未完全阐明。
2025年1月10日,空军军医大学西京医院孙冬冬教授团队在国际糖尿病领域经典期刊Diabetes (中科院一区Top期刊)发表了题为“Rnd3 Ameliorates Diabetic Cardiac Microvascular Injury via Facilitating Trim40-mediated Rock1 Ubiquitination”的原创研究,揭示了Rnd3在糖尿病心肌微血管损伤中的关键作用及调控机制。

作者通过分析GEO数据库(GSE213337)的单细胞RNA测序数据,发现链脲佐菌素诱导的1型糖尿病小鼠心肌内皮细胞中Rnd3表达显著降低。这一结果在高脂饮食和低剂量链脲佐菌素诱导的2型糖尿病小鼠模型及瘦素受体敲除(db/db)小鼠的心肌微血管内皮细胞中也得到了验证。
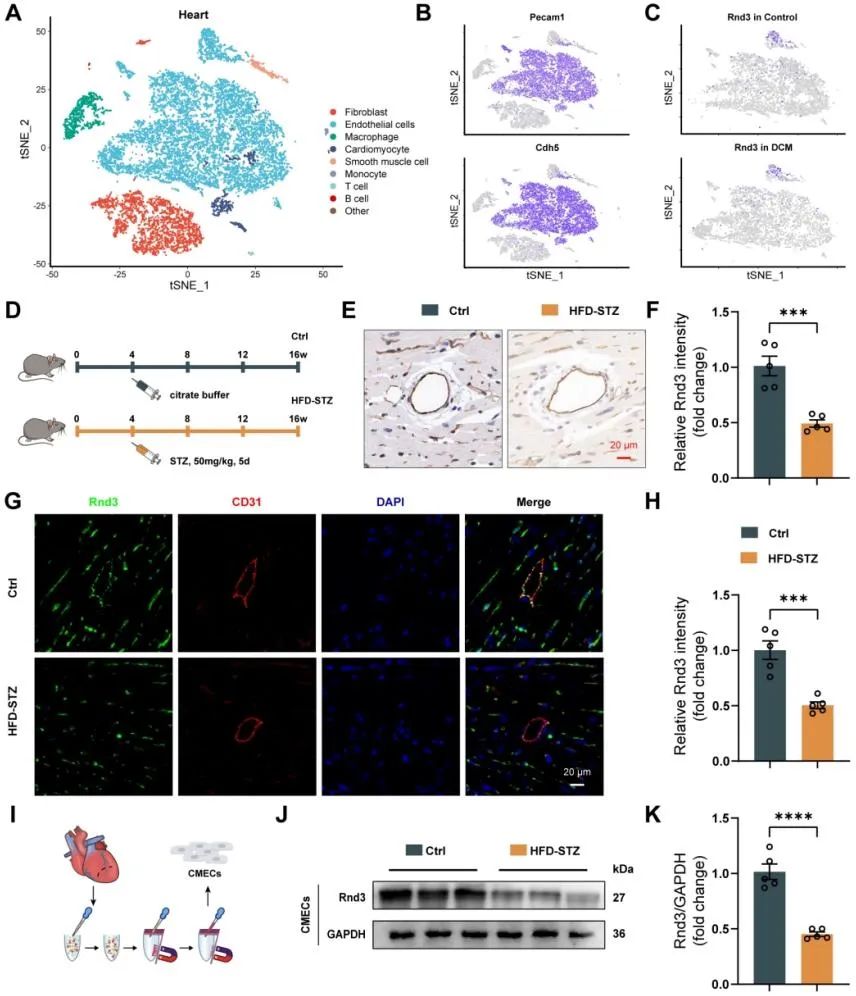
作者利用内皮细胞特异性Rnd3基因过表达(Rnd3-Tg)小鼠和Rnd3基因敲除(Rnd3-/-)小鼠构建2型糖尿病模型,发现Rnd3过表达显著减轻糖尿病引起的心肌微血管功能障碍,而Rnd3敲除则加重了损伤。
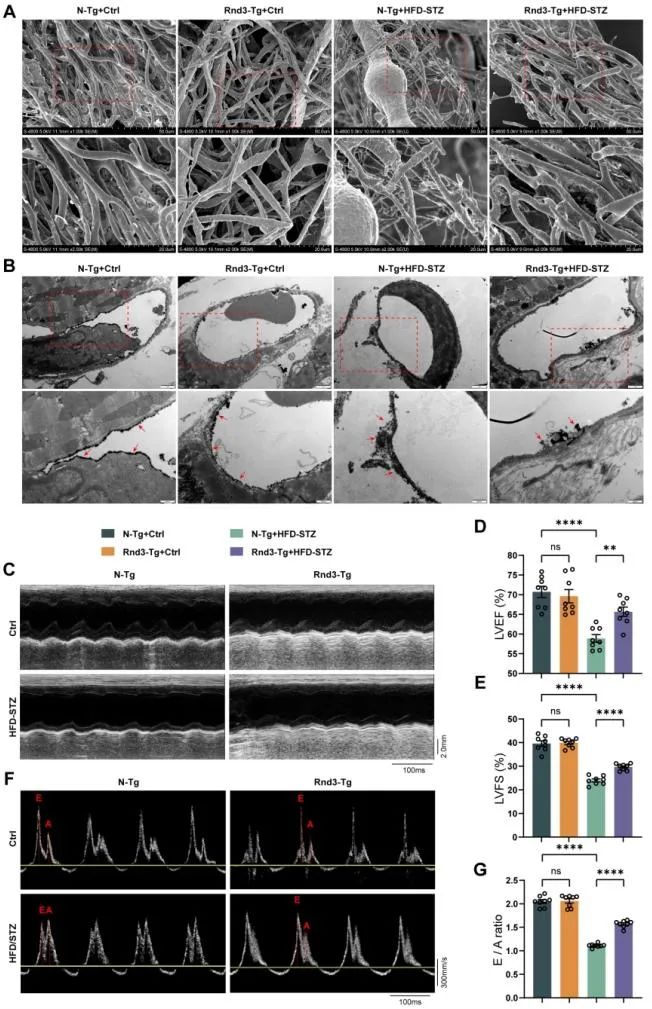
作者提取原代小鼠微血管内皮细胞(CMECs)进行机制研究,发现Rnd3通过抑制Rho-GTPases信号通路,降低Rock1的表达以及肌球蛋白轻链(MLC)磷酸化水平,从而减轻糖尿病导致微血管内皮细胞的高通透性。此外,免疫共沉淀和分子对接实验表明,Rnd3能够与Trim40结合,促进Rock1泛素化降解。同时,抑制Trim40则会抵消Rnd3过表达对糖尿病心肌微血管内皮细胞的保护作用。
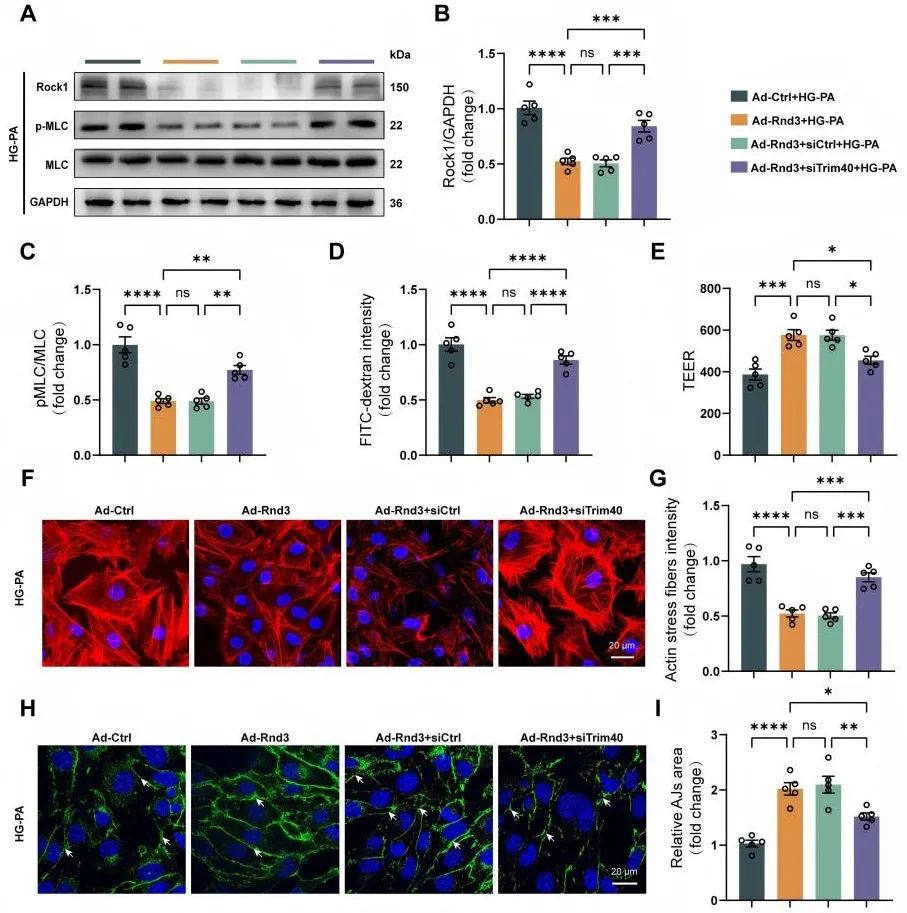
综上,本研究通过体内与体外实验相结合,从整体到分子水平全面揭示了Rnd3在糖尿病心肌微血管损伤中的作用及分子机制,为探索糖尿病心肌病的潜在治疗靶点提供了重要依据。
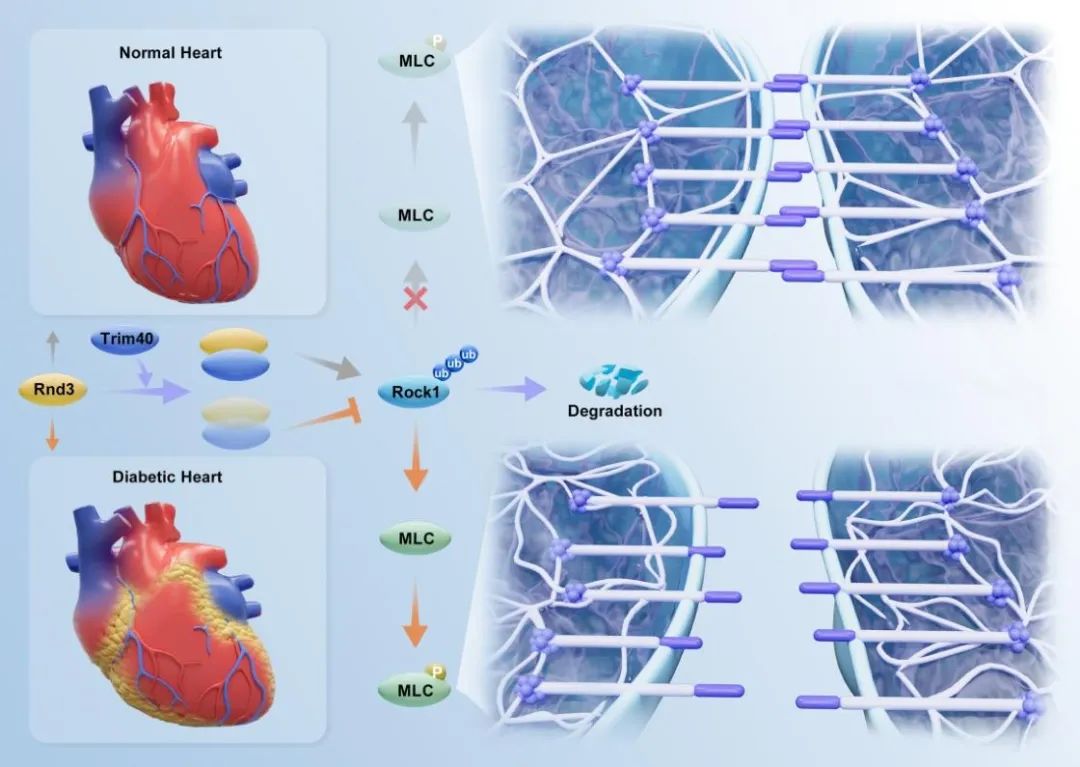
空军军医大学西京医院孙冬冬教授为本研究的独立通讯作者,蔺杰助理研究员、硕士研究生张学斌、葛闻为共同第一作者。
原文链接:
https://doi.org/10.2337/db24-0543
作者:论道心血管
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#糖尿病# #心肌微血管损伤#
5