WJG:抗病毒治疗对肝脏肿瘤形成和肝癌再发的影响
2014-02-13 佚名 丁香园
治疗用抗病毒药物如作为核苷(酸)类似物(Nucs)或干扰素(IFN)-α可以迅速抑制HBV复制,从而减少纤维化的进展和HCC的发生。虽然局部或全身的化疗可以治疗肿瘤,但手术切除或肝移植仍是治疗HCC的最有效方法。术后HCC复发是常见的现象。预防乙肝相关性肝癌的发生和复发需要接受综合性治疗,这一观点已得到广泛的认识。 因此,来自南京医科大学附属第一医院的研究人员综述了HBV诱导肝癌的机制,讨论
治疗用抗病毒药物如作为核苷(酸)类似物(Nucs)或干扰素(IFN)-α可以迅速抑制HBV复制,从而减少纤维化的进展和HCC的发生。虽然局部或全身的化疗可以治疗肿瘤,但手术切除或肝移植仍是治疗HCC的最有效方法。术后HCC复发是常见的现象。预防乙肝相关性肝癌的发生和复发需要接受综合性治疗,这一观点已得到广泛的认识。【原文下载】
因此,来自南京医科大学附属第一医院的研究人员综述了HBV诱导肝癌的机制,讨论了抗HBV治疗的趋势,及其预防肝癌的发生及复发的作用。该综述发表在2013年12月的《世界胃肠道杂志》(World journal of Gatraoenterology)上。
摘要
慢性乙型肝炎病毒(HBV)感染是肝脏疾病进展的关键因素,可以导致肝功能不全,肝硬化和肝细胞癌(HCC)。治疗的主要目的是抑制或消除HBV的复制,减少肝炎的活动,从而减少或减缓肝脏疾病的进展。核苷(酸)类似物可能导致快速抑制HBV的复制,使血清转氨酶正常化,恢复肝功能,从而提高肝功能失代偿患者的生存周期。长期的核苷(酸)类似物疗法可能改善肝组织学,逆转肝纤维化,减少疾病进展,如肝癌。
干扰素(IFN)-α有限的治疗周期可以带来长远利益,包括持续和累积的病毒学反应,以及乙型肝炎表面抗原(HbsAg)血清清除和减少肝硬化和/或肝癌的发生。聚乙二醇化干扰素(PEG-IFN)和更新的Nucs药物可能会达到更好的长期结果,因为它们的功效得到改善,而且耐药性产生的风险较低。但是,这些药物的治疗效果还远远不能令人满意。另外,了解肝癌切除后或肝移植抗后,HBV治疗对肝癌的发病率和复发的影响需要进一步的研究。
乙型肝炎病毒(HBV)是嗜肝病毒家族的成员。全球有超过20亿人感染HBV.HBV感染是肝硬化和肝细胞癌产生的主要原因。肝细胞癌(HCC)增加了这些患者的发病率和死亡率。HBV在肝细胞中复制。HBV感染者HCC的风险是非感染者的10到100倍。
HBV感染诱导慢性炎症和癌症发生
HBV可以在永生化肝细胞中持续复制,而且不出现明显的细胞损伤或死亡。这意味着该病毒不能直接导致细胞病变,肝炎的发病机制是免疫介导的。肝损伤是由于炎性肝炎引发的炎症反应,这一反应主要由非实质细胞(NPC)参与,如髓系的枯否(Kupffer)细胞和肝星状细胞。
Toll样受体核因子(NF)-κB信号激活可能引发先天性免疫应答,从而抑制病毒在HBV转基因小鼠中的复制。NPC分泌的NF-κB调节肝有丝分裂原[如肿瘤坏死因子(TNF-α),白细胞介素(IL-6)和肝细胞生长因子],这促进了静态肝细胞的代偿性增生。这些肝细胞携带HBV诱导的突变。这个过程允许基因的改变转移到子细胞中,从而有利于肝肿瘤的进展。
另外,肝细胞转化生长因子(TGF-β)的自分泌可以诱导细胞存活和增殖,却无肝脏损伤,与NPC-介导的肝有丝分裂原分泌无关。增殖的增加会导致不典型增生,腺瘤和肝癌的形成。总之,NF-κB活化相关的致癌作用可能依赖于下游的肝丝裂原的释放和代偿性增殖。
HBV X(HBx)蛋白是由乙肝病毒开放读码框编码的最小蛋白,有154个氨基酸,约17.5 kDa的分子量。 HBx蛋白可以定位到线粒体,作为一个适配器或激酶激活剂影响信号通路的转导,如:蛋白激酶C,JAK / STAT的激活剂,SAPK / JNK,RAS- RAF- MAPK,ERK.这可能是HBx蛋白发挥多重功能的统一机制,包括转录,细胞周期调控和凋亡。
此外,据报道该HBx蛋白能够直接激活NF-κB通路,这可能是通过NF-κB激酶活性的抑制剂的上调和雷帕霉素蛋白(mTOR )途径。如上所述,各种炎性细胞因子,包括TNF-α, IL- 1α ,IL- 1β,IL- 6和IL- 8在肝脏的炎症,癌变中起重要作用。这些细胞因子都是NF-κB介导活化的,其中IL-6是最重要的。最近,研究人员发现,IL- 22也可以通过STAT3的活化促进肝癌的发生,这表明炎性细胞因子作为炎症与肝癌的中介得到了相当多的关注。
此外, HBx蛋白可通过其它炎性细胞干扰抗肿瘤的免疫应答。受感染的肝内自然杀伤(NK)细胞可以诱导细胞溶解活性却无IFN- γ的产生,这表明肝细胞的死亡无法清除病毒。树突状细胞可能感染HBV,这将导致有缺陷的慢性HBV感染,导致较差的适应性免疫。 CD4 + CD25 + FOX3P +调节性T细胞可以通过HBx的刺激诱导产生TGF-β1,并且它们与Th17细胞的相互作用有助于在肝脏中形成免疫耐受和清除的平衡。
乙肝相关性肿瘤发生机制
越来越多的证据表明,乙肝病毒可以通过直接调节途径促进肝细胞的恶性转化。首先,乙肝病毒的插入与大量的宿主遗传变异有关:缺失,重复和染色体易位。这些事件既可以诱导染色体在表达或功能的改变,还可以有助于产生染色体不稳定性的改变。例如,HBx基因片段的插入(316-462/262-462 bP)直接使人类正常肝L02细胞变换为永生细胞模型。
此外,在44项临床HBV阳性的肝癌组织中有5项检测到这些组合方式。在宿主基因特异位点的整合可能有助于产生有生长优势的克隆细胞群,但随后额外的突变会得到累积。
在两个独立的肝癌组织中,研究人员发现视黄酸受体和细胞周期蛋白A为乙肝病毒整合的目标。最近,更多参与细胞存活,增殖和永生化的基因也被报告为乙肝病毒整合的目标。如人端粒酶逆转录酶(hTERT ,端粒酶的调节器),血小板衍生生长因子受体,钙信号传导相关基因,以及核糖体蛋白基因。
虽然有人建议HBx蛋白和HBV S蛋白的表达上调,在转基因小鼠模型中与肝癌的发生率相关,但具体的机制仍不清楚。值得注意的是,在肝硬化的肝脏中肝细胞增殖下降。复制性衰老表型占主导地位,特点是端粒缩短和永久的细胞周期停滞。然而,在肝细胞增生时,肝硬化时低或无端粒酶活性与HBx或前-S2蛋白的上调相关。在55名肝癌患者和17名慢性肝炎患者的研究中,肝癌的81%端粒酶阳性,而肝癌的平均端粒长度与慢性肝炎相比较显著缩短。
HBx蛋白可通过干扰有丝分裂的主要关卡,使染色体不稳定。 HBx蛋白诱导的表观遗传变化,包括DNA甲基化畸变,组蛋白修饰和miRNA的表达。 Jiang等人报道,在男性患者中miR – 22表达量的增加与肝癌发展相关。 Xu等人的研究认为:HBx激活可以抑制miR- 148A从而增加肿瘤的发生率。此外, HBx蛋白结合和失活p53,并与DNA损伤结合蛋白1(DDB1,DNA修复蛋白质)的相互作用,可能影响DNA的修复功能,从而使遗传改变得到积累,产生耐药性突变和抗肿瘤药物的突变。
抗病毒药物治疗的现状
在过去的十年中,抗HBV的治疗得到显着改善。目前治疗慢性HBV感染是基于两种不同的策略:(1) IFN-α或者胸腺素-A1(T- a1),旨在诱导产生持续的抗病毒反应,以及( 2)口服抗乙肝病毒的核苷(酸)类似物,实现对HBV复制的长期完全抑制。
第一种策略是通常在轻度肝病的患者中使用,这些患者具有很高的谷丙转氨酶(ALT)和不太高的HBV DNA复制。这种治疗在年轻患者和那些感染HBV基因型A或B的患者中特别成功。由于首次使用IFN- α是在1976年,干扰素治疗的长远利益已经包括了持续累积免疫响应。T- a1是一种免疫调节剂,它可以触发淋巴细胞和T细胞功能的成熟。它能促进免疫缺陷重建和HBV复制相关疾病的缓解。在乙肝患者e抗原(HBeAg)阳性慢性B型肝炎中停止病毒复制,而且无显著副作用。
18例HBeAg阳性和血清HBVDNA阳性的慢性乙型肝炎患者接受6个月的T- A1治疗。每周两次皮下注射1.6毫克T- A1.30例患者接受6个月的3-5 MU皮下IFN-α(每日注射15 d后,每周三次)。接受T- A1的患者取得了较好的HBV载量的减少和血清转换结果。本试验的结果表明, T型A1是潜在抗-HBe和HBV DNA阳性的患者中具有良好的效果。
对IFN- α2b加入12 - kDa的线性聚乙二醇(PEG)和干扰素-α2A的40 - kDa的分支PEG.使干扰素的注射周期从已经从每天或每周三次延长到每周一次。从而明显改善了药物的耐受性和易用性。
此外,HBeAg阳性慢性乙型肝炎患者,聚乙二醇化干扰素(PEG IFN-α2A)的疗效比拉米夫定更好。这主要体现在HBeAg血清转换, HBV DNA抑制,和B型肝炎表面抗原(HBsAg)的血清转化。总体而言,PEG的IFN-α是HBeAg阴性的慢性B型肝炎患者的一种理想的治疗选择。由于其公认的和可预测的安全性和抗病毒活性的独特机制,从而导致长期持久的免疫控制。
对于那些高HBV DNA水平的患者,通常使用核苷(酸)类似物。还有那些伴随有严重的肝脏疾病,干扰素治疗失败或不能耐受的患者主要使用核苷(酸)类似物。然而,主要的限制是耐药性的产生:例如,5年的拉米夫定( L-核苷)治疗后, 76%的患者出现耐药性。替比夫定,另一种L-核苷,强于拉米夫定。经过2年治疗后,HBeAg阳性的患者25%, HBeAg阴性的患者有11%出现耐药性。
阿德福韦,一种无环膦酸盐,抗病毒能力相对较弱,但对拉米夫定和替比夫定耐药性突变的病毒有效。使用的方式应当为组合,而不是取代。耐阿德福韦的发展相对缓慢,在HBeAg阴性的患者中使用阿德福韦5年后,耐药性上升到29%。单独使用时,耐药突变产生更快。
目前,两个一线Nucs是恩替卡韦和替诺福韦。恩替卡韦,环戊烷(D-核苷),是非常有效的抗病毒药物,5年后有94%的患者使HBV DNA降低到检测线以下。而耐药性只有1.2%。替诺福韦,另一个无环核苷酸,更强大的的抗病毒活性但与阿德福韦相比具有较少肾毒性。它可以单独使用,且对拉米夫定耐药突变有效。替诺福韦在3年或更长的时间不产生耐药性。
总之, HBeAg阳性慢性B型肝炎的患者,PEG IFN-α提供了优越的疗效。有较好的HBeAg血清转换,HBV DNA抑制和HBsAg血清学转换。新的治疗方案PEG IFN-α和第三代Nucs如恩替卡韦和替诺福韦,可以增加HBsAg清除的速率。
抗病毒治疗抑制慢性炎症到癌症的过渡
有一项11年随访的前瞻性队列研究,表明HBV DNA浓度> 104拷贝/ mL是30岁以上出现肝癌风险的一个预测指标,且与血清ALT水平无关。有一点可以肯定的是抗乙肝病毒治疗可以改善慢性HBV感染的临床结局,特别是在肝癌的发病率方面。
在一项台湾地区的101例男性患者的随机对照试验中,IFN-α治疗组(67例中有1例)在1.1-11.5年治疗后比对照组(34例里有4例)的肝癌累积发生率显著下降。此外,一项回顾性研究表明:天然类淋巴母IFN-α(IFN-αNL)和IFN疗法可能会提供更好的长期的有利影响。比安慰剂HBV清除,减少方面肝癌,并延长生存期。干扰素-αNL组中的1.5%,IFN-α2A组的3.7%,对照组的14.7%出现肝癌。
至于Nucs的长期利益,在一个随机对照试验,拉米夫定治疗组的肝癌发生率为3.9%,而对照组的发生率为7.4%。这项研究共纳入651例患者(HR = 0.49,P = 0.047)。
在656例HBeAg阴性患者(54%有慢性肝炎,30%有肝硬化),拉米夫定治疗组(中位数22月,范围为1-66 ),可以有效减少病毒载量,降低肝癌的发展和肝硬化患者的疾病恶化。
一个韩国研究还表明代偿期的肝硬化患者HCC的发生率。拉米夫定治疗组(4.9%)与未经治疗的病人相比减少。在最近的一项系统性回顾,回顾了21项研究,包括3881治疗和未经治疗的534例患者,结果发现肝癌在核苷(酸)类似物治疗的患者中较少( 2.8%对6.4%,P < 0.003)。
在一项对比IFN和核苷(酸)类似物疗法效果的系统评价中,在过去的10年间,宋等人[ 46 ]的研究表明IFN- α或核苷(酸)类似物治疗可以显著降低肝癌的风险。
虽然干扰素使肝硬化患者收益更大, Nucs使那些与非肝硬化和HBeAg阳性得患者收益更大。但是这两种治疗方法都可以持续抑制HBV的复制,从而以减少肝癌的发生率。
抗病毒治疗对HCC复发的影响
抗乙肝病毒治疗是否可以减少肝癌的复发风险的最有效的方法,从而减少肿瘤负担:部分肝切除或肝移植?如此前建议,对于所有早期肝癌患者的5年总生存率为58%(移植:63%;切除术:53%)。 Huang等[ 48 ]报道,与患者肝切除术后HBV再激活有较高的肝衰竭发生率,较低的3年无病生存率和较低的总生存率(11.8%对6.4%,P = 0.002,34.1%比46.0%,P = 0.009和51.6%比67.2%,P <0.001)。
探索性亚组分析显示,辅助IFN-α对pTNM分期Ⅰ/Ⅱ期肿瘤无生存获益(两个组的5年存活率在90%左右,P = 0.917)。但可以防止肿瘤的早期复发,使Ⅲ/ ⅣA肿瘤患者的5年生存期由24 %的肿瘤提高到68%(P = 0.038)。 Lee等人也报道,肿瘤转移相关蛋白1阳性肝癌术后复发率为28%(93名患者中有26名),尽管PEG干扰素组有显著降低整体累积复发率低于对照组(在1年和2年,分别为7%和14%比24%和34%,P < 0.05)。
此外,PEG IFN治疗组1 年和2年累积生存率分别高于对照组(100%对93%和100%对87%,P <0.05)。在一项237例肝癌切除术后的HCC报告中,IFN-α组的中位总生存期为63.8月,安慰剂组为38.8月(P = 0.0003),中位无病生存期为31.2与17.7个月(P = 0.142)。 Chen等人的结果表明佐剂干扰素-α2b的治疗并没有减少术后病毒性肝炎相关的肝细胞癌复发。
关于Nucs对肝癌复发的效果,安塞尔莫等认为乙肝免疫球蛋白(HBIG)和拉米夫定治疗可以显著降低乙肝复发率,显著提高肝移植术后1年和3年无复发生存率。Chan等人也报道,1年,3年和5年无病生存率与拉米夫定或恩替卡韦治疗的患者分别为66.5%,51.4%和51.4%,48.9%,33.8%和33.8%。 Kubo等[55]报道,拉米夫定治疗组切除后无瘤生存率显著高于对照组。最近,多因素分析显示,移植后HCC复发与乙肝病毒再感染有关。然而,乙肝免疫球蛋白是与不良预后相关以及乙肝病毒再感染和HCC复发相关(P= 0.002 , P <0.01和P < 0.001)。
在研究人员所在的中心(肝脏移植中心,南京医科大学附属第一医院),研究结果表明,HBV DNA拷贝/mL > 104或103-104/mLHBsAg阳性患者可使肝脏功能受损,必须在根治性手术后采取拉米夫定。
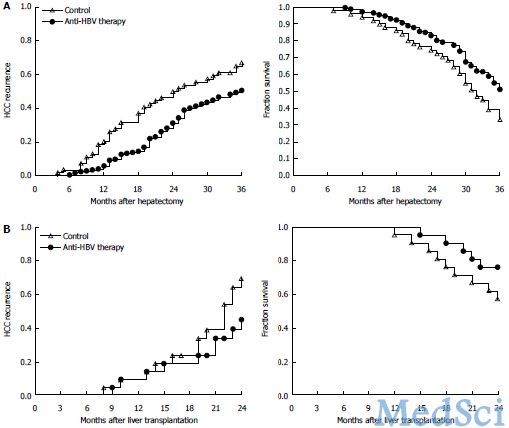
图1 肝部分切除和肝移植患者使用抗HBV治疗和安慰剂治疗后HCC的复发率和临床结局的比较
此外,对于那些有YMDD变异的乙型肝炎病毒的初始治疗,恩替卡韦和/或阿德福韦酯应该被用作替换。如果出现耐药性,可以使用富马酸替诺福韦酯。在研究人员的随机对照临床研究中,研究人员验证了对于接受部分肝切除和肝移植患者,标准化的抗乙肝病毒治疗可显著提高疗效,降低复发率。
结论
该文献从两个不同的方面描述了慢性HBV感染的肿瘤发生机制:通过HBV DNAHBx蛋白直接诱导宿主DNA不稳定;和HBV感染相关的肝脏炎症和免疫调节失衡。文章还简要介绍了当前对HBV感染的治疗方法,同时表明,在慢性HBV感染中及时使用Nucs和免疫调节剂,可以防止疾病进一步恶化,包括肝癌。
长期研究可能会确认新的抗病毒药物,如恩替卡韦,替诺福韦和替比夫定能提供更为减少优于拉米夫定疾病进展的机会治疗。对于接受肝切除或肝移植的患者,肿瘤复发必须通过超声和α-胎蛋白来监视。更重要的是,从我们的经验看,也应进行监测HBV复制情况。因为持续乙肝病毒激活或复发与肝癌发展和复发显著相关。标准化的抗HBV最终的治疗可延缓肝癌复发和效益生存。
由于PEG-IFN为那些没有肝硬化或纤维化的患者提供一个更好的机会,来抑制HBV的复制。它给患者在降低肝癌的发展和复发方面提供了广阔的前景。虽然在许多第三世界国家,拉米夫定仍是一线药物,未来可以大规模使用新开发的干扰素,从而展现更美好的前景。
总之,开发安全和负担得起的药物,维持乙肝病毒抑制的治疗措施,应该是慢性HBV感染治疗的最终目标。
原始出处:
Tan ZM, Sun BC.Effects of antiviral therapy on preventing liver tumorigenesis and hepatocellular carcinoma recurrence.World J Gastroenterol. 2013 Dec 21;19(47):8895-901. doi: 10.3748/wjg.v19.i47.8895.【原文下载】
作者:佚名
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言





#肿瘤形成#
50
#肝脏肿瘤#
0
#抗病毒#
42
#抗病毒治疗#
44