ACS Appl Mater Interfaces:近红外激发新型纳米粒子或可有效治疗三阴乳腺癌
2017-09-21 MedSci MedSci原创
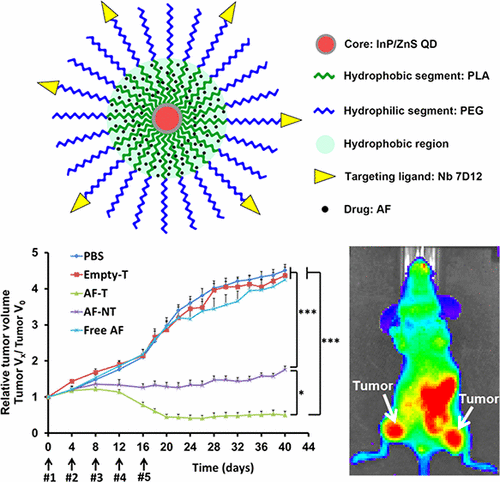
基于量子点(QD)的胶束与抗表皮生长因子受体(EGFR)纳米体(Nb)结合再负载抗癌药物氨基黄酮(AF),被研制用于EGFR过表达的癌症治疗。近红外(NIR)荧光激发磷酸铟核心/硫化锌壳量子点(InP/ZnS QDs)可探究体内纳米粒子的生物分布。抗EGFR纳米体7D12共轭改善了EGFR过表达MDA-MB-468三阴性乳腺癌(TNBC)细胞中基于QD胶束的细胞摄取和细胞毒性。与AF封装的非靶向(
基于量子点(QD)的胶束与抗表皮生长因子受体(EGFR)纳米体(Nb)结合再负载抗癌药物氨基黄酮(AF),被研制用于EGFR过表达的癌症治疗。近红外(NIR)荧光激发磷酸铟核心/硫化锌壳量子点(InP/ZnS QDs)可探究体内纳米粒子的生物分布。
抗EGFR纳米体7D12共轭改善了EGFR过表达MDA-MB-468三阴性乳腺癌(TNBC)细胞中基于QD胶束的细胞摄取和细胞毒性。与AF封装的非靶向(即没有Nb共轭)胶束相比,AF-包封的Nb-缀合的(即靶向)胶束以较高浓度在肿瘤中积聚,导致原位三阴性乳腺癌异种移植小鼠模型中肿瘤更有效的消退。此外,治疗没有观察到全身毒性。
因此,这种基于QD的Nb-共轭胶束可以用作EGFR过表达癌症(如TNBCs)的有效治疗选择。
原始出处:
Yuyuan Wang, Yidan Wang., et al., Quantum-Dot-Based Theranostic Micelles Conjugated with an Anti-EGFR Nanobody for Triple-Negative Breast Cancer Therapy. ACS Appl. Mater. Interfaces, 2017, 9 (36), pp 30297–30305.
作者:MedSci
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#纳米粒#
33
#ACE#
35
#FAC#
34
#近红外#
43
#ACS#
46