CRISPR编辑的CAR-T细胞疗法增强了对抗血癌的能力
2020-12-08 Allan MedSci原创
宾夕法尼亚大学医学院研究人员的最新临床前数据显示,使用CRISPR / Cas9技术敲除一种已知可抑制T细胞活化的蛋白,从而增强了工程T细胞消除血液癌的能力。
宾夕法尼亚大学医学院研究人员的最新临床前数据显示,使用CRISPR / Cas9技术敲除一种已知可抑制T细胞活化的蛋白,从而增强了工程T细胞消除血液癌的能力。研究结果已在12月7日第62届美国血液学会(ASH)年度会议上展示。
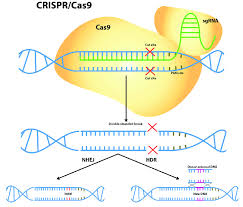
研究小组使用CRISPR-Cas9敲除了CAR-T细胞上的CD5基因,该基因编码T细胞表面的CD5蛋白并可以抑制其活化,然后将其注入患有T细胞和B细胞白血病的小鼠中。与注入未经编辑的CAR-T细胞的小鼠相比,注入CD5缺失的CAR-T细胞的小鼠在外周血中具有更高水平的T细胞增殖,并且肿瘤大小显著减少,其存活率更高。
CRISPR技术使科学家能够定位和编辑任何不需要的基因。该方法与CAR-T细胞疗法密切相关,在CAR-T细胞疗法中,研究人员采集患者自身的T细胞,并对其进行基因改造,使其表达出能够寻找并攻击癌细胞的新受体。
宾夕法尼亚大学佩雷尔曼医学院血液肿瘤学部门Marco Ruella博士说:“我们首次证明,使用CRISPR-Cas9敲除CAR-T细胞上的CD5能够增强其攻击癌症的能力。在几种癌症模型中,编辑过的和未编辑过的CAR-T细胞存在惊人差异”。
原始出处:
作者:Allan
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#CAR-#
45
#CRISPR#
42
#Car-T细胞疗法#
42
#T细胞疗法#
44
#血癌#
35