ViiV两月一次长效注射剂cabotegravir用于预防HIV,获得FDA的突破性疗法称号
2020-11-19 MedSci原创 MedSci原创
与每日口服FTC/TDF片剂相比,cabotegravir预防HIV的效率提高了66%。
葛兰素史克(GlaxoSmithKline)子公司ViiV Healthcare宣布,其两月一次的长效注射剂Cabotegravir预防HIV,获得美国食品和药物管理局(FDA)的突破性疗法称号(BTD)。
BTD是基于IIb/III HPTN 083期试验的结果,该试验比较了Cabotegravir与HIV暴露前预防性用药(PrEP)标准治疗药物——每日一次口服药物Truvada(FTC/TDF,恩曲他滨/替诺福韦,200mg/300mg片剂)对HIV的预防效果。
研究结果显示,与每日口服FTC/TDF片剂相比,cabotegravir预防HIV的效率提高了66%,cabotegravir组HIV发生率为0.41%,FTC/TDF组的HIV发生率为1.22%。
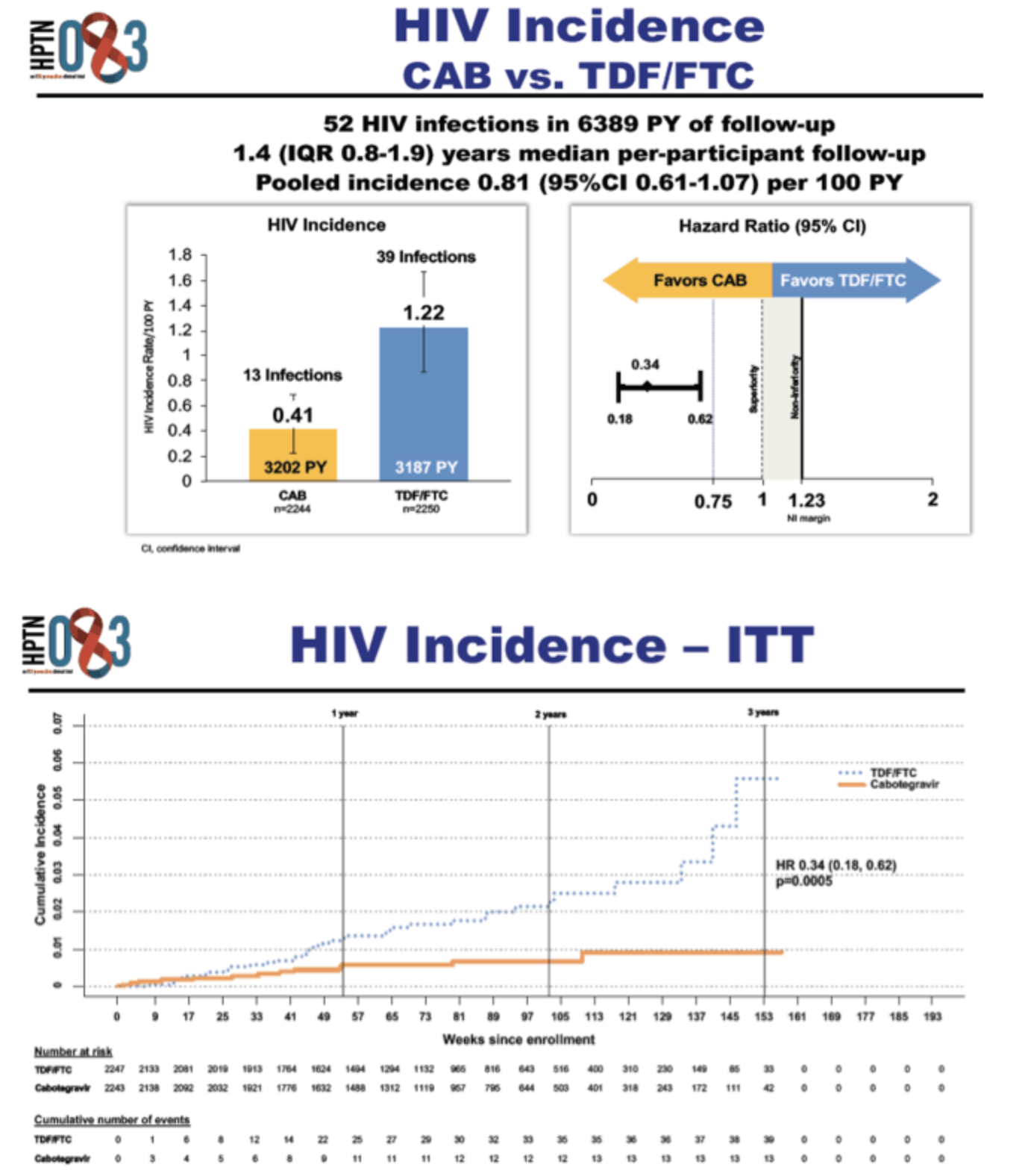
图片来源:https://www.natap.org/2020/IAC/IAC_28.htm
根据ViiV的数据,目前约有3800万人感染艾滋病毒,2019年底报告了170万艾滋病毒新发病例。
原始出处:
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#突破性疗法称号#
44
#Cabotegravir#
0
#注射剂#
32
#突破性疗法#
56
#ABO#
39