Oncogene:河北医科大学赵群/孟令娇合作发现新型circRNA在胃癌中促进淋巴结转移
2024-08-21 iNature iNature
该研究发现了一种新的N6-甲基腺苷(m6A)修饰的circRNA,circPAK2,它在胃癌组织和转移性LN组织中显著上调。
环状RNA(circRNA)已成为癌症发生和进展的关键调控因子,也是癌症诊断和预后的有希望的生物标志物。然而,与胃癌淋巴结(LN)转移有关的circRNA的潜在机制仍不清楚。
2024年7月17日,河北医科大学赵群、孟令娇共同通讯在Oncogene 在线发表题为“N6-methyladenosine modified circPAK2 promotes lymph node metastasis via targeting IGF2BPs/VEGFA signaling in gastric cancer”的研究论文。该研究发现了一种新的N6-甲基腺苷(m6A)修饰的circRNA,circPAK2,它在胃癌组织和转移性LN组织中显著上调。
功能上,circPAK2在体内和体外增强胃癌的迁移、侵袭、淋巴管生成、血管生成、上皮-间质转化(EMT)和转移。机制上,circPAK2由含YTH结构域的蛋白1(YTHDC1)以m6A甲基化依赖的方式从细胞核输出到细胞质。此外,增加的细胞质circPAK2与胰岛素样生长因子2mRNA结合蛋白(IGF2BPs)相互作用并形成circPAK2/IGF2BPs/VEGFA复合物以稳定VEGFAmRNA,这有助于胃癌血管形成和侵袭性。临床上,高circPAK2表达与胃癌淋巴结转移和预后不良呈正相关。本研究强调了m6A修饰的circPAK2是胃癌淋巴结转移的关键调节因子,从而支持circPAK2作为胃癌有希望的治疗靶点和预后生物标志物。

胃癌是消化系统常见的恶性肿瘤,死亡率和发病率较高。尽管治疗方法取得了重大进展,但胃癌患者的总体存活率仍然很低。癌症复发和转移是胃癌相关死亡的主要原因。值得注意的是,超过70%的患者在诊断时出现淋巴结(LN)转移,这种情况与预后不良密切相关,因此5年生存率仅为30%。因此,开发能够准确预测胃癌淋巴结转移的新型生物标志物势在必行。在淋巴结转移性疾病中,淋巴管会发生重大变化,包括淋巴管生成,即从现有淋巴管中形成新淋巴管的过程。虽然淋巴管生成在肿瘤淋巴结转移中起着至关重要的作用,但胃癌中涉及的具体机制尚未完全阐明。因此,研究胃癌淋巴结转移的调控机制对制定更有针对性和更有效的治疗策略至关重要。
环状RNA(circRNA)是一类具有闭合单链环结构的新型RNA转录本,主要由真核生物基因组中外显子的前体mRNA(pre-mRNA)反向剪接产生。在发现之初,circRNA曾被认为是错误剪接的副产物,几乎没有生物学功能。最近发现,circRNA参与了各种生理和病理过程,包括恶性癌症进展。在胃癌中,发现circNFATC3通过与IGF2BP3相互作用并抑制其泛素化来增强CCND1的mRNA稳定性,从而增强细胞增殖。据报道,circPDIA4还通过与ERK1/2相互作用并限制由DUSP6介导的去磷酸化,从而激活MAPK通路,促进胃癌进展。相反,circIPO7通过竞争性结合caprin-1,诱导EGFR和mTOR的翻译抑制,从而抑制PI3K/AKT/mTOR通路,抑制肿瘤增殖。
circURI1通过与异质性核糖核蛋白M(hnRNPM)相互作用,调控胃癌的选择性剪接,抑制细胞迁移、侵袭和转移。然而,以上研究涉及的circRNA的机制主要集中在它们与蛋白相互作用,介导下游通路的靶向调控。进一步了解胃癌中circRNA的表观遗传修饰状态,可能有助于理解胃癌的发生和转移。众所周知,N6-甲基腺苷(m6A)是哺乳动物中最普遍、特征最明显的转录后RNA修饰,可以影响RNA剪接、翻译、稳定性以及某些非编码RNA的表观遗传效应。因此,针对环状RNA中m6A修饰的研究已成为近年来肿瘤领域的重要组成部分,迫切需要在胃癌中深入探索。
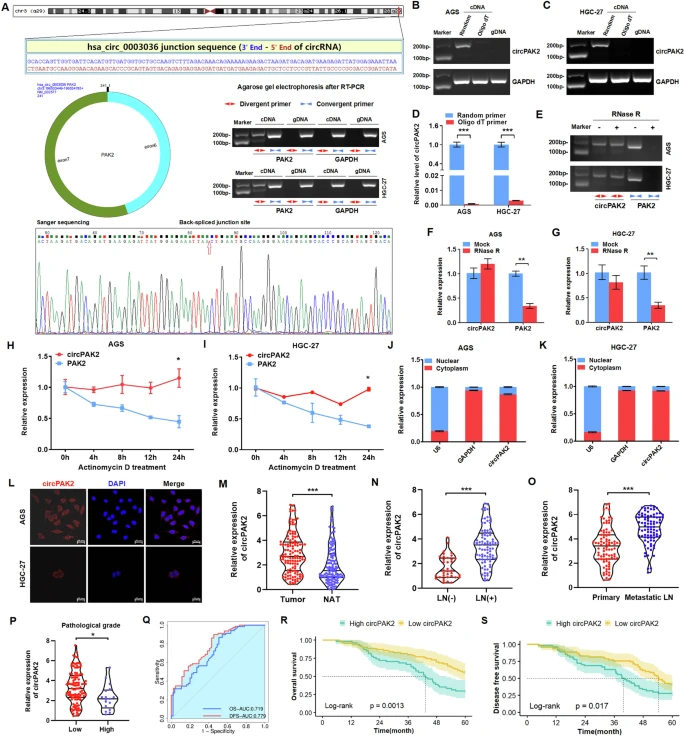
circPAK2在胃癌细胞和组织中的特点(图源自Oncogene )
在本研究中,作者通过分析胃癌中circRNA的表达谱,鉴定出一个由PAK2基因外显子6和7产生的新型circRNA,hsa_circ_0003036,被指定为circPAK2。与匹配的邻近正常组织相比,CircPAK2在胃癌组织中经常上调,与原发性组织相比,在转移性LN组织中也上调。功能上,circPAK2在体内和体外增强胃癌的迁移、侵袭、淋巴管生成、血管生成、上皮-间质转化(EMT)和转移。作者进一步证明circPAK2通过含YTH结构域的蛋白1(YTHDC1)从细胞核输出到细胞质,以m6A甲基化依赖的方式。此外,增加的细胞质circPAK2通过与胰岛素样生长因子2mRNA结合蛋白(IGF2BPs)结合来促进VEGFAmRNA的稳定性,从而促进胃癌血管形成和侵袭性。临床上,高circPAK2表达与胃癌淋巴结转移和预后不良呈正相关。这些数据表明circPAK2可能作为胃癌患者淋巴结转移的潜在预测因子和胃癌有希望的治疗靶点。作者期望作者的研究结果将为胃癌的临床管理提供新的见解。
参考消息:
https://www.nature.pubapi.xyz/articles/s41388-024-03099-w
作者:iNature
版权声明:
本网站所有注明“来源:梅斯医学”或“来源:MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明“来源:梅斯医学”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#胃癌# #淋巴结转移# #circRNA#
64